Clear Sky Science · he
מבנה ומנגנון של הליגאז HECT מסוג HECTD3
כיצד התאים מסמנים את חלבוניהם לפעולה
בתוך כל תא פועל מערכת איתות זעירה שמחליטה אילו חלבונים יתוקנו, מוּבזרים או יותאמו למשימות חדשות. המחקר הזה מתמקד באחת האנזימים שמנהלים את המערכת הזו, חלבון בשם HECTD3. HECTD3 נקשר לסרטן, לדלקת ולזיהומים ויראליים, אך האופן שבו הוא פועל ברמת האטום נותר לא ברור. על ידי שילוב כלים הדמייתיים וביוכימיים רבי‑עוצמה, המחברים חושפים כיצד HECTD3 בנוי, כיצד הוא בוחר את שותפיו המולקולריים וכיצד הוא מעטר חלבונים אחרים בתגים קטנים שיכולים לשנות את גורלם.
מכונת סימון תאית עם תפקידים רבים
תאים משנים לעיתים קרובות את חלבוניהם במולקולה קטנה בשם יוביקוויטין, שיכולה לפעול כמו תג צבעוני במחסן מיון. רצפים של תגים אלה, המסודרים בדרכים שונות, משדרים מסרים שונים: חלקם מסמנים חלבון להשמדה, אחרים מווסתים את פעולתו או מיקומו. אנזימים שנקראים E3 ליגאזים אחראים על בחירת החלבונים שמסומנים ואופן הסימון. HECTD3 משתייך לענף של E3 ליגאזים הידוע ביצירת קשר כימי זמני עם היוביקוויטין לפני העברתו למטרה. הוא פעיל באופן חריג בכמה סוגי סרטן וקשור לתהליכים כמו מוות תאי מתוכנת, איתות חיסוני ורפליקציה ויראלית, אולם המבנה והלוגיקה התפקודית שלו היו במידה רבה בלתי ידועים.
אנזים שמוכן תמיד לפעולה עם צורה ייחודית
המבקשים שאלו תחילה האם HECTD3 מתנהג כמו מתג שניתן להדליקו או לכבותו. ליגאזים קרובים רבים מווסתים את עצמם על‑ידי קיפול לצורות החוסמות את הפעילות או על‑ידי הצמדות לאסמבלאים גדולים יותר. באמצעות בדיקות ביוכימיות וטכניקה שמודדת את גודל החלבון בתמיסה, הצוות מצא ש‑HECTD3 מתקיים בדרך כלל כעותק יחיד ולא נראה כי הוא סוגר את עצמו באמצעות עיכוב עצמי או צבירה יציבה. גם החלק הקטליטי הגרעיני וגם החלבון במלוא אורכו פעילים, עם העדפה ברורה לעבודה עם משפחה מסוימת של אנזימים מסייעים שמספקים את היוביקוויטין. משמעות הדבר היא ש‑HECTD3 למעשה "מוכן לפעולה" וסביר להניח שנשלט בתאים על‑ידי גורמים אחרים ולא על‑ידי עיכוב עצמי פשוט.
חשיפת ארכיטקטורה חלבונית חדשה
כדי להבין כיצד HECTD3 בנוי, המחברים השתמשו במיקרוסקופ אלקטרונים קפוא (cryo‑EM) ללכוד תמונות של מולקולות בודדות הקפואות בקרח דק. הם קבעו מבנים של החלבון לבדו ובמצב שבו מולקולת יוביקוויטין קשורה באופן יציב לאתר הפעיל שלו. הצילומים מראים ש‑HECTD3 קומפקטי ולא בצורת טבעת, עם אזור קטליטי קלאסי בעל שני לובוסים בקצה אחד ואזור N‑טרמינלי שהיה קודם לכן תעלומה בקצה האחר. החצי N‑טרמינלי מתגלה כיצירת שני קיפולים חדשים לחלוטין, שהמחברים קוראים להם D3NA ו‑D3NB, המסודרים כפלטפורמה הליקלית התומכת במודול DOC הקושר סובסטרט. כאשר היוביקוויטין טעון, הלובוסים הקטליטיים מאמצים סידור בצורת L ספציפי, ושאריות חומציות מסוימות ליד אתר הפעילות מסייעות להכין שרשראות הצד של החלבון הקולטות את התג. העבודה מראה שלמרות ש‑HECTD3 פועל לפי הכללים הכלליים של משפחת האנזימים שלו, הוא משתמש בשילוב מובחן של אלמנטים מבניים להשגת זאת.
כיצד HECTD3 מסמן את עצמו ואת היעדים שלו
בהמשך בחנו החוקרים אילו דפוסי יוביקוויטין HECTD3 יוצר. במקום לבנות שרשראות ארוכות מסוג יחיד, האנזים בעיקר מצמיד יחידות יוביקוויטין בודדות מרובות ושרשראות קצרות, עם ראיות לחלק משרשראות המעדיפות קישוריות הידועה כמקדמת פירוק חלבונים. הדבר מצביע ש‑HECTD3 טוב יותר בפתיחת אירועי סימון מאשר בהארכתם לאותות ארוכים. המחברים פנו אז לחלבון יעד מוצע בשם PARP1, גורם תיקון DNA שכבר ידוע כי משפיע על תגובות לטיפולי סרטן. בתגובות במבחנה, HECTD3 שינה ביעילות את PARP1, ובעטף מספר שיירי ליזין בחצי הקושר‑DNA שלו בתגים שכוללים שרשראות המקושרות להסרת חלבונים. באמצעות צימוד כימי ומשרעת ספקטרומטרית מסה מיפו נקודות מגע בין HECTD3 ל‑PARP1, ואישרו שמודול ה‑DOC והאזור הקטליטי מסייעים למקם את הסובסטרט. מוטציה בשני חומצות אמינו חשופות על פני שטח ה‑DOC הקטינה באופן חמור את סיפון ה‑PARP1 מבלי לפגוע בכימיה הגרעינית, מה שמדגיש אותן כעוגנים מרכזיים להכרה בסובסטרט.
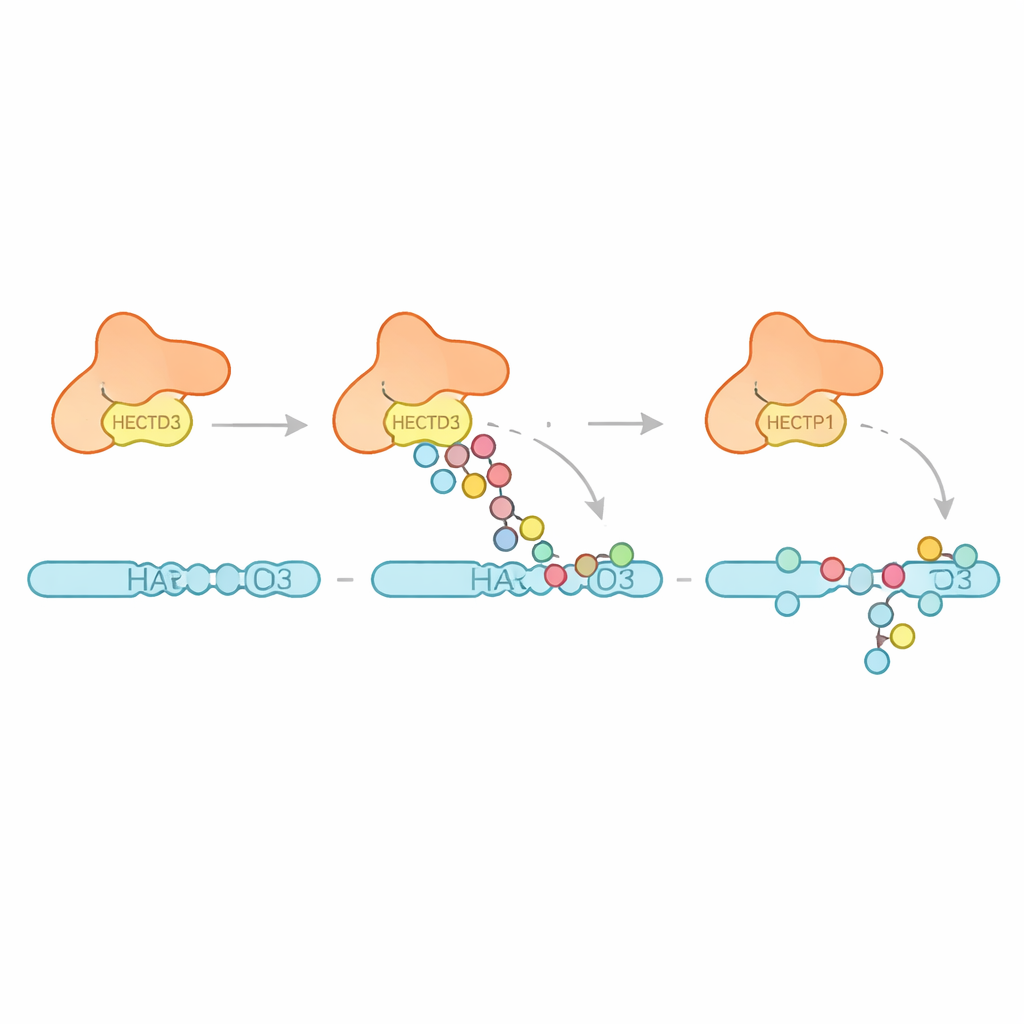
מדוע זה חשוב למחלה ולטיפול
ביחד, ממצאים אלה מציירים את HECTD3 כמכונת סימון פעילה תמיד אך מתוחכמת מבחינה מבנית, שמתחילה בעיקר את סימוני היוביקוויטין ומתבססת על חצי N‑טרמינלי גמיש וייחודי כדי לזהות שותפים ספציפיים כמו PARP1. מאחר שפעילות HECTD3 מוגברת במספר סוגי סרטן ומשפיעה על אופן הטיפול בחלבוני תיקון ה‑DNA, הבנת המבנה והמנגנון שלו פותחת דלתות לתכנון מולקולות שיפריעו למשטחי העיגון שלו או למרכז הקטליטי. התערבויות ממוקדות כאלה יכולות, בתיאוריה, לשנות את האופן שבו תאים קובעים את גורל החלבונים הקריטיים במצבים של סרטן, זיהום ומחלה דלקתית.
ציטוט: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
מילות מפתח: ליגאז יוביקוויטין, HECTD3, סימון חלבונים, PARP1, ביולוגיית סרטן