Clear Sky Science · ru
Структура и механизм лигазы HECT HECTD3
Как клетки маркируют свои белки для разных задач
Внутри каждой клетки работает крошечная сигнальная система, решающая, какие белки отремонтировать, переработать или перенастроить для новых функций. В этом исследовании внимание сосредоточено на одном из ферментов, управляющих этой системой — белке под названием HECTD3. HECTD3 связан с раком, воспалением и вирусными инфекциями, но его работа на атомарном уровне оставалась неясной. Сочетая мощные методы визуализации и биохимические инструменты, авторы показывают, как устроен HECTD3, как он выбирает молекулярных партнёров и как он помечает другие белки малыми метками, способными менять их судьбу.
Клеточная машина маркировки с множеством ролей
Клетки часто модифицируют свои белки небольшим молекулой, называемой убиквитином, которая может действовать как цветная метка на сортировочном складе. Цепочки таких меток, расположенные по-разному, посылают разные сигналы: одни помечают белок для разрушения, другие настраивают его активность или локализацию. Ферменты, называемые E3‑лигазами, отвечают за то, какие белки будут маркироваться и каким образом. HECTD3 относится к ветви E3‑лигаз, которые образуют временную химическую связь с убиквитином перед передачей его на мишень. Он необычно активен при нескольких типах рака и вовлечён в процессы, такие как программируемая гибель клеток, иммунная сигнализация и репликация вирусов, но его структура и принципы работы были в значительной степени неизвестны.
Постоянно активный фермент с уникальной формой
Исследователи сначала задали вопрос, ведёт ли себя HECTD3 как выключатель, который можно включать или выключать. Многие родственные лигазы сдерживают себя, сворачиваясь в самоблокирующиеся формы или объединяясь в большие комплексы. С помощью биохимических тестов и метода, измеряющего размер белков в растворе, команда обнаружила, что HECTD3 в основном существует в виде одиночной копии и, по-видимому, не выключается посредством самоблокировки или стабильного скопления. И его каталитическая часть, и полноразмерный белок активны, с явным предпочтением работать с одной семьёй помощников (E2), которые передают убиквитин. Это означает, что HECTD3 по сути «готов к работе» и, вероятно, регулируется в клетке не простыми механизмами самоблокировки.
Выявление новой архитектуры белка
Чтобы понять устройство HECTD3, авторы использовали крио‑электронную микроскопию, захватывая изображения отдельных молекул, замороженных в тонком льду. Они получили структуры белка в свободном состоянии и в состоянии, когда молекула убиквитина прочно прикреплена к его активному участку. Эти снимки показывают, что HECTD3 компактен, а не кольцеобразен, с классическим двухдольным каталитическим регионом на одном конце и ранее загадочной N‑концевой областью на другом. N‑концевая половина оказалась сформирована двумя полностью новыми фолдами, которые авторы называют D3NA и D3NB, расположенными как спиральная платформа, поддерживающая модуль DOC для связывания субстрата. Когда убиквитин загружен, каталитические дольки принимают характерную L‑образную конфигурацию, а специфичные кислые остатки рядом с активным центром помогают подготовить приходящие боковые цепи аминокислот для принятия метки. Работа показывает, что, хотя HECTD3 следует общим правилам своей семейства ферментов, он использует уникальное сочетание структурных элементов для их реализации.
Как HECTD3 помечает себя и свои мишени
Далее команда изучила, какие типы убиквитиновых меток создаёт HECTD3. Вместо того чтобы строить длинные цепи одного типа, фермент в основном прикрепляет несколько одиночных молекул убиквитина и короткие цепочки, с признаками некоторых связей, которые ассоциируются с направлением белка на разрушение. Это предполагает, что HECTD3 лучше запускает события маркировки, чем удлиняет их в длинные сигналы. Авторы затем обратились к предполагаемой мишени PARP1 — фактору репарации ДНК, уже известному тем, что влияет на ответы на онкотерапию. В пробирочных реакциях HECTD3 эффективно модифицировал PARP1, помечая несколько лизиновых сайтов в его ДНК‑связывающей половине метками, включая цепочки, связанные с удалением белка. С помощью химического перекрестного связывания и масс‑спектрометрии они отобразили точки контакта между HECTD3 и PARP1, подтвердив, что и модуль DOC, и каталитическая область помогают позиционировать субстрат. Замена двух выступающих аминокислот на поверхности DOC резко уменьшала маркировку PARP1, не нарушая основной химии, выделив эти остатки как ключевые анкеры для распознавания субъекта.
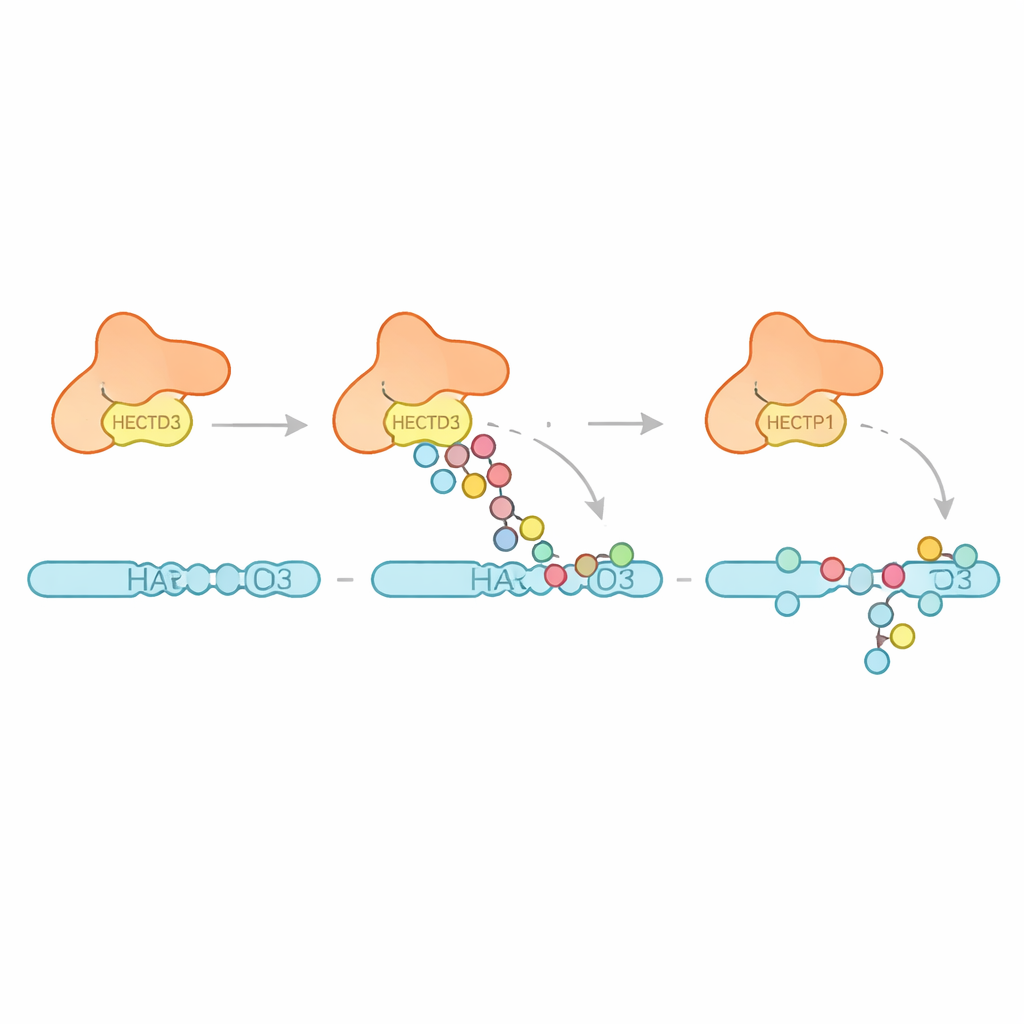
Почему это важно для болезней и терапии
В сумме эти результаты рисуют образ HECTD3 как постоянно активной, но структурно сложной машины маркировки, которая в основном инициирует убиквитиновые метки и опирается на гибкую, уникальную N‑концевую область для распознавания конкретных партнёров, таких как PARP1. Поскольку активность HECTD3 повышена при нескольких видах рака и влияет на обработку белков репарации ДНК, понимание его структуры и механизма открывает возможности для разработки молекул, мешающих его рецепторным поверхностям или каталитическому центру. Такие таргетные вмешательства теоретически могут изменить решения клетки о судьбе ключевых белков при раке, инфекциях и воспалительных заболеваниях.
Цитирование: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
Ключевые слова: убиквитинлигаза, HECTD3, маркеровка белков, PARP1, онкобиология