Clear Sky Science · nl
Structuur en mechanisme van de HECT-ligase HECTD3
Hoe cellen hun eiwitten labelen voor actie
In elke cel beslist een klein signaleringssysteem welke eiwitten gerepareerd, gerecycled of omgeprogrammeerd worden voor nieuwe taken. Deze studie richt zich op een van de enzymen die dit systeem aanstuurt, een eiwit genaamd HECTD3. HECTD3 is in verband gebracht met kanker, ontsteking en virale infectie, maar hoe het op atomair niveau werkt, bleef onduidelijk. Door krachtige beeldvormende en biochemische technieken te combineren, laten de auteurs zien hoe HECTD3 is opgebouwd, hoe het zijn moleculaire partners kiest en hoe het andere eiwitten voorziet van kleine labels die hun lot kunnen veranderen.
Een cellulair labelapparaat met veel rollen
Cellen modificeren hun eiwitten vaak met een klein molecuul genaamd ubiquitine, dat kan werken als een gekleurd label in een sorteerlager. Ketens van deze labels, in verschillende configuraties, sturen verschillende boodschappen: sommige markeren een eiwit voor afbraak, andere regelen de activiteit of locatie. Enzymen die E3-ligases worden genoemd, zijn verantwoordelijk voor het kiezen welke eiwitten gelabeld worden en op welke manier. HECTD3 behoort tot een tak van E3-ligases die een tijdelijke chemische binding met ubiquitine aangaan voordat ze het op een target overdragen. Het is ongewoon actief in meerdere vormen van kanker en is gekoppeld aan processen zoals geprogrammeerde celdood, immuunsignalering en virale replicatie, maar de structuur en werkingslogica waren grotendeels onbekend.
Een voortdurend actief enzym met een unieke vorm
De onderzoekers vroegen zich eerst af of HECTD3 zich gedraagt als een schakelaar die aan of uit gezet kan worden. Veel verwante ligases houden zichzelf in toom door in zelfblokkerende vormen te vouwen of door samen grotere assemblages te vormen. Met biochemische tests en een techniek die de grootte van eiwitten in oplossing meet, vonden ze dat HECTD3 voornamelijk als enkelvoudig exemplaar voorkomt en niet lijkt te worden uitgeschakeld door zelfremming of stabiele clustering. Zowel het kern-catalytische deel als het volledige eiwit zijn actief, met een duidelijke voorkeur voor samenwerken met één familie van helper-enzymen die ubiquitine overdragen. Dit betekent dat HECTD3 min of meer "klaar voor gebruik" is en waarschijnlijk in cellen gereguleerd wordt door factoren anders dan eenvoudige zelfblokkering.
Een nieuwe eiwitarhitectuur onthuld
Om te begrijpen hoe HECTD3 is opgebouwd, gebruikten de auteurs cryo-elektronenmicroscopie om beelden vast te leggen van enkele moleculen bevroren in een dunne ijslaag. Ze bepaalden structuren van het eiwit alleen en in een staat waarin een ubiquitinemolecuul stevig aan het actieve centrum is bevestigd. Deze momenten tonen dat HECTD3 compact is in plaats van ringvormig, met een klassieke tweelobbige katalytische regio aan het ene uiteinde en een eerder mysterieuze N-terminale regio aan het andere. De N-terminale helft blijkt twee volledig nieuwe vouwingen te vormen, die de auteurs D3NA en D3NB noemen, geordend als een helicaal platform dat een substraatbindende DOC-module ondersteunt. Wanneer ubiquitine geladen is, nemen de katalytische lobben een specifieke L-vormige configuratie aan, en specifieke zure residuen dicht bij het actieve centrum helpen inkomende eiwitzijdeketens voor te bereiden om het label te accepteren. Het werk toont dat, hoewel HECTD3 de algemene regels van zijn enzymfamilie volgt, het een unieke combinatie van structurele elementen gebruikt om dat te doen.
Hoe HECTD3 zichzelf en zijn doelwitten labelt
Vervolgens onderzocht het team welke soorten ubiquitinepatronen HECTD3 aanbrengt. In plaats van lange ketens van één specifiek type te bouwen, hecht het enzym vooral meerdere enkele ubiquitine-eenheden en korte ketens, met bewijs voor sommige ketens die een verbinding bevorderen die bekendstaat om eiwitafbraak te stimuleren. Dit suggereert dat HECTD3 beter is in het starten van labelingsgebeurtenissen dan in het uitbouwen ervan tot lange signalen. De auteurs richtten zich daarna op een voorgesteld doelwit, PARP1, een DNA-reparatiefactor die al bekendstaat om haar invloed op reacties op kankertherapie. In reageerbuisreacties modificeerde HECTD3 PARP1 efficiënt, waarbij meerdere lysineplaatsen in de DNA-bindende helft werden gelabeld met tags die ketens omvatten die geassocieerd zijn met eiwitverwijdering. Door chemische crosslinking en massaspectrometrie te gebruiken, brachten ze contactpunten tussen HECTD3 en PARP1 in kaart, waarmee werd bevestigd dat zowel de DOC-module als de katalytische regio helpen bij het positioneren van het substraat. Het muteren van twee blootliggende aminozuren op het DOC-oppervlak verminderde de PARP1-labeling scherp zonder de kernchemie te schaden, waarmee ze als cruciale ankerpunten voor substraatherkenning werden geïdentificeerd.
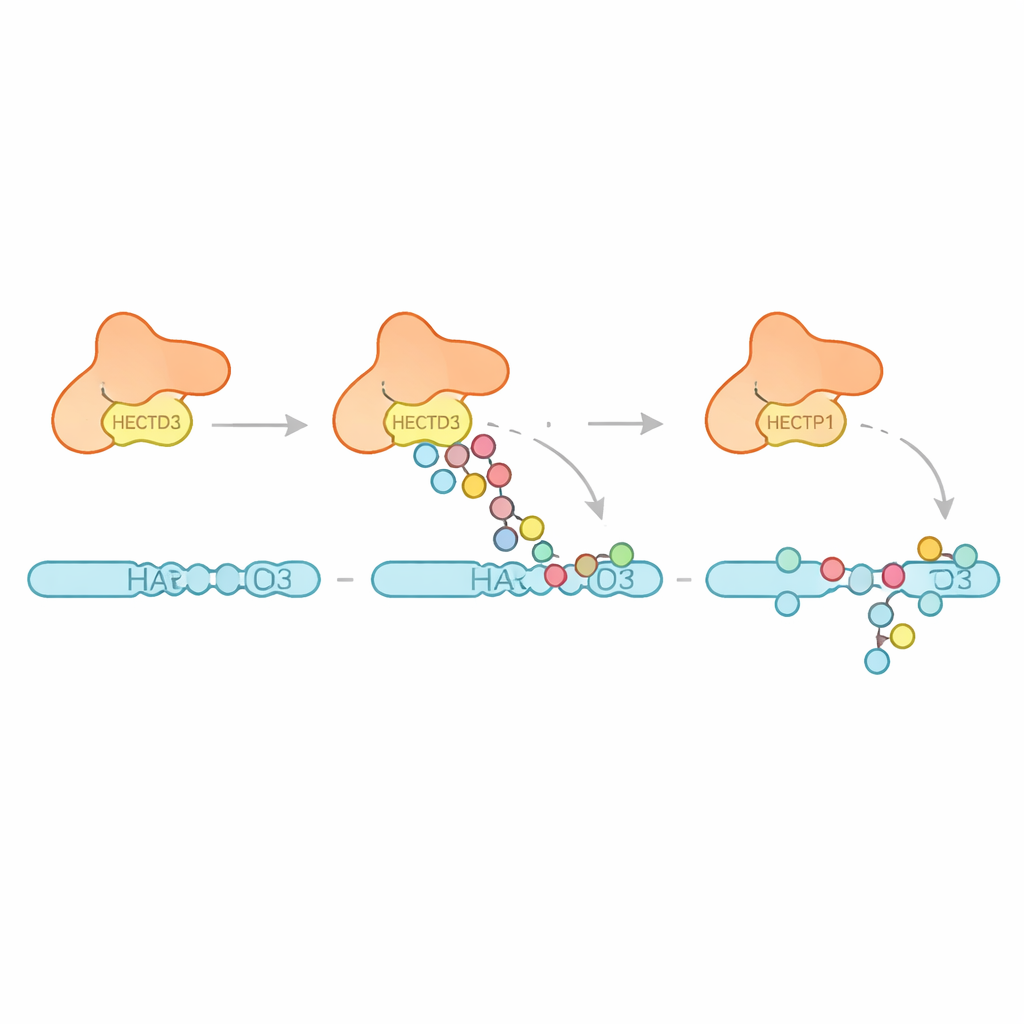
Waarom dit belangrijk is voor ziekte en behandeling
Gezamenlijk schetsen deze bevindingen HECTD3 als een voortdurend actief maar structureel verfijnd labelapparaat dat vooral het aanzetten van ubiquitinemarkeringen verzorgt en vertrouwt op een flexibele, unieke N-terminale regio om specifieke partners zoals PARP1 te herkennen. Omdat HECTD3-activiteit verhoogd is in meerdere vormen van kanker en bepaalt hoe DNA-reparatie-eiwitten worden behandeld, opent begrip van zijn structuur en mechanisme de deur naar het ontwerpen van moleculen die zijn dockingsoppervlakken of katalytisch centrum verstoren. Dergelijke gerichte interventies zouden in principe kunnen verschuiven hoe cellen beslissen over het lot van cruciale eiwitten bij kanker, infectie en ontstekingsziekten.
Bronvermelding: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
Trefwoorden: ubiquitine-ligase, HECTD3, eiwitlabeling, PARP1, kankerbiologie