Clear Sky Science · es
Estructura y mecanismo de la ligasa HECT HECTD3
Cómo las células etiquetan sus proteínas para actuar
En el interior de cada célula, un pequeño sistema de señalización decide qué proteínas se reparan, reciclan o reconvierten para nuevas funciones. Este estudio se centra en una de las enzimas que dirige ese sistema, una proteína llamada HECTD3. HECTD3 se ha relacionado con el cáncer, la inflamación y la infección viral, pero su funcionamiento a nivel atómico seguía siendo poco claro. Al combinar potentes técnicas de imagen y herramientas bioquímicas, los autores revelan cómo está construido HECTD3, cómo elige a sus socios moleculares y cómo etiqueta otras proteínas con pequeñas marcas que pueden cambiar su destino.
Una máquina celular de etiquetado con muchos papeles
Con frecuencia, las células modifican sus proteínas con una pequeña molécula llamada ubiquitina, que puede actuar como una etiqueta de color en un almacén de clasificación. Cadenas de estas etiquetas, dispuestas de distintas maneras, envían mensajes diferentes: algunas señalan una proteína para destrucción, otras modulan su actividad o su localización. Las enzimas llamadas ligasas E3 son responsables de elegir qué proteínas se etiquetan y cómo. HECTD3 pertenece a una rama de ligasas E3 que forman un enlace químico temporal con la ubiquitina antes de transferirla al objetivo. Está inusualmente activa en varios cánceres y se ha vinculado a procesos como la muerte celular programada, la señalización inmune y la replicación viral, sin embargo su estructura y su lógica de funcionamiento eran en gran medida desconocidas.
Una enzima constantemente activa con una forma única
Los investigadores preguntaron primero si HECTD3 se comporta como un interruptor que puede activarse o desactivarse. Muchas ligasas relacionadas se controlan plegándose en formas que se bloquean a sí mismas o emparejándose en ensamblajes mayores. Mediante ensayos bioquímicos y una técnica que mide el tamaño de las proteínas en solución, el equipo encontró que HECTD3 suele existir como copia única y no parece inhibirse a sí mismo mediante auto‑bloqueo ni por agregación estable. Tanto su sección catalítica central como la proteína completa son activas, con una clara preferencia por trabajar con una familia de enzimas auxiliares que entregan ubiquitina. Esto significa que HECTD3 está esencialmente “listo para actuar” y que probablemente se regula en la célula por factores distintos al auto‑bloqueo simple.
Revelando una nueva arquitectura proteica
Para entender cómo está formado HECTD3, los autores utilizaron crioelectrónica (cryo‑EM) para capturar imágenes de moléculas individuales congeladas en una capa fina de hielo. Determinaron estructuras de la proteína sola y en un estado donde una molécula de ubiquitina está firmemente unida a su sitio activo. Estas instantáneas muestran que HECTD3 es compacto en lugar de en forma de anillo, con una clásica región catalítica de dos lóbulos en un extremo y una previamente misteriosa región N‑terminal en el otro. La mitad N‑terminal resulta formar dos plegamientos totalmente nuevos, que los autores denominan D3NA y D3NB, dispuestos como una plataforma helicoidal que sustenta un módulo DOC de unión al sustrato. Cuando la ubiquitina está cargada, los lóbulos catalíticos adoptan una disposición particular en forma de L, y residuos ácidos específicos cerca del sitio activo ayudan a preparar las cadenas laterales de las proteínas entrantes para aceptar la etiqueta. El trabajo muestra que, aunque HECTD3 sigue las reglas generales de su familia enzimática, utiliza una combinación distinta de elementos estructurales para hacerlo.
Cómo HECTD3 se etiqueta a sí mismo y a sus dianas
A continuación, el equipo examinó qué tipos de patrones de ubiquitina crea HECTD3. En lugar de construir largas cadenas de un tipo específico, la enzima principalmente adjunta múltiples unidades de ubiquitina individuales y cadenas cortas, con evidencia de algunas cadenas que favorecen un enlace conocido por promover la degradación proteica. Esto sugiere que HECTD3 es mejor iniciando eventos de etiquetado que extendiéndolos en señales largas. Los autores se centraron entonces en una proteína diana propuesta llamada PARP1, un factor de reparación del ADN ya conocido por influir en las respuestas a terapias contra el cáncer. En reacciones de tubo de ensayo, HECTD3 modificó eficientemente PARP1, decorando varios sitios de lisina en su mitad de unión al ADN con etiquetas que incluyen cadenas asociadas a la eliminación de proteínas. Mediante entrecruzamiento químico y espectrometría de masas, mapearon los puntos de contacto entre HECTD3 y PARP1, confirmando que tanto el módulo DOC como la región catalítica ayudan a posicionar el sustrato. Mutar dos aminoácidos expuestos en la superficie del DOC redujo drásticamente el etiquetado de PARP1 sin dañar la química central, lo que los señala como anclajes clave para el reconocimiento del sustrato.
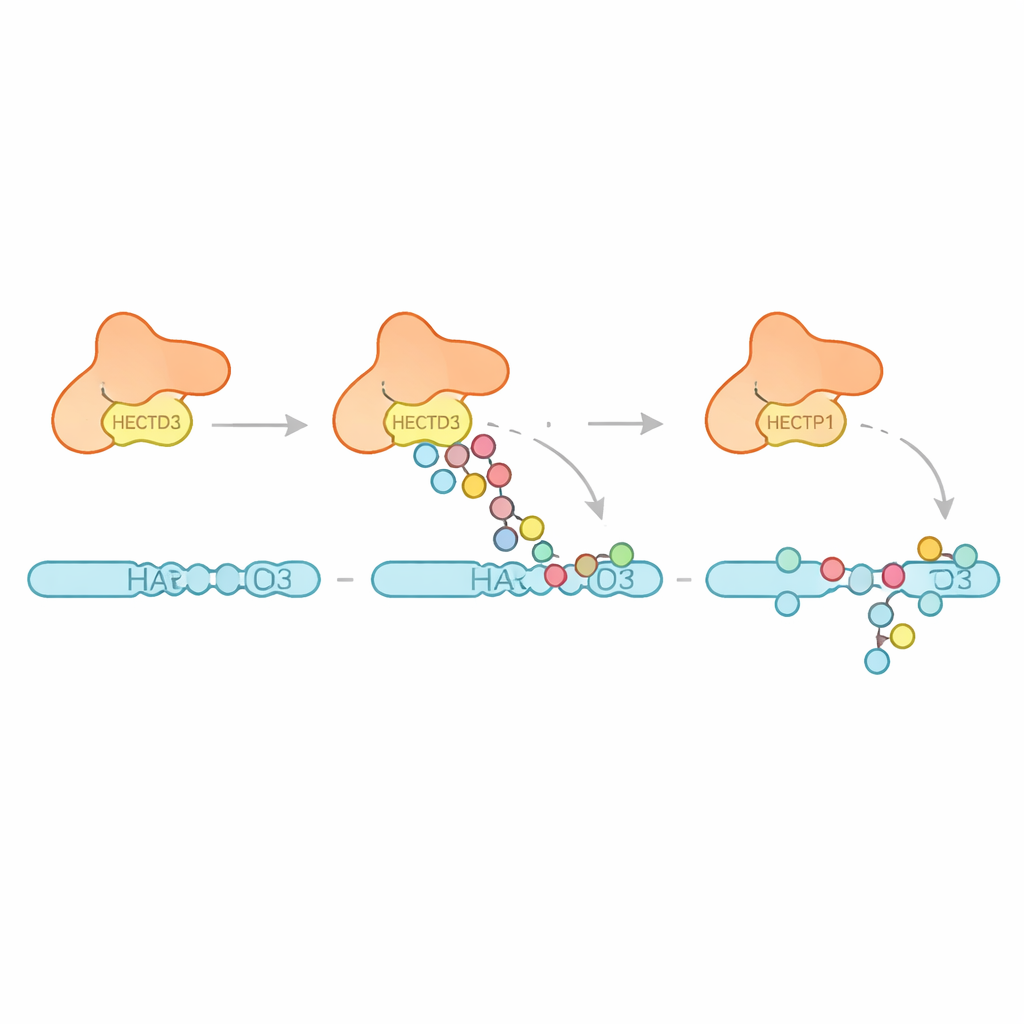
Por qué importa esto para la enfermedad y el tratamiento
En conjunto, estos hallazgos describen a HECTD3 como una máquina de etiquetado constantemente activa pero estructuralmente sofisticada que principalmente inicia marcas de ubiquitina y depende de una región N‑terminal flexible y única para reconocer socios específicos como PARP1. Dado que la actividad de HECTD3 está elevada en varios cánceres y modula cómo se manejan las proteínas de reparación del ADN, comprender su estructura y mecanismo abre la puerta al diseño de moléculas que interfieran con sus superficies de acoplamiento o con su centro catalítico. Tales intervenciones dirigidas podrían, en principio, alterar cómo las células deciden el destino de proteínas críticas en el cáncer, la infección y la enfermedad inflamatoria.
Cita: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
Palabras clave: ligasa de ubiquitina, HECTD3, marcado de proteínas, PARP1, biología del cáncer