Clear Sky Science · sv
Struktur och mekananism hos HECT‑ligasen HECTD3
Hur celler märker sina proteiner för åtgärd
Inuti varje cell finns ett litet signalsystem som avgör vilka proteiner som repareras, återvinns eller byggs om för nya uppgifter. Denna studie fokuserar på ett av enzymerna som driver systemet, ett protein kallat HECTD3. HECTD3 har kopplats till cancer, inflammation och virusinfektioner, men hur det fungerar på atomnivå har varit oklart. Genom att kombinera kraftfulla avbildnings‑ och biokemiska metoder visar författarna hur HECTD3 är uppbyggt, hur det väljer sina molekylära partners och hur det förser andra proteiner med små märken som kan ändra deras öde.
En cellulär märkningsmaskin med många roller
Celler modifierar ofta sina proteiner med en liten molekyl kallad ubiquitin, som kan fungera som en färgad tagg i ett sorteringslager. Strängar av dessa taggar, arrangerade på olika sätt, ger olika budskap: vissa markerar ett protein för nedbrytning, andra fintunerar dess aktivitet eller plats. Enzymer kallade E3‑ligaser ansvarar för att välja vilka proteiner som märks och hur. HECTD3 tillhör en gren av E3‑ligaser som är kända för att bilda en tillfällig kemisk bindning med ubiquitin innan taggen överförs till ett mål. Det är ovanligt aktivt i flera cancerformer och har kopplats till processer som programmerad celldöd, immunsignalering och virusreplikation, men dess struktur och arbetslogik var till stor del okänd.
En ständigt aktiv enzym med unik form
Forskarna frågade först om HECTD3 beter sig som en strömbrytare som kan slås på eller av. Många närbesläktade ligaser håller sig i schack genom att vika sig i själv‑blockerande former eller genom att para ihop sig till större komplex. Med biokemiska tester och en teknik som mäter proteiners storlek i lösning fann teamet att HECTD3 till största delen förekommer som en ensam kopia och inte tycks stänga av sig själv via själv‑inhibering eller stabil klustring. Både dess katalytiska kärna och det fullängdsproteinet är aktiva, med en tydlig preferens för att samarbeta med en familj av hjälparenzymer som överför ubiquitin. Det innebär att HECTD3 i praktiken är ”redo att gå” och sannolikt regleras i cellen av andra faktorer än enkel själv‑blockering.
Avslöjar en ny proteinarkitektur
För att förstå hur HECTD3 är uppbyggt använde författarna kryoelektronmikroskopi för att fånga bilder av enskilda molekyler frusna i tunn is. De bestämde strukturer av proteinet ensam och i ett tillstånd där en ubiquitinmolekyl är fast bunden till dess aktiva yta. Dessa ögonblicksbilder visar att HECTD3 är kompakt snarare än ringformat, med en klassisk två‑lobad katalytisk region i ena änden och en tidigare mystisk N-terminal region i den andra. Den N‑terminala halvan visar sig bilda två helt nya foldar, som författarna namnger D3NA och D3NB, ordnade som en spiralplattform som stöder en substratbindande DOC‑modul. När ubiquitin är på plats antar de katalytiska lobarna en särskild L‑formad konfiguration, och specifika sura rester nära den aktiva ytan hjälper till att förbereda inkommande sidokedjor på proteiner att ta emot taggen. Arbetet visar att även om HECTD3 följer de allmänna reglerna för sin enzymfamilj använder det en distinkt kombination av strukturella element för att göra det.
Hur HECTD3 märker sig själv och sina mål
Nästa undersökte teamet vilka typer av ubiquitinmönster HECTD3 skapar. Istället för att bygga långa kedjor av en specifik typ fäster enzymet framför allt flera enstaka ubiquitinenheter och korta kedjor, med tecken på vissa kedjor som gynnar en koppling som är känd för att främja proteinnedbrytning. Detta tyder på att HECTD3 är bättre på att starta märkningshändelser än att förlänga dem till långa signaler. Författarna riktade sig sedan mot ett föreslaget målprotein kallat PARP1, en DNA‑reparationsfaktor som redan är känd för att påverka svar på cancerbehandling. I provrörsreaktioner modifierade HECTD3 effektivt PARP1 och dekorerade flera lysinplatser i dess DNA‑bindande halva med taggar som inkluderar kedjor associerade med proteinnedbrytning. Genom att använda kemisk korslänkning och masspektrometri kartlade de kontaktpunkter mellan HECTD3 och PARP1, vilket bekräftade att både DOC‑modulen och den katalytiska regionen hjälper till att positionera substratet. Mutation av två exponerade aminosyror på DOC‑ytan minskade kraftigt PARP1‑märkningsgraden utan att skada kärnkemin, vilket pekar ut dem som viktiga ankare för substratigenkänning.
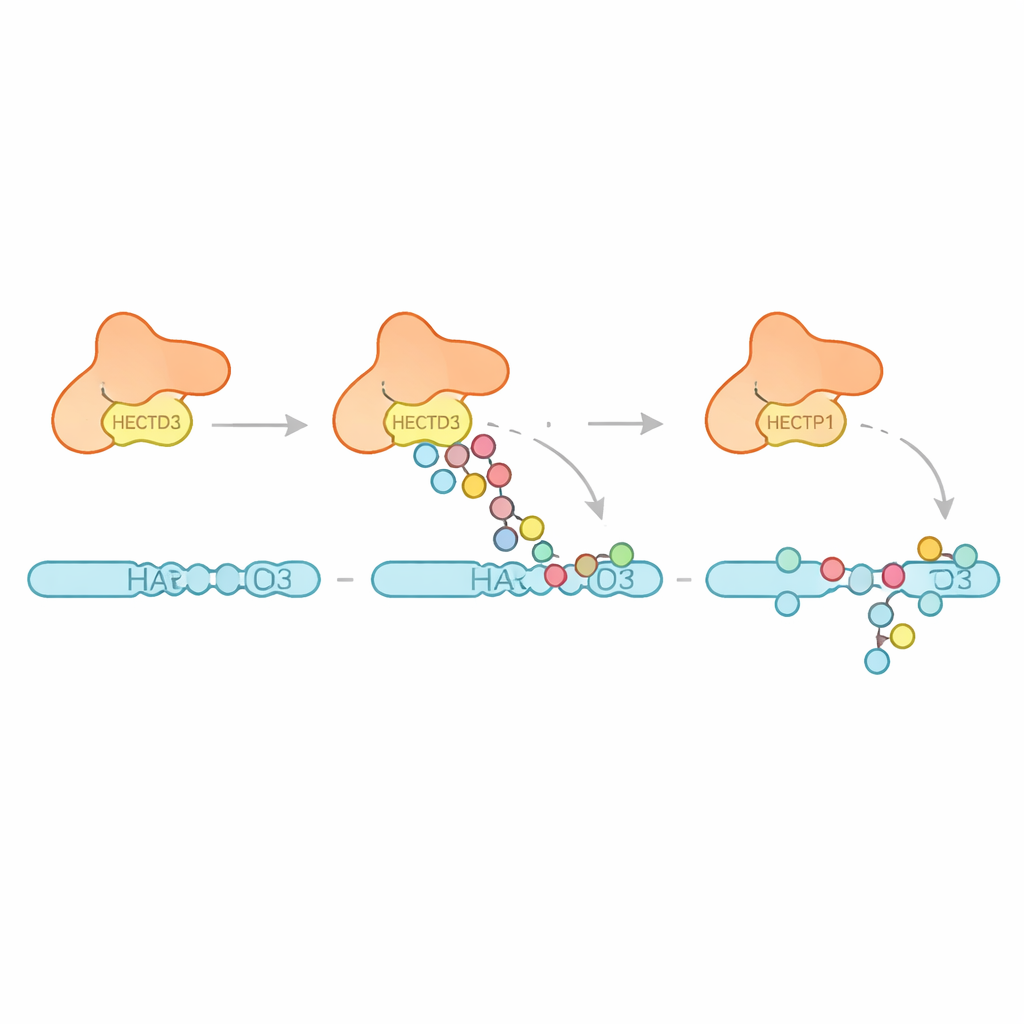
Varför detta spelar roll för sjukdom och behandling
Tillsammans målar dessa fynd upp HECTD3 som en ständigt aktiv men strukturellt sofistikerad märkningsmaskin som främst initierar ubiquitinmarkeringar och förlitar sig på en flexibel, unik N‑terminal region för att känna igen specifika partners som PARP1. Eftersom HECTD3‑aktivitet är förhöjd i flera cancerformer och påverkar hur DNA‑reparationsproteiner hanteras öppnar förståelsen av dess struktur och mekanism möjligheter att designa molekyler som stör dess dockningsytor eller katalytiska centrum. Sådana riktade ingrepp skulle i princip kunna förändra hur celler avgör ödet för kritiska proteiner vid cancer, infektion och inflammatorisk sjukdom.
Citering: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
Nyckelord: ubiquitinligas, HECTD3, proteinetikettering, PARP1, cancerbiologi