Clear Sky Science · ja
HECTリガーゼHECTD3の構造と機構
細胞がタンパク質にタグを付ける仕組み
すべての細胞内には、どのタンパク質を修復し、再利用し、あるいは新たな役割に切り替えるかを決める小さなシグナル系が存在します。本研究はこのシステムを動かす酵素の一つであるHECTD3というタンパク質に焦点を当てます。HECTD3はがん、炎症、ウイルス感染と関連づけられてきましたが、その原子レベルでの働きは不明でした。著者らは高性能なイメージングと生化学的手法を組み合わせ、HECTD3の構造、どの分子を選ぶか、そして他のタンパク質に運命を変える小さなタグをどのように付けるかを明らかにしました。
多様な役割を持つ細胞のタグ付け装置
細胞はしばしばユビキチンという小さな分子でタンパク質を修飾します。これは倉庫の色分けタグのように振る舞い得ます。異なる配列で並んだユビキチン鎖は異なるメッセージを伝え、あるものはタンパク質を分解へ導き、また別のものは活性や局在を調節します。E3リガーゼと呼ばれる酵素群が、どのタンパク質をどのようにタグ付けするかを選びます。HECTD3は、ユビキチンと一時的な化学結合を作ってから標的に渡すことで知られるE3リガーゼの系統に属します。HECTD3は複数のがんで異常に活性化しており、プログラム細胞死、免疫シグナル伝達、ウイルス複製などと結び付けられてきましたが、その構造と動作原理はほとんど明らかになっていませんでした。
常に作動する酵素、独特の形状
研究者らはまず、HECTD3がオン・オフを切り替えるスイッチのように振る舞うかを調べました。多くの関連リガーゼは自己抑制のために折り畳まれた自己遮断構造を取ったり、より大きな集合体を形成したりします。生化学的検査と溶液中でタンパク質のサイズを測る手法により、HECTD3は主に単量体として存在し、自己抑制や安定したクラスター化で自らをシャットダウンしているようには見えないことが示されました。触媒コア部位と全長タンパク質の両方に活性があり、ユビキチンを渡す補助酵素ファミリーの一つを明確に好むことも分かりました。これはHECTD3が本質的に「常に準備ができている」状態にあり、細胞内では単純な自己遮断以外の因子によって制御されている可能性を示唆します。
新たなタンパク質アーキテクチャの解明
HECTD3の構造を理解するために、著者らはクライオ電子顕微鏡を用いて薄い氷に凍結した単分子の像を取得しました。タンパク質単体の構造と、ユビキチン分子が活性部位にしっかり結合した状態の構造を決定しました。これらのスナップショットは、HECTD3がリング状ではなくコンパクトであり、片端に古典的な二葉構造の触媒領域、反対側にこれまで謎だったN末端領域を持つことを示しています。N末端半分は実は二つのまったく新しいフォールドを形成しており、著者らはそれらをD3NAとD3NBと命名し、基質結合DOCモジュールを支えるヘリカルなプラットフォームとして配列していることが分かりました。ユビキチンがロードされると触媒葉は特定のL字型配列を取り、活性部位近傍の特定の酸性残基が入ってくる基質側鎖をタグ受容に備えるのを助けます。本研究はHECTD3が酵素ファミリーの一般的ルールに従いながらも、独自の構造要素の組み合わせを用いて機能していることを示しています。
HECTD3が自身と標的をどのようにタグ付けするか
次にチームはHECTD3がどのようなユビキチンパターンを作るかを調べました。特定の型の長い鎖を伸ばすのではなく、酵素は主に複数の単一ユビキチンの付着と短鎖の形成を行い、タンパク質分解を促すことが知られている結合様式を好む鎖の存在も示されました。これはHECTD3がタグ付けの開始には長けているが、それを長いシグナルへと伸ばすのは得意でないことを示唆します。著者らは次にPARP1という提案された標的タンパク質に注目しました。PARP1はDNA修復因子で、がん治療への応答にも影響することが知られています。試験管内反応でHECTD3はPARP1を効率的に修飾し、DNA結合領域のいくつかのリジン残基にタンパク質除去と関連する鎖を含むタグを付けました。化学的クロスリンクと質量分析を用いてHECTD3とPARP1の接触点をマッピングしたところ、DOCモジュールと触媒領域の両方が基質の位置決めに寄与していることが確認されました。DOC表面の露出した二つのアミノ酸を変異させると、コアの化学反応を損なうことなくPARP1のタグ付けが著しく低下し、これらが基質認識の重要なアンカーであることが示されました。
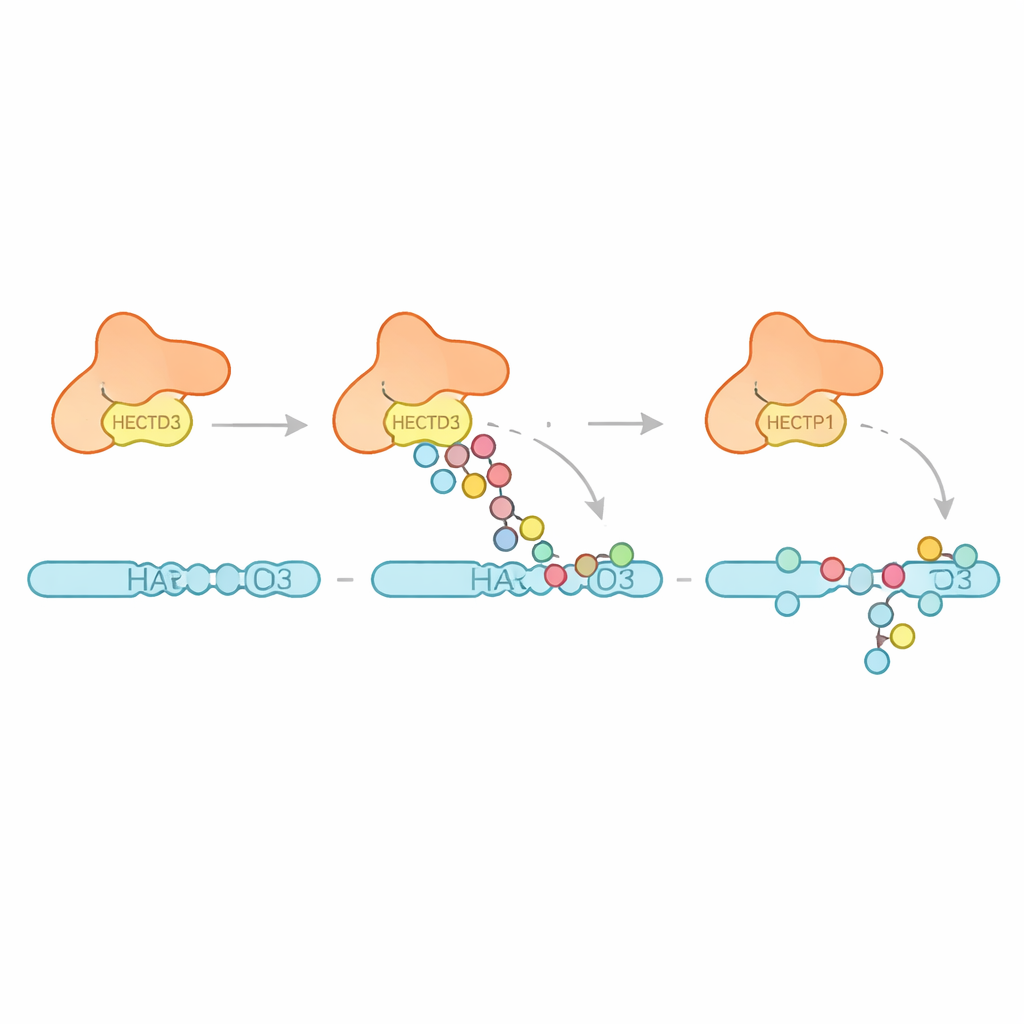
疾患と治療への意義
これらの結果は、HECTD3が常に活性だが構造的に洗練されたタグ付け装置であり、主にユビキチンマークの開始を担い、柔軟で独特なN末端領域を用いてPARP1のような特定のパートナーを認識することを描き出します。HECTD3の活性は複数のがんで高まっており、DNA修復タンパク質の取り扱いに影響を与えるため、その構造と機構を理解することは、ドッキング面や触媒中心を妨げる分子の設計につながります。そのような標的介入は、理論的にはがん、感染症、炎症性疾患において重要タンパク質の運命決定を変える可能性があります。
引用: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
キーワード: ユビキチンリガーゼ, HECTD3, タンパク質タグ付け, PARP1, がん生物学