Clear Sky Science · ar
البنية والآلية لإنزيم الليغاز HECT من نوع HECTD3
كيف تصنف الخلايا بروتيناتها للعمل
داخل كل خلية، نظام إشارات دقيق يقرّر أي البروتينات تُصلح أو تُعاد تدويرها أو تُعاد برمجتها لمهام جديدة. تركز هذه الدراسة على أحد الإنزيمات التي تُشغّل هذا النظام، وهو بروتين يسمى HECTD3. ارتبط HECTD3 بالسرطان والالتهاب والعدوى الفيروسية، لكن آلية عمله على المستوى الذري بقيت غير واضحة. من خلال الجمع بين تقنيات تصوير قوية وأدوات كيميائية حيوية، يكشف المؤلفون كيف يُبنى HECTD3، وكيف يختار شركاءه الجزيئيين، وكيف يزيّن بروتينات أخرى بعلامات صغيرة يمكن أن تغيّر مصيرها.
آلة وسم خلوية ذات أدوار متعددة
غالباً ما تعدّل الخلايا بروتيناتها بجزيء صغير يُسمى اليوبيكويتين، الذي يمكن أن يعمل كوسم ملون في مستودع فرز. سلاسل هذه الوسوم، المصطفة بطرق مختلفة، تنقل رسائل مختلفة: بعضها يشير إلى تدمير البروتين، وأخرى تضبط نشاطه أو مكانه. إنزيمات تُسمى ليغازات E3 مسؤولة عن اختيار أي البروتينات تُوسم وبأي شكل. ينتمي HECTD3 إلى فرع من ليغازات E3 المعروفة بتشكيل رابطة كيميائية مؤقتة مع اليوبيكويتين قبل أن تنقله إلى الهدف. يكون نشاطه مرتفعاً بشكل غير عادي في عدة سرطانات وارتبط بعمليات مثل الموت المبرمج للخلايا، وإشارات المناعة، وتكاثر الفيروسات، ومع ذلك كانت بنيته ومنطق عمله إلى حد كبير غير معروفة.
إنزيم جاهز دائماً وشكل فريد
سأل الباحثون أولاً ما إذا كان HECTD3 يتصرف كمفتاح قابل للتشغيل والإيقاف. العديد من الليغازات المماثلة تضبط نفسها من خلال الطي إلى أشكال تُعيقها ذاتياً أو من خلال التجمع في تراكيب أكبر. باستخدام اختبارات كيميائية حيوية وتقنية تقيس حجم البروتينات في المحلول، وجد الفريق أن HECTD3 يوجد في الغالب كنسخة مفردة ولا يبدو أنه يغلق نفسه عبر تثبيط ذاتي أو تجمعات مستقرة. كل من القسم التحفيزي الأساسي والبروتين بكامله نشطان، مع تفضيل واضح للعمل مع عائلة واحدة من الإنزيمات المساعدة التي تُسلّم اليوبيكويتين. هذا يعني أن HECTD3 «جاهز للاستخدام» على نحو أساسي ومن المرجح أن تُتحكم فيه في الخلايا عوامل أخرى غير التثبيط الذاتي البسيط.
كشف بنية بروتينية جديدة
لفهم كيف يُبنى HECTD3، استخدم المؤلفون الميكروسكوب الإلكتروني بالتبريد لالتقاط صور لجزيئات مفردة مجمدة في طبقة رقيقة من الجليد. حددوا هياكل للبروتين بمفرده وفي حالة مرتبط فيها جزيء يوبيكويتين بثبات بموقعه النشط. تُظهر هذه اللقطات أن HECTD3 مدمج بدلاً من أن يكون على شكل حلقي، مع منطقة تحفيزية تقليدية ذات فصين عند أحد الطرفين ومنطقة غامضة سابقة عند الطرف الآخر. يتضح أن النصف الأمامي من الطرف N يشكل طياتين جديدتين تماماً، أطلق المؤلفون عليهما اسم D3NA وD3NB، مرتبتين كمنصة لولبية تدعم وحدة DOC المرتبطة بالركائز. عند تحميل اليوبيكويتين، تتخذ الفصوص التحفيزية ترتيباً معيناً على شكل حرف L، وتساعد بقايا حمضية محددة قريبة من الموقع النشط في تحضير سلاسل جانبية من البروتينات الواردة لقبول الوسم. يُظهر العمل أنه بالرغم من أن HECTD3 يتبع القواعد العامة لعائلته الإنزيمية، فإنه يستخدم مجموعة مميزة من العناصر البنائية للقيام بذلك.
كيف يوسم HECTD3 نفسه وهدافه
بعد ذلك فحص الفريق أنواع أنماط اليوبيكويتين التي ينتجها HECTD3. بدلاً من بناء سلاسل طويلة من نوع واحد محدد، يرفق الإنزيم في المقام الأول وحدات يوبيكويتين مفردة متعددة وسلاسل قصيرة، مع دلائل على بعض السلاسل التي تفضل وصلات معروفة بتعزيز تحلل البروتين. هذا يشير إلى أن HECTD3 أفضل في بدء أحداث الوسم منه في تمديدها إلى إشارات طويلة. ثم تطرق المؤلفون إلى بروتين مستهدف مقترح يُدعى PARP1، وهو عامل إصلاح DNA معروف بتأثيره على استجابة العلاجات ضد السرطان. في تفاعلات أنبوبية، عدّل HECTD3 PARP1 بكفاءة، مزيّناً مواقع عدة من الليسين في نصفه المربوط بالحمض النووي بوسوم تتضمن سلاسل مرتبطة بإزالة البروتين. باستخدام الربط الكيميائي والتحليل الطيفي الكتلي، رصدوا نقاط تماس بين HECTD3 وPARP1، مؤكّدين أن وحدة DOC والمنطقة التحفيزية تساعدان معا في موضع الركيزة. أدت طفرات في حمضين أمينيين مكشوفين على سطح DOC إلى تقليل شديد في وسم PARP1 دون إلحاق ضرر بالكيمياء الأساسية، مما يبرزها كمراسي رئيسية للتعرف على الركائز.
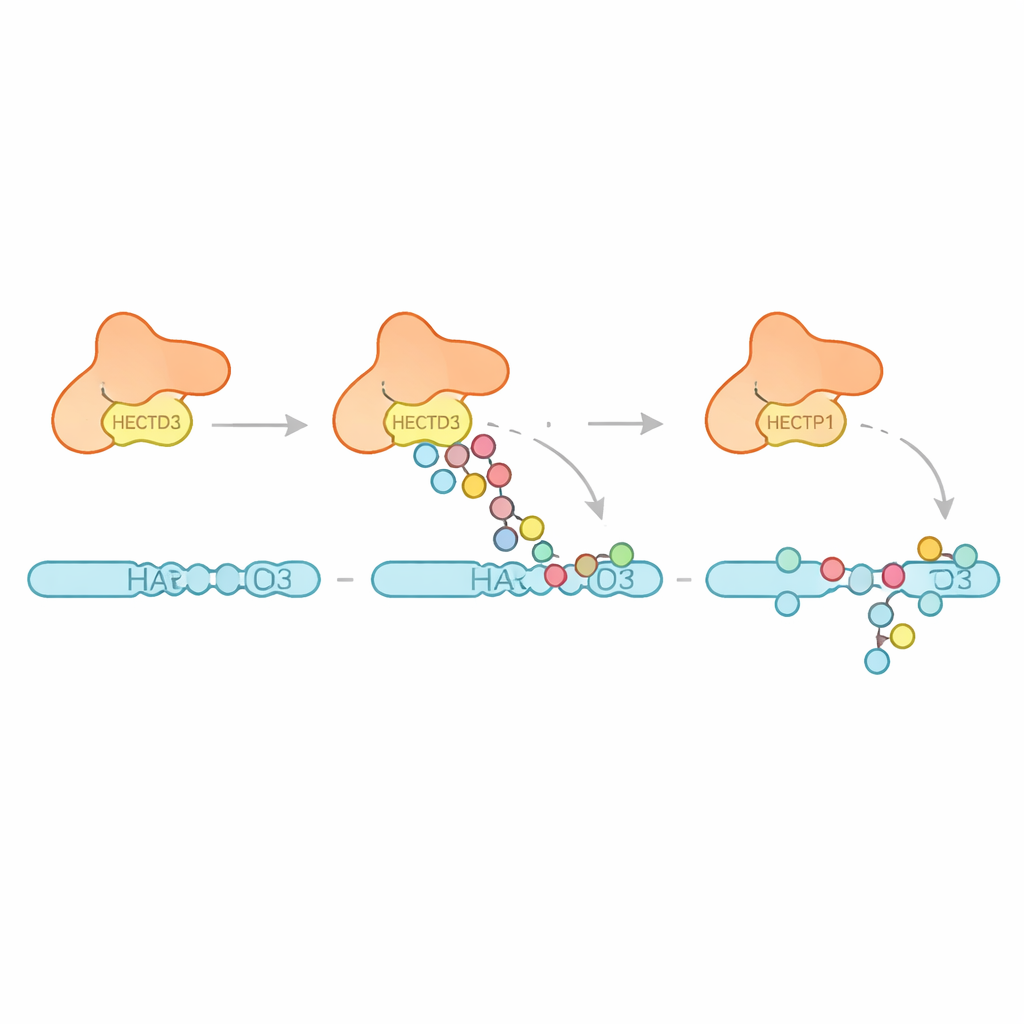
لماذا يهم هذا للمرض والعلاج
مجتمعة، ترسم هذه النتائج صورة HECTD3 كآلة وسم نشطة دائماً لكنها متقنة البنية، تطلق بشكل أساسي بداية علامات اليوبيكويتين وتعتمد على منطقة N الطرفية الفريدة والمرنة للتعرف على شركاء محددين مثل PARP1. بما أن نشاط HECTD3 مرتفع في عدة سرطانات ويؤثر على كيفية تعامل الخلايا مع بروتينات إصلاح الحمض النووي، فإن فهم بنيته وآليته يفتح أبواباً لتصميم جزيئات تعيق أسطح اقترانه أو مركزه التحفيزي. مثل هذه التدخلات المستهدفة قد تغيّر، من حيث المبدأ، طريقة قرار الخلايا بشأن مصير بروتينات حاسمة في السرطان والعدوى والأمراض الالتهابية.
الاستشهاد: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
الكلمات المفتاحية: ليغاز يوبكويتين, HECTD3, وسم البروتين, PARP1, بيولوجيا السرطان