Clear Sky Science · tr
HECT ligaz HECTD3’ün Yapısı ve Mekanizması
Hücreler Proteinlerini Nasıl Etiketler?
Her hücrenin içinde hangi proteinlerin onarılacağı, geri dönüştürüleceği veya yeni görevler için yeniden yönlendirileceğine karar veren küçük bir sinyal sistemi vardır. Bu çalışma, bu sistemi yöneten enzimlerden biri olan HECTD3 adlı proteine odaklanıyor. HECTD3 kanser, iltihaplanma ve viral enfeksiyonlarla ilişkilendirilmiş, ancak atomik düzeyde nasıl çalıştığı belirsiz kalmıştı. Araştırmacılar güçlü görüntüleme ve biyokimyasal araçları birleştirerek HECTD3’ün nasıl yapılandığını, moleküler partnerlerini nasıl seçtiğini ve diğer proteinleri kaderlerini değiştirebilecek küçük etiketlerle nasıl süslediğini ortaya koyuyorlar.
Çok Yönlü Bir Hücresel Etiketleme Makinesi
Hücreler sıkça proteinlerini ubiquitin adı verilen küçük bir molekülle değiştirir; bu, bir ayırma deposundaki renkli bir etikete benzer. Bu etiketlerin farklı düzenlerde dizilmesi farklı mesajlar gönderir: bazıları proteini yok edilmek üzere işaretler, diğerleri ise aktivitesini veya konumunu ayarlar. Hangi proteinlerin nasıl etiketleneceğine E3 ligazlar karar verir. HECTD3, ubiquitin ile hedefine geçmeden önce geçici bir kimyasal bağ kurmasıyla bilinen E3 ligaz grubuna aittir. Birçok kanserde alışılmadık biçimde aktif olduğu ve programlı hücre ölümü, bağışıklık sinyali ve viral çoğalma gibi süreçlerle ilişkilendirildiği halde, yapısı ve çalışma mantığı büyük ölçüde bilinmiyordu.
Sürekli Aktif Olan ve Benzersiz Şekilli Bir Enzim
Araştırmacılar önce HECTD3’ün açılıp kapanabilen bir anahtar gibi davranıp davranmadığını sordular. İlişkili birçok ligaz, kendini engelleyen katlanmalar veya daha büyük kümelenmeler oluşturarak aktifliğini sınırlar. Biyokimyasal testler ve çözeltide proteinlerin boyutunu ölçen bir teknik kullanılarak, ekip HECTD3’ün çoğunlukla tek kopya halinde bulunduğunu ve kendini engelleme ya da stabil kümeleşme yoluyla kapanmadığını belirledi. Hem katalitik çekirdek bölgesi hem de tam uzunluklu protein aktiftir ve ubiquitin’i devralan yardımcı enzimlerin bir ailesiyle çalışma konusunda belirgin bir tercih gösterir. Bu, HECTD3’ün temelde “harekete hazır” olduğunu ve hücrelerde basit kendi kendini engelleme yerine başka faktörlerle kontrol edildiğini gösterir.
Yeni Bir Protein Mimarisi Ortaya Çıkıyor
HECTD3’ün nasıl yapılandığını anlamak için yazarlar kriyo-elektron mikroskopisi kullanarak ince buzda donmuş tek moleküllerin görüntülerini yakaladılar. Proteinin yalnız hali ve aktif bölgesine sıkıca bağlı bir ubiquitin molekülünün bulunduğu durumun yapısını belirlediler. Bu anlık görüntüler HECTD3’ün halka şeklinde değil, kompakt olduğunu; bir uçta klasik iki loplu katalitik bölge ve diğer uçta daha önce gizemli kalan N-terminus bölümü bulunduğunu gösteriyor. N-terminusun yarısı, yazarların D3NA ve D3NB adını verdiği tamamen yeni iki katlanış oluşturur; bunlar helikal bir platform olarak düzenlenmiş ve bir substrat-bağlama DOC modülünü destekler. Ubiquitin yüklendiğinde, katalitik loplar belirli bir L şeklini alır ve aktif bölgeye yakın özgül asidik kalıntılar gelen protein yan zincirlerini etiketi kabul etmeye hazırlamaya yardımcı olur. Çalışma, HECTD3’ün enzim ailesinin genel kurallarına uyduğunu, ancak bunu yapmak için farklı bir yapısal eleman kombinasyonu kullandığını gösteriyor.
HECTD3 Kendi Kendini ve Hedeflerini Nasıl Etiketler?
Sonraki adımda ekip HECTD3’ün hangi tür ubiquitin desenlerini oluşturduğunu inceledi. Tek tip uzun zincirler oluşturmak yerine, enzim çoğunlukla çoklu tek ubiquitin birimleri ve kısa zincirler takar; bazı zincirlerin protein yıkımını teşvik eden bir bağlantı türünü tercih ettiğine dair kanıtlar vardır. Bu, HECTD3’ün uzun sinyaller halinde uzatmaktan çok etiketleme olaylarını başlatmada daha yetkin olduğunu düşündürür. Yazarlar daha sonra PARP1 adı verilen ve kanser tedavisi yanıtlarını etkileyebilen bir DNA onarım faktörü olduğu bilinen önerilen bir hedef proteine yöneldi. Deney tüpü reaksiyonlarında HECTD3, PARP1’i verimli biçimde modifiye ederek DNA-bağlayan yarısındaki birkaç lizin bölgesini protein uzaklaştırma ile ilişkilendirilen zincirleri de içerecek şekilde etiketledi. Kimyasal çapraz bağlama ve kütle spektrometrisi kullanarak HECTD3 ile PARP1 arasındaki temas noktalarını haritaladılar ve DOC modülü ile katalitik bölgenin substratı konumlandırmada her ikisinin de rol oynadığını doğruladılar. DOC yüzeyinde yer alan iki açıkta kalan aminoasidin mutasyonu, temel kimyayı etkilemeden PARP1 etiketlemesini belirgin şekilde azalttı; bu da onları substrat tanıma için kilit çapa noktaları olarak öne çıkarıyor.
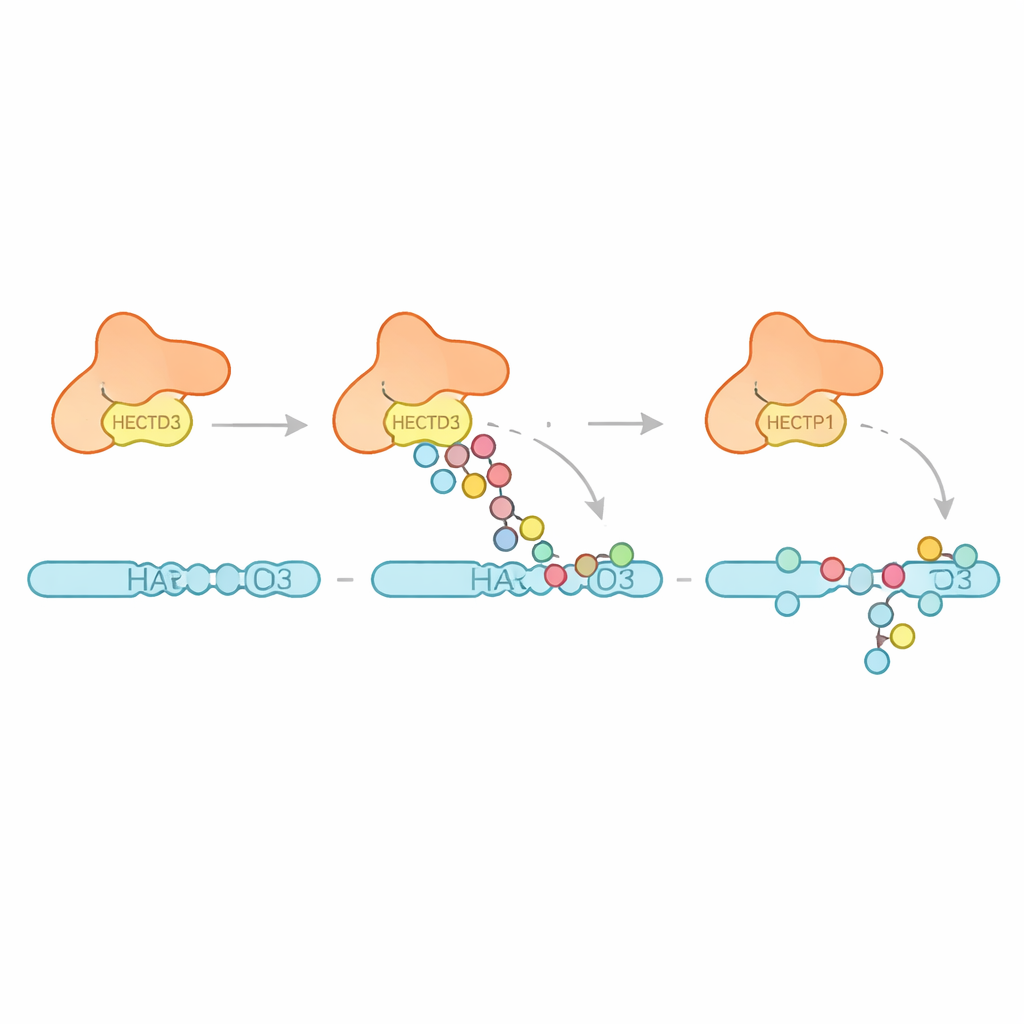
Hastalık ve Tedavi Açısından Neden Önemli?
Bu bulgular HECTD3’ü sürekli aktif fakat yapısal olarak sofistike bir etiketleme makinesi olarak resmediyor: esasen ubiquitin işaretlerini başlatıyor ve PARP1 gibi belirli partnerleri tanımak için esnek, benzersiz bir N-terminus bölgesine dayanıyor. HECTD3 aktivitesi birkaç kanserde artmış olduğundan ve DNA onarım proteinlerinin nasıl ele alındığını şekillendirdiğinden, yapısını ve mekanizmasını anlamak; onun kenetlenme yüzeylerine veya katalitik merkezine müdahale eden moleküllerin tasarlanmasına kapı açıyor. Teorik olarak böyle hedefe yönelik müdahaleler, hücrelerin kritik proteinlerin kaderine ilişkin kararlarını kanser, enfeksiyon ve inflamatuar hastalıklarda değiştirebilir.
Atıf: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
Anahtar kelimeler: ubiquitin ligaz, HECTD3, protein etiketleme, PARP1, kanser biyolojisi