Clear Sky Science · fr
Structure et mécanisme de la ligase HECT HECTD3
Comment les cellules étiquettent leurs protéines pour agir
À l’intérieur de chaque cellule, un minuscule système de signalisation décide quelles protéines doivent être réparées, recyclées ou réorientées vers de nouvelles tâches. Cette étude se concentre sur l’un des enzymes qui pilotent ce système, une protéine nommée HECTD3. HECTD3 a été associée au cancer, à l’inflammation et aux infections virales, mais son mode d’action à l’échelle atomique restait obscure. En combinant des méthodes d’imagerie puissantes et des outils biochimiques, les auteurs révèlent comment HECTD3 est construit, comment il choisit ses partenaires moléculaires et comment il décore d’autres protéines avec de petites étiquettes pouvant modifier leur destin.
Une machine cellulaire d’étiquetage aux multiples rôles
Les cellules modifient souvent leurs protéines par une petite molécule appelée ubiquitine, qui peut agir comme une étiquette colorée dans un centre de tri. Des chaînes de ces étiquettes, organisées de façons différentes, envoient des messages distincts : certaines marquent une protéine pour destruction, d’autres ajustent son activité ou sa localisation. Les enzymes appelées ligases E3 sont responsables de choisir quelles protéines sont marquées et comment. HECTD3 appartient à une famille de ligases E3 connues pour former un lien chimique temporaire avec l’ubiquitine avant de la transférer sur une cible. Elle est anormalement active dans plusieurs cancers et liée à des processus tels que la mort cellulaire programmée, la signalisation immune et la réplication virale, mais sa structure et sa logique de fonctionnement restaient pour l’essentiel inconnues.
Une enzyme constamment active avec une forme singulière
Les chercheurs ont d’abord cherché à savoir si HECTD3 se comporte comme un interrupteur qu’on peut activer ou désactiver. De nombreuses ligases apparentées se contrôlent en se repliant dans des conformations auto‑bloquantes ou en s’assemblant en complexes plus larges. Grâce à des essais biochimiques et à une technique mesurant la taille des protéines en solution, l’équipe a constaté que HECTD3 existe majoritairement sous forme monomérique et ne semble pas s’éteindre par auto‑inhibition ni par un regroupement stable. Tant la région catalytique centrale que la protéine en longueur complète sont actives, avec une nette préférence pour une famille d’enzymes auxiliaires qui transfèrent l’ubiquitine. Autrement dit, HECTD3 est essentiellement « prêt à agir » et est probablement régulé dans la cellule par des facteurs autres que l’auto‑blocage simple.
Révélation d’une nouvelle architecture protéique
Pour comprendre la construction de HECTD3, les auteurs ont utilisé la cryo‑microscopie électronique pour capturer des images de molécules individuelles figées dans une mince couche de glace. Ils ont déterminé des structures de la protéine seule et dans un état où une molécule d’ubiquitine est fermement liée à son site actif. Ces instantanés montrent que HECTD3 est compact plutôt qu’en forme d’anneau, avec une région catalytique classique à deux lobes à une extrémité et une région N‑terminale auparavant mystérieuse à l’autre. La moitié N‑terminale forme en réalité deux replis entièrement nouveaux, que les auteurs nomment D3NA et D3NB, disposés en une plate‑forme hélicoïdale soutenant un module DOC de liaison au substrat. Lorsque l’ubiquitine est chargée, les lobes catalytiques adoptent une configuration en L particulière, et des résidus acides spécifiques proches du site actif aident à préparer les chaînes latérales des protéines entrantes pour accepter l’étiquette. Le travail montre que, bien que HECTD3 respecte les règles générales de sa famille d’enzymes, il utilise une combinaison distincte d’éléments structuraux pour le faire.
Comment HECTD3 s’étiquette lui‑même et marque ses cibles
L’équipe a ensuite examiné quels types de motifs d’ubiquitination HECTD3 produit. Plutôt que d’allonger de longues chaînes d’un type unique, l’enzyme attache principalement plusieurs unités d’ubiquitine simples et de courtes chaînes, avec des preuves de certaines liaisons favorisant un lien connu pour promouvoir la dégradation protéique. Cela suggère que HECTD3 est mieux adapté pour initier les événements d’étiquetage que pour les étendre en longs signaux. Les auteurs se sont ensuite intéressés à une cible proposée, PARP1, un facteur de réparation de l’ADN déjà connu pour influencer les réponses aux thérapies anticancéreuses. Dans des réactions en éprouvette, HECTD3 modifiait efficacement PARP1, décorant plusieurs lysines de sa moitié de liaison à l’ADN avec des marques incluant des chaînes associées à l’élimination des protéines. En utilisant un réticulage chimique et la spectrométrie de masse, ils ont cartographié les points de contact entre HECTD3 et PARP1, confirmant que le module DOC et la région catalytique aident tous deux à positionner le substrat. La mutation de deux acides aminés exposés à la surface du DOC réduisait fortement l’étiquetage de PARP1 sans affecter la chimie de base, les désignant comme des ancrages clés pour la reconnaissance du substrat.
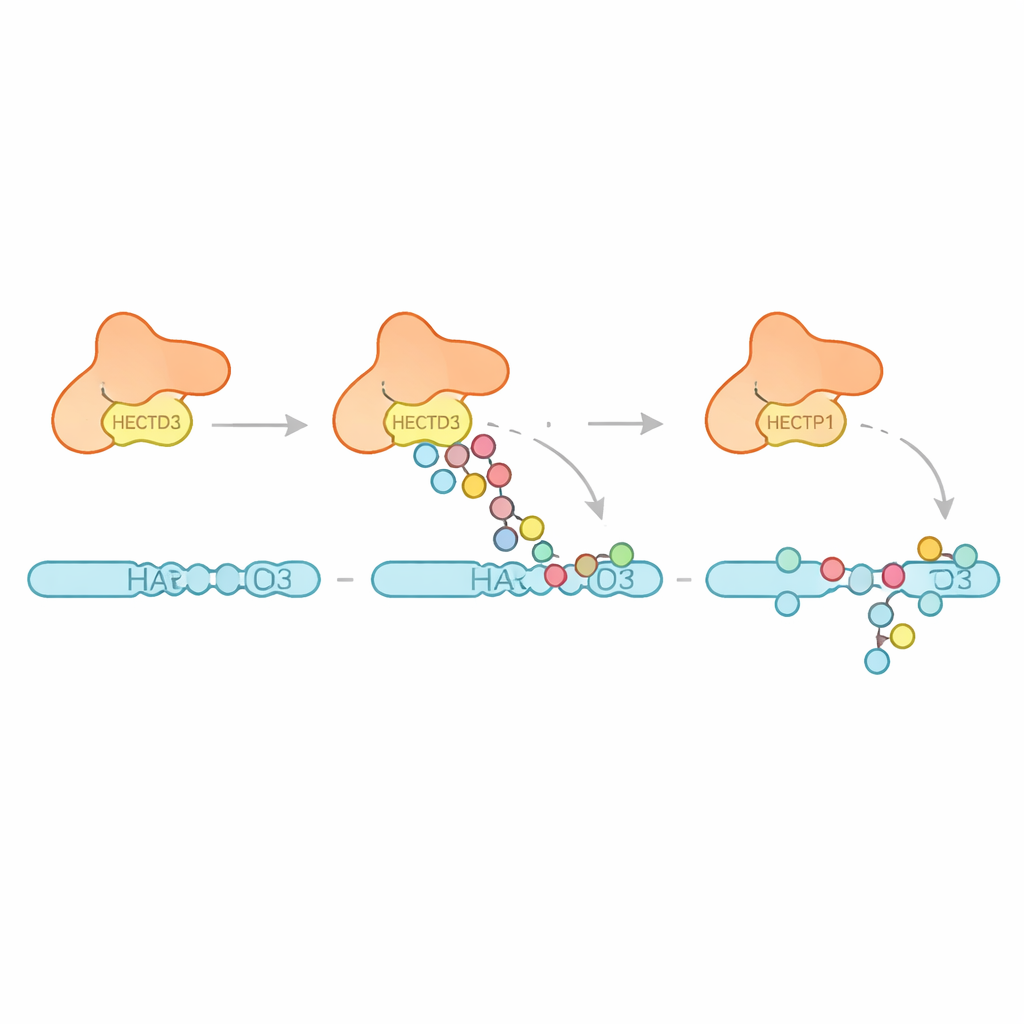
Pourquoi cela compte pour la maladie et le traitement
Ensemble, ces résultats dépeignent HECTD3 comme une machine d’étiquetage constamment active mais structurellement sophistiquée qui initie principalement les marques d’ubiquitine et s’appuie sur une région N‑terminale flexible et unique pour reconnaître des partenaires spécifiques comme PARP1. Parce que l’activité de HECTD3 est accrue dans plusieurs cancers et influence la gestion des protéines de réparation de l’ADN, comprendre sa structure et son mécanisme ouvre la voie à la conception de molécules pouvant interférer avec ses surfaces d’accrochage ou son centre catalytique. De telles interventions ciblées pourraient, en principe, modifier la façon dont les cellules décident du sort de protéines essentielles dans le cancer, l’infection et les maladies inflammatoires.
Citation: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
Mots-clés: ligase ubiquitine, HECTD3, marquage des protéines, PARP1, biologie du cancer