Clear Sky Science · it
Struttura e meccanismo della ligasi HECT HECTD3
Come le cellule marcano le loro proteine per l’azione
All’interno di ogni cellula, un minuscolo sistema di segnalazione decide quali proteine devono essere riparate, riciclate o rimodulate per nuovi compiti. Questo studio si concentra su uno degli enzimi che gestiscono questo sistema, una proteina chiamata HECTD3. HECTD3 è stata collegata al cancro, all’infiammazione e alle infezioni virali, ma il suo funzionamento a livello atomico è rimasto poco chiaro. Combinando potenti tecniche di imaging e strumenti biochimici, gli autori rivelano come è fatta HECTD3, come sceglie i suoi partner molecolari e come decora altre proteine con piccoli marcatori in grado di modificarne il destino.
Una macchina cellulare di marcatura con molti ruoli
Le cellule spesso modificano le loro proteine con una piccola molecola chiamata ubiquitina, che può comportarsi come un’etichetta colorata in un magazzino di smistamento. Catene di queste etichette, disposte in modi differenti, inviano messaggi diversi: alcune segnalano la degradazione della proteina, altre ne modulano l’attività o la localizzazione. Enzimi chiamati ligasi E3 sono responsabili di scegliere quali proteine vengono etichettate e in che modo. HECTD3 appartiene a un ramo delle ligasi E3 noto per formare un legame chimico temporaneo con l’ubiquitina prima di trasferirla al bersaglio. È insolitamente attivo in diversi tumori ed è stato implicato in processi come la morte cellulare programmata, la segnalazione immunitaria e la replicazione virale, tuttavia la sua struttura e la sua logica d’azione erano in gran parte sconosciute.
Un enzima costantemente attivo con una forma unica
I ricercatori hanno innanzitutto chiesto se HECTD3 si comporta come un interruttore che può essere acceso o spento. Molte ligasi correlate si controllano piegandosi in conformazioni auto‑inibitorie o associandosi in complessi maggiori. Attraverso test biochimici e una tecnica che misura le dimensioni delle proteine in soluzione, il gruppo ha scoperto che HECTD3 esiste principalmente come monomero e non sembra inattivarsi mediante auto‑inibizione o aggregazione stabile. Sia la porzione catalitica centrale sia la proteina a lunghezza intera sono attive, con una chiara preferenza per lavorare con una famiglia di enzimi ausiliari che trasferiscono ubiquitina. Ciò significa che HECTD3 è essenzialmente “pronto all’azione” e probabilmente regolato nelle cellule da fattori diversi dalla semplice auto‑inibizione.
Rivelata una nuova architettura proteica
Per capire come è strutturata HECTD3, gli autori hanno usato la crio‑microscopia elettronica per catturare immagini di molecole singole congelate in un sottile strato di ghiaccio. Hanno determinato strutture della proteina da sola e in uno stato in cui una molecola di ubiquitina è saldamente legata al sito attivo. Questi scatti mostrano che HECTD3 è compatta piuttosto che a forma di anello, con una classica regione catalitica a due lobi a un estremo e una regione N‑terminale precedentemente misteriosa all’altro. La metà N‑terminale risulta formare due nuovi fold, che gli autori chiamano D3NA e D3NB, disposti come una piattaforma elicoidale che sostiene un modulo DOC di legame al substrato. Quando l’ubiquitina è caricata, i lobi catalitici adottano un particolare assetto a L, e residui acidi specifici vicino al sito attivo aiutano a predisporre i gruppi laterali delle proteine in arrivo ad accettare l’etichetta. Il lavoro mostra che, sebbene HECTD3 segua le regole generali della sua famiglia enzimatica, utilizza una combinazione distintiva di elementi strutturali per farlo.
Come HECTD3 marca se stesso e i suoi bersagli
Il gruppo ha quindi esaminato che tipo di pattern di ubiquitinazione HECTD3 crea. Piuttosto che costruire lunghe catene di un singolo tipo, l’enzima principalmente aggiunge più unità singole di ubiquitina e brevi catene, con evidenze per alcune catene che favoriscono un legame noto per promuovere la degradazione proteica. Questo suggerisce che HECTD3 è più abile nell’avviare eventi di marcatura che nell’estenderli in segnali lunghi. Gli autori si sono quindi concentrati su un bersaglio proposto, PARP1, un fattore di riparazione del DNA già noto per influenzare le risposte alle terapie oncologiche. In reazioni in vitro, HECTD3 ha modificato efficacemente PARP1, decorando diversi siti lisinici nella sua metà legante il DNA con marcatori che includono catene associate alla rimozione della proteina. Usando cross‑linking chimico e spettrometria di massa, hanno mappato i punti di contatto tra HECTD3 e PARP1, confermando che sia il modulo DOC sia la regione catalitica aiutano a posizionare il substrato. La mutazione di due amminoacidi esposti sulla superficie del DOC ha ridotto nettamente la marcatura di PARP1 senza compromettere la chimica di base, evidenziandoli come ancore chiave per il riconoscimento del substrato.
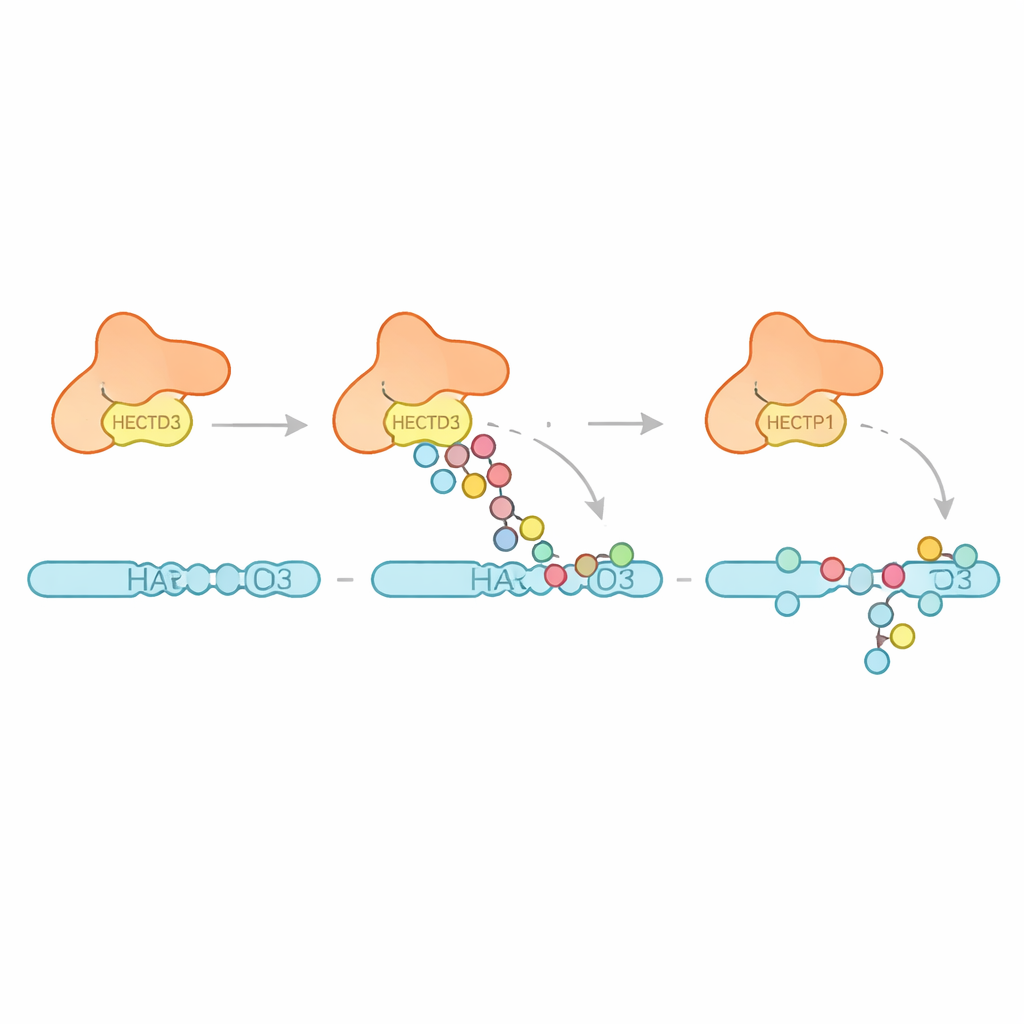
Perché questo è importante per malattie e terapie
Complessivamente, questi risultati descrivono HECTD3 come una macchina di marcatura costantemente attiva ma strutturalmente sofisticata che principalmente avvia i marchi di ubiquitina e si affida a una regione N‑terminale flessibile e unica per riconoscere partner specifici come PARP1. Poiché l’attività di HECTD3 è elevata in diversi tumori e influenza il modo in cui vengono gestite le proteine coinvolte nella riparazione del DNA, comprendere la sua struttura e il suo meccanismo apre la strada alla progettazione di molecole che interferiscano con le sue superfici di aggancio o con il centro catalitico. Interventi mirati di questo tipo potrebbero, in principio, modificare il processo decisionale delle cellule sul destino di proteine critiche nel cancro, nelle infezioni e nelle malattie infiammatorie.
Citazione: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
Parole chiave: ligasi dell'ubiquitina, HECTD3, marcatura delle proteine, PARP1, biologia del cancro