Clear Sky Science · pl
Struktura i mechanizm ligazy HECT HECTD3
Jak komórki oznaczają swoje białka
W każdej komórce istnieje drobny system sygnalizacyjny, który decyduje, które białka należy naprawić, recyklingować lub przekierować do nowych zadań. W tym badaniu skupiono się na jednym z enzymów zarządzających tym systemem — białku o nazwie HECTD3. HECTD3 wiązano z rakiem, stanami zapalnymi i infekcjami wirusowymi, ale jego działanie na poziomie atomowym pozostawało niejasne. Dzięki połączeniu zaawansowanych metod obrazowania i narzędzi biochemicznych autorzy ujawniają, jak zbudowany jest HECTD3, jak wybiera swoich partnerów molekularnych i jak przytwierdza do innych białek małe znaczki mogące zmienić ich los.
Komórkowa maszyna do znakowania o wielu rolach
Komórki często modyfikują swoje białka małą cząsteczką zwaną ubiquityną, która może działać jak kolorowy znacznik w magazynie sortującym. Łańcuchy tych znaczników, ułożone na różne sposoby, przekazują odmienne informacje: niektóre oznaczają białko do zniszczenia, inne regulują jego aktywność lub lokalizację. Enzymy zwane ligazami E3 odpowiadają za wybór białek do oznaczenia i sposób tworzenia tych oznaczeń. HECTD3 należy do gałęzi ligaz E3, które tworzą tymczasowe powiązanie chemiczne z ubiquityną, zanim przekażą ją na cel. Jest wyjątkowo aktywny w kilku typach nowotworów i powiązano go z procesami takimi jak programowana śmierć komórkowa, sygnalizacja odpornościowa i replikacja wirusów, jednak jego struktura i logika działania były w dużej mierze nieznane.
Enzym cały czas aktywny o unikalnym kształcie
Naukowcy najpierw sprawdzili, czy HECTD3 zachowuje się jak przełącznik, który można włączać lub wyłączać. Wiele pokrewnych ligaz hamuje swoją aktywność poprzez składanie się w konformacje blokujące lub przez łączenie w większe zespoły. Wykorzystując testy biochemiczne i technikę mierzącą wielkość białek w roztworze, zespół odkrył, że HECTD3 występuje przeważnie jako pojedyncza kopia i nie wydaje się wyciszany przez samoograniczanie ani trwałe składowanie. Zarówno jego rdzeniowa część katalityczna, jak i białko w pełnej długości są aktywne, z wyraźnym preferowaniem pracy z jedną rodziną pomocniczych enzymów przekazujących ubiquitynę. Oznacza to, że HECTD3 jest zasadniczo „gotowy do działania” i prawdopodobnie w komórkach kontrolowany jest przez czynniki inne niż proste samoograniczanie.
Odkrycie nowej architektury białka
Aby zrozumieć budowę HECTD3, autorzy wykorzystali krioelektronową mikroskopię, aby uchwycić obrazy pojedynczych cząsteczek zamrożonych w cienkim lodzie. Określili struktury białka w stanie wolnym oraz w stanie, gdy cząsteczka ubiquityny jest trwale związana z jego centrum aktywnym. Te migawki pokazują, że HECTD3 jest zwarty, a nie pierścieniowaty, z klasycznym dwu‑płatowym regionem katalitycznym na jednym końcu i wcześniej tajemniczym regionem N‑terminalnym na drugim. Połowa N‑terminalna okazuje się tworzyć dwie zupełnie nowe fałdy, które autorzy nazwali D3NA i D3NB, ułożone jako helicalna platforma podpierająca moduł DOC wiążący substrat. Gdy ubiquityna jest załadowana, płaty katalityczne przyjmują charakterystyczne ułożenie w kształcie litery L, a konkretne kwaśne reszty blisko centrum aktywnego pomagają przygotować łańcuchy boczne nadchodzących aminokwasów do przyjęcia znacznika. Praca pokazuje, że choć HECTD3 podąża za ogólnymi zasadami swojej rodziny enzymatycznej, wykorzystuje odmienną kombinację elementów strukturalnych do realizacji tych reguł.
Jak HECTD3 oznacza siebie i swoje cele
Następnie zespół przeanalizował, jakie wzorce ubiquitynacji tworzy HECTD3. Zamiast budować długie łańcuchy jednego typu, enzym głównie przytwierdza wiele pojedynczych jednostek ubiquityny i krótkie łańcuchy, z dowodami na obecność pewnych łączeń sprzyjających degradacji białek. Sugeruje to, że HECTD3 lepiej zaczyna procesy znakowania niż przedłuża je do długich sygnałów. Autorzy zwrócili się następnie do proponowanego celu, białka PARP1 — czynnika naprawy DNA znanego z wpływu na odpowiedź na terapię przeciwnowotworową. W reakcjach in vitro HECTD3 sprawnie modyfikował PARP1, ozdabiając kilka reszt lizyn w jego części wiążącej DNA znacznikami, w tym łańcuchami powiązanymi z usuwaniem białka. Przy użyciu chemicznego sieciowania i spektrometrii mas zmapowali punkty kontaktu między HECTD3 a PARP1, potwierdzając, że moduł DOC i region katalityczny pomagają w pozycjonowaniu substratu. Zmiana dwóch odsłoniętych aminokwasów na powierzchni DOC znacznie zmniejszyła znakowanie PARP1 bez uszczerbku dla rdzeniowej aktywności chemicznej, wskazując na nie jako kluczowe kotwice rozpoznawania substratu.
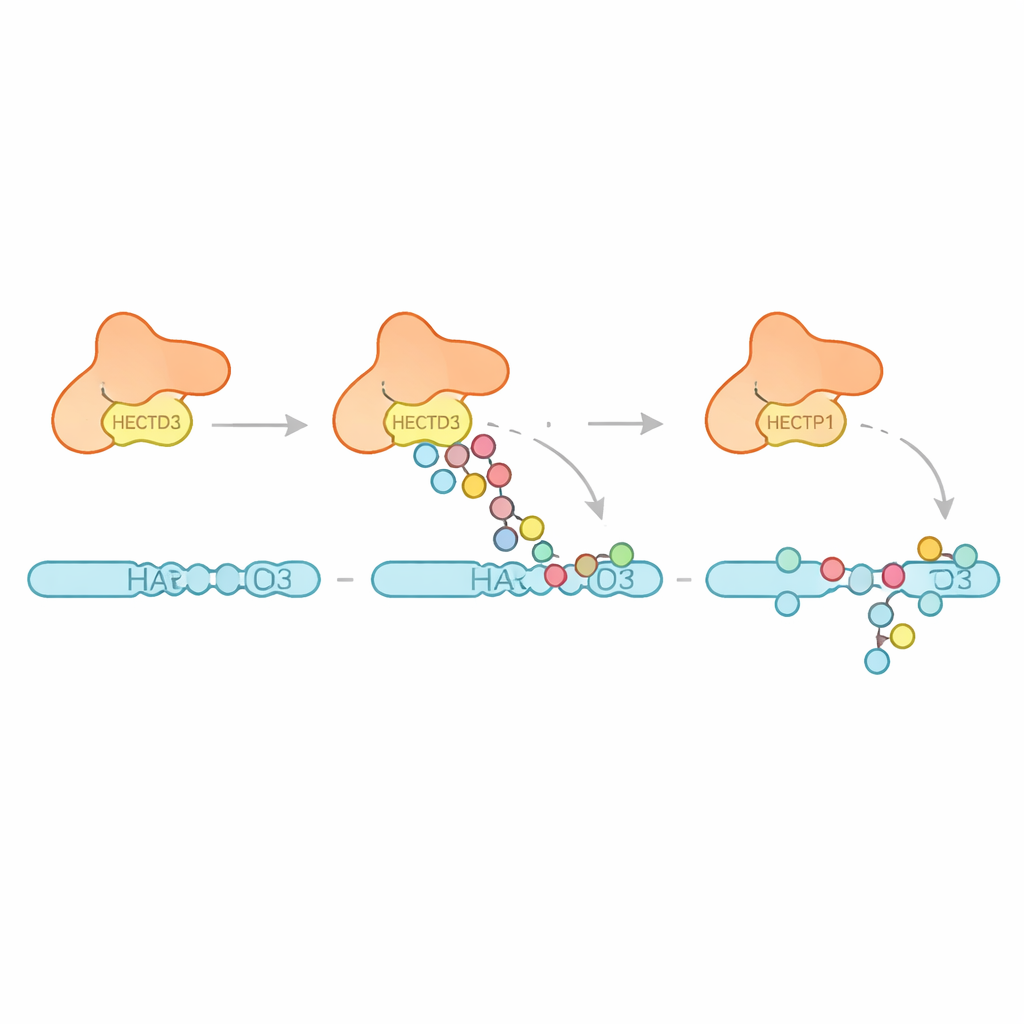
Dlaczego to ma znaczenie dla chorób i terapii
W sumie wyniki malują obraz HECTD3 jako ciągle aktywnej, ale strukturalnie wysublimowanej maszyny znakującej, która głównie inicjuje oznaczenia ubiquitynowe i polega na elastycznym, unikalnym regionie N‑terminalnym do rozpoznawania specyficznych partnerów, takich jak PARP1. Ponieważ aktywność HECTD3 jest podwyższona w kilku nowotworach i wpływa na to, jak traktowane są białka naprawy DNA, zrozumienie jego struktury i mechanizmu otwiera możliwości projektowania cząsteczek zakłócających jego powierzchnie dokujące lub centrum katalityczne. Takie ukierunkowane interwencje mogłyby potencjalnie zmieniać sposób, w jaki komórki decydują o losie kluczowych białek w raku, infekcjach i chorobach zapalnych.
Cytowanie: Huber, J., Esposito, D., Maslen, S. et al. Structure and mechanism of the HECT ligase HECTD3. Nat Commun 17, 2783 (2026). https://doi.org/10.1038/s41467-026-69520-y
Słowa kluczowe: ligaza ubiquityny, HECTD3, oznaczanie białek, PARP1, biologia nowotworów