Clear Sky Science · zh
用于药效与毒性分析的高通量多器官蛋白组学工作流
为何更快的蛋白质图谱对医学重要
我们的身体由数千种不同的蛋白质构成,这些蛋白质会随疾病和药物的作用发生变化。在多器官同时读取这些变化,对于理解治疗为何奏效、何时失败以及可能造成哪些副作用至关重要。本研究介绍了一种能够每天测量数百份组织样本的快速方法,并将其应用于一种名为L‑天冬酰胺酶(L‑asparaginase)的抗癌药,揭示了该药如何在全身范围内重塑生物学状态。
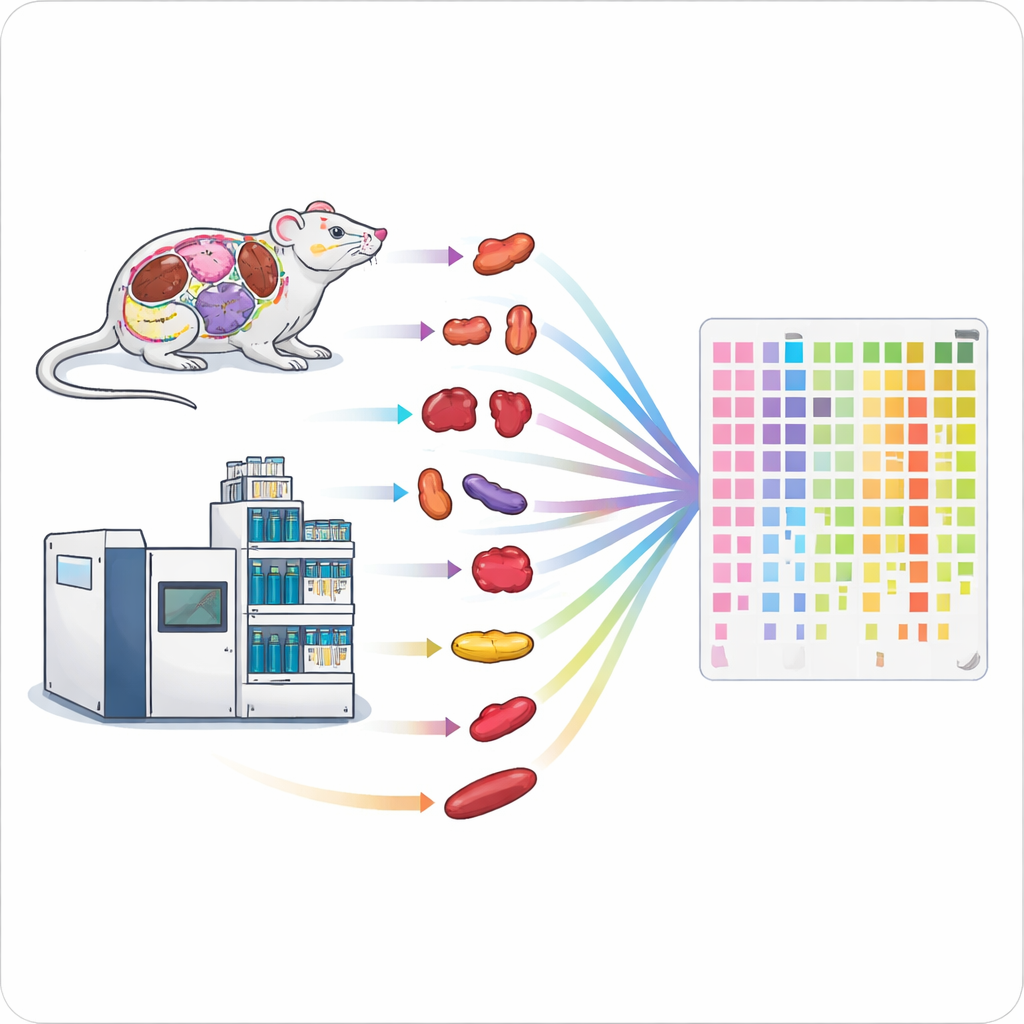
加速蛋白质生产线
传统的蛋白质测量方法既缓慢又耗时,难以用于研究整个生物体或大规模患者群体。作者将两种高性能技术——一种快速质谱和短时液相色谱运行——结合到单一简化的工作流中。通过精细调整诸如离子收集时间和扫描质量范围等参数,他们在每个样本仅一到二分钟的测量时间内实现了深入的蛋白覆盖。经优化的方案在一分钟运行中可鉴定约6,200种人类蛋白,在两分钟中约7,500种,远超早期的高通量方法。
从组织到数据在一天内完成
快速采集数据只是挑战的一半;样本制备往往是更大的瓶颈。为了解决这一问题,团队为固体组织设计了并行样本处理管线。他们使用自动化的珠状匀浆器同时破碎多达24块组织,然后在96孔板中用超声辅助将蛋白酶解为肽段,并使用专用吸头快速去盐。这种高通量管线可以在约五小时内处理96个组织样本,而标准工作流可能需要数天。对小鼠脑、肾和肺的测试显示,快速方法回收的蛋白数量相似,定量结果高度可比,但通量提高了七倍以上。
观察抗癌药在全身的作用
为了展示该平台能揭示的内容,研究者选择了L‑天冬酰胺酶,这是一种用于儿童白血病的酶类药物,但因副作用和耐药性难以在成人中重新定位。他们将小鼠分为接受标准L‑天冬酰胺酶、一种对相关氨基酸活性降低的改良版本,或对照溶液的组别,并在八天的过程中收集了13种不同器官样本。总计在507个样本中定量了超过11,000种蛋白。蛋白数据的模式清晰地区分了脑、肝和脂肪储存区等组织,并显示标准药物(而非突变体)在许多器官中引发了大范围的蛋白水平变化。血液和组织中小分子测量证实,标准药物显著耗竭了氨基酸天冬酰胺(asparagine),而突变体仅引起短暂变化,这有助于解释其疗效较弱的原因。
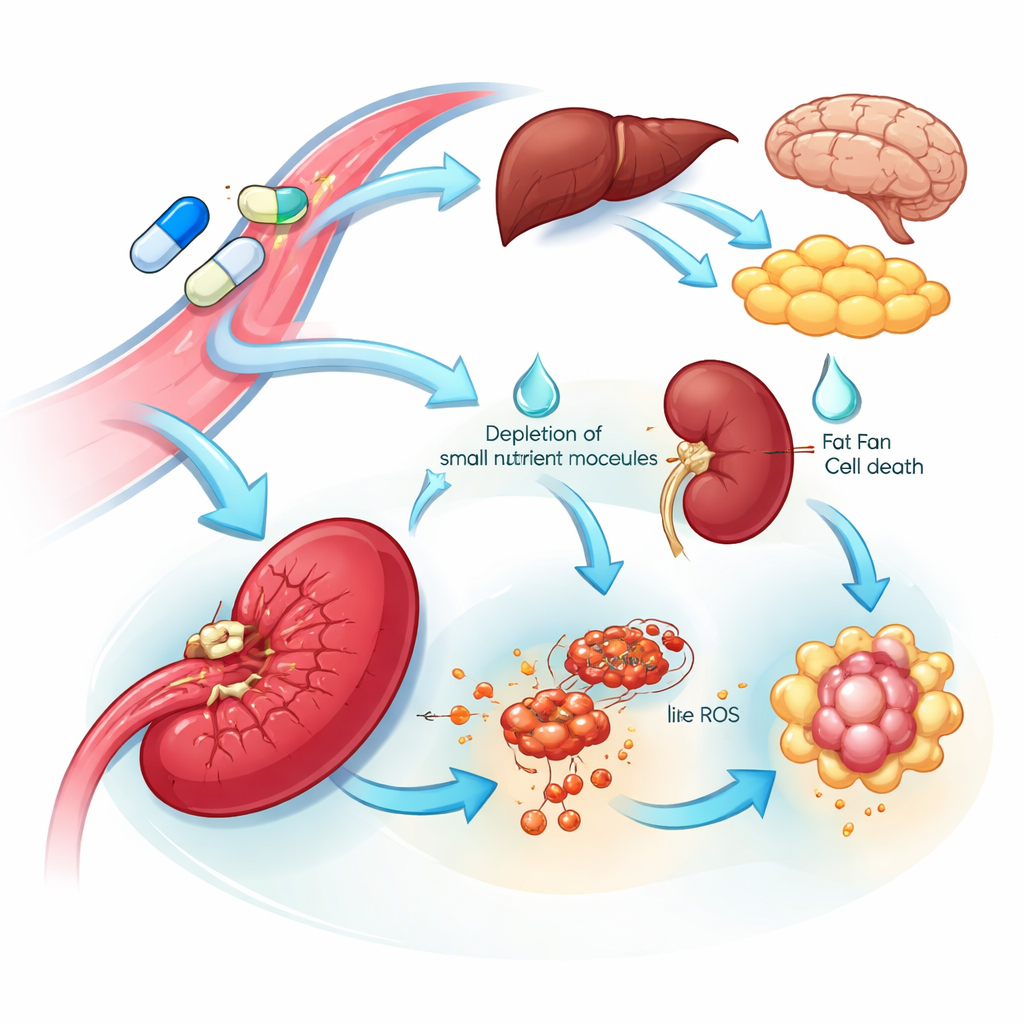
有关器官脆弱性与副作用的线索
多器官视角揭示了易受影响的靶点和潜在毒性来源。许多组织在接受L‑天冬酰胺酶处理后增加了合成天冬酰胺的酶,提示存在一种内在的耐药程序帮助恢复这一营养物质。相反,脾脏显示出该酶显著下降,并伴随相关氨基酸和DNA合成前体的减少,以及与铁依赖性细胞死亡相一致的信号。这些变化表明与脾脏相关的细胞可能对该药物特别敏感。在几乎所有器官中,标准药物——但非突变体——抑制了参与血液凝固调控和胆固醇处理的蛋白质。这种广泛且协调的下调与该药物已知的临床问题相呼应,包括血栓障碍和血液中甘油三酯升高,并指向一些可用于监测或作为干预靶点的血液蛋白,以降低这些风险。
这对未来治疗意味着什么
通过将快速、可扩展的蛋白测量管线与全身药物研究相结合,作者创建了L‑天冬酰胺酶的一种分子地图:它作用于何处、器官如何适应或未能适应,以及哪些通路将其疗效与毒性联系起来。对非专业读者而言,关键信息是:现在可以在一天内扫描跨多个器官的数千种蛋白,将复杂的药物效应转化为详细且可检验的地图。此类工作流可加速更安全癌症疗法的设计,指导剂量与给药方案的决策,并有助于识别在保留抗癌效力的同时减轻危险副作用的联合治疗策略。
引用: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
关键词: 蛋白组学, 药物毒性, 癌症治疗, 质谱, 系统生物学