Clear Sky Science · nl
High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis
Waarom snellere eiwitkaarten van belang zijn voor de geneeskunde
Ons lichaam bestaat uit duizenden verschillende eiwitten die veranderen als reactie op ziekte en medicijnen. Het gelijktijdig uitlezen van die veranderingen in meerdere organen is cruciaal om te begrijpen waarom een behandeling werkt, wanneer ze faalt en welke bijwerkingen ze kan veroorzaken. Deze studie introduceert een snelle methode om eiwitten in honderden weefselmonsters per dag te meten en past die toe op een kankerremmend middel genaamd L‑asparaginase, waarmee wordt onthuld hoe het middel de biologie door het hele lichaam herschikt.
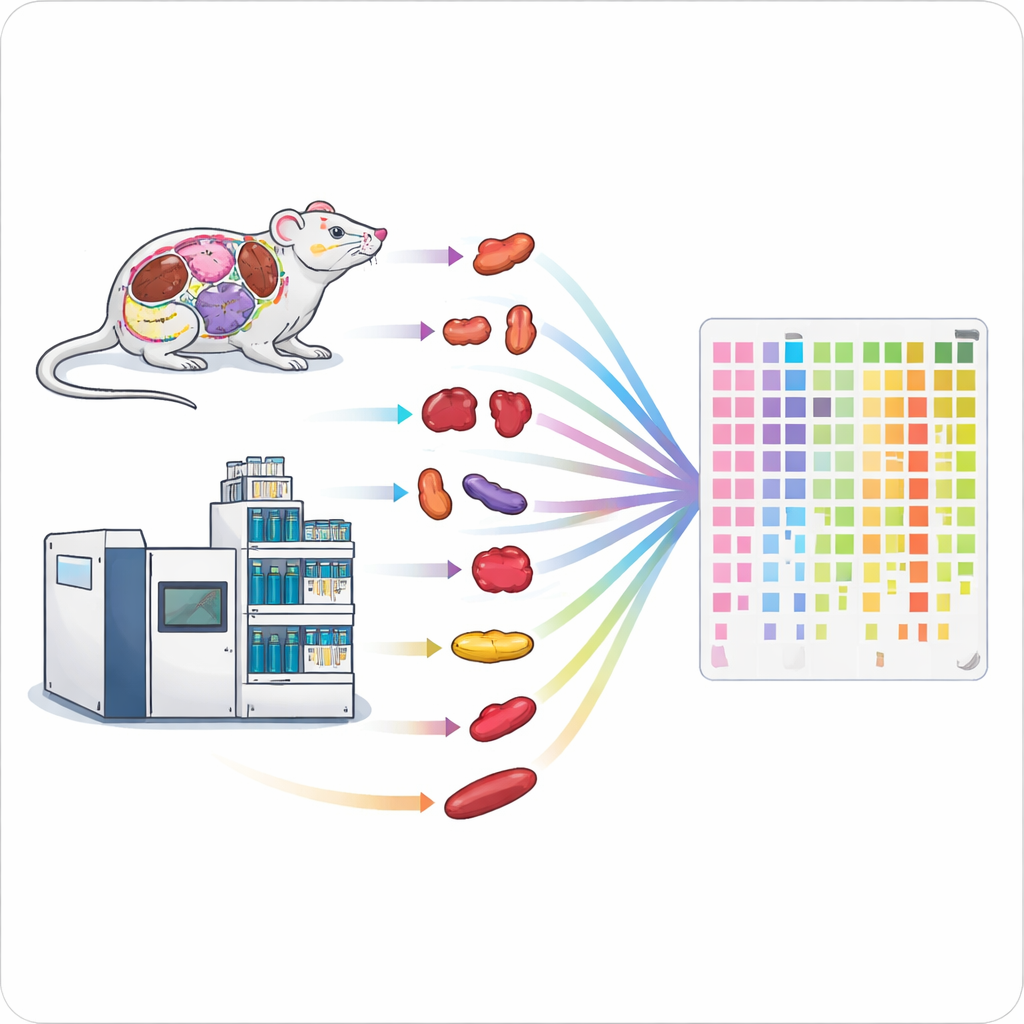
De eiwitproductielijn versnellen
Traditionele methoden om eiwitten te meten zijn traag en arbeidsintensief, waardoor het moeilijk is om hele organismen of grote patiëntengroepen te bestuderen. De auteurs combineerden twee hoogpresterende technologieën—een snel type massaspectrometrie en korte vloeistofchromatografieruns—tot één gestroomlijnde workflow. Door instellingen zorgvuldig af te stemmen, zoals hoe lang ionen worden verzameld en welke massastringen worden gescand, bereikten ze diepe eiwitdekking in slechts één tot twee minuten meettijd per monster. Hun geoptimaliseerde opstelling kon ongeveer 6.200 humane eiwitten identificeren in een run van één minuut en ongeveer 7.500 in twee minuten, wat eerdere high‑throughput methoden ver achter zich liet.
Van weefsel tot data in één dag
Snel data verzamelen is maar de helft van de uitdaging; de monsterbereiding kan een nog groter knelpunt zijn. Om dit aan te pakken ontwierp het team een parallelle monsterverwerkingspijplijn voor solide weefsels. Ze gebruikten geautomatiseerde, parelgebaseerde homogenisatoren om tot 24 weefselstukjes tegelijk open te breken, gevolgd door ultrasoongeassisteerde vertering van eiwitten tot peptiden in 96‑well platen en snelle ontzouting met gespecialiseerde tips. Deze high‑throughput pijplijn maakte het mogelijk om 96 weefsels in ongeveer vijf uur te verwerken, vergeleken met meerdere dagen met een standaardworkflow. Tests in muizenhersenen, nieren en longen toonden aan dat de snelle methode vergelijkbare aantallen eiwitten terugvond en zeer vergelijkbare kwantitatieve resultaten gaf, maar met meer dan zeven keer hogere doorvoer.
Een kankerremmer in actie door het hele lichaam
Om te demonstreren wat dit platform kan onthullen, richtten de onderzoekers zich op L‑asparaginase, een enzymatisch geneesmiddel dat wordt gebruikt bij leukemie bij kinderen en moeilijk te herbestemmen is voor volwassenen vanwege bijwerkingen en medicijnresistentie. Ze behandelden muizen met standaard L‑asparaginase, een gemodificeerde versie met verminderde activiteit op een verwant aminozuur, of een controlesolutie, en verzamelden vervolgens 13 verschillende organen over een periode van acht dagen. In totaal kwantificeerden ze meer dan 11.000 eiwitten in 507 monsters. Patronen in de eiwitdata scheidden weefsels zoals hersenen, lever en vetdepots duidelijk en lieten zien dat het standaardmiddel, maar niet de gemuteerde versie, grote verschuivingen in eiwitniveaus in veel organen veroorzaakte. Metingen van kleine moleculen in bloed en weefsels bevestigden dat het standaardmiddel het aminozuur asparagine sterk uitputte, terwijl de mutant slechts kortstondige veranderingen veroorzaakte, wat helpt verklaren waarom deze minder effectief is.
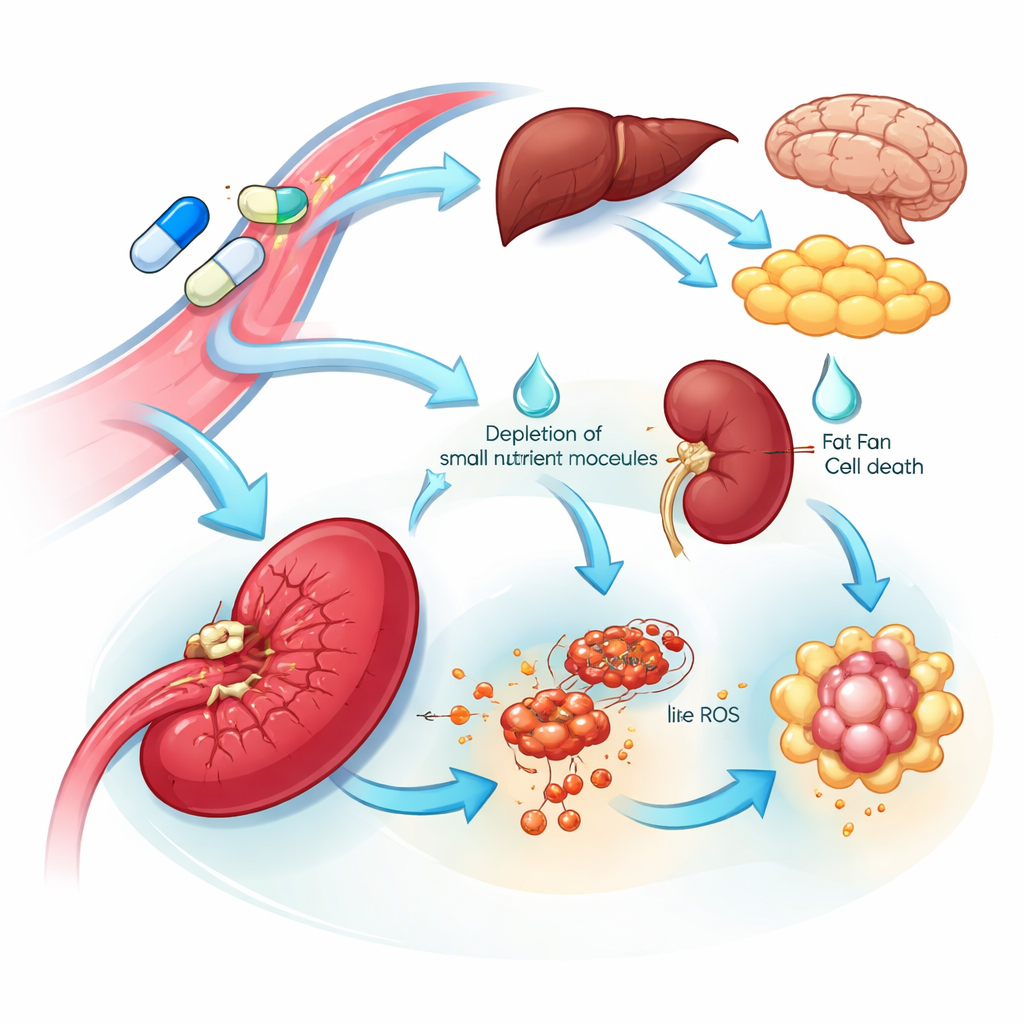
Aanwijzingen voor organengevoeligheid en bijwerkingen
De multi‑organ blik onthulde zowel kwetsbare doelen als mogelijke bronnen van toxiciteit. Veel weefsels reageerden op L‑asparaginase door het enzym dat asparagine maakt te verhogen, wat wijst op een ingebouwd resistentieprogramma dat helpt dit voedingsstofgehalte te herstellen. In tegenstelling daarmee toonde de milt een opvallende ineenstorting van dit enzym en een daling in gerelateerde aminozuren en DNA‑bouwstenen, samen met signalen consistent met ijzer‑gedreven celdood. Deze veranderingen suggereren dat miltgerelateerde cellen bijzonder gevoelig kunnen zijn voor het middel. In bijna alle organen onderdrukte het standaardmiddel—maar niet de mutant—eiwitten die betrokken zijn bij bloedstollingsregulatie en cholesterolverwerking. Deze brede, gecoördineerde terugval weerspiegelt bekende klinische problemen met het middel, waaronder stollingsstoornissen en hoge bloedtriglyceriden, en wijst op specifieke bloedproteïnen die mogelijk gemonitord of gericht kunnen worden om deze risico’s te verminderen.
Wat dit betekent voor toekomstige behandelingen
Door een snelle, schaalbare eiwitmeetpijplijn te combineren met een totaal‑lichaam medicijnstudie, creëerden de auteurs een soort moleculair atlas voor L‑asparaginase: waar het werkt, hoe organen zich aanpassen of falen zich aan te passen, en welke routes de voordelen koppelen aan de schadelijke effecten. Voor niet‑specialisten is de kernboodschap dat het nu mogelijk is om duizenden eiwitten in vele organen in slechts één dag te scannen, waardoor complexe medicijneffecten in gedetailleerde, toetsbare kaarten worden omgezet. Dergelijke workflows kunnen het ontwerp van veiligere kankertherapieën versnellen, dosering en schema‑beslissingen sturen en helpen combinatiebehandelingen te identificeren die het antikankervermogen behouden terwijl gevaarlijke bijwerkingen worden verminderd.
Bronvermelding: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
Trefwoorden: proteomics, drug toxicity, cancer therapy, mass spectrometry, systems biology