Clear Sky Science · tr
İlaç etkinliği ve toksisite analizleri için yüksek verimli çok-organ proteomik iş akışı
Neden Daha Hızlı Protein Haritaları Tıp İçin Önemli?
Vücudumuz, hastalıklar ve ilaçlara yanıt olarak değişen binlerce farklı proteinden oluşur. Birçok organ boyunca bu değişiklikleri aynı anda okumak, bir tedavinin neden işe yaradığını, ne zaman başarısız olduğunu ve hangi yan etkilere yol açabileceğini anlamanın anahtarıdır. Bu çalışma, günde yüzlerce doku örneğinde hızla protein ölçümü yapmanın bir yolunu tanıtıyor ve kanser ilacı L-asparaginaz’a uygulayarak ilacın vücut genelinde biyolojiyi nasıl yeniden şekillendirdiğini ortaya koyuyor.
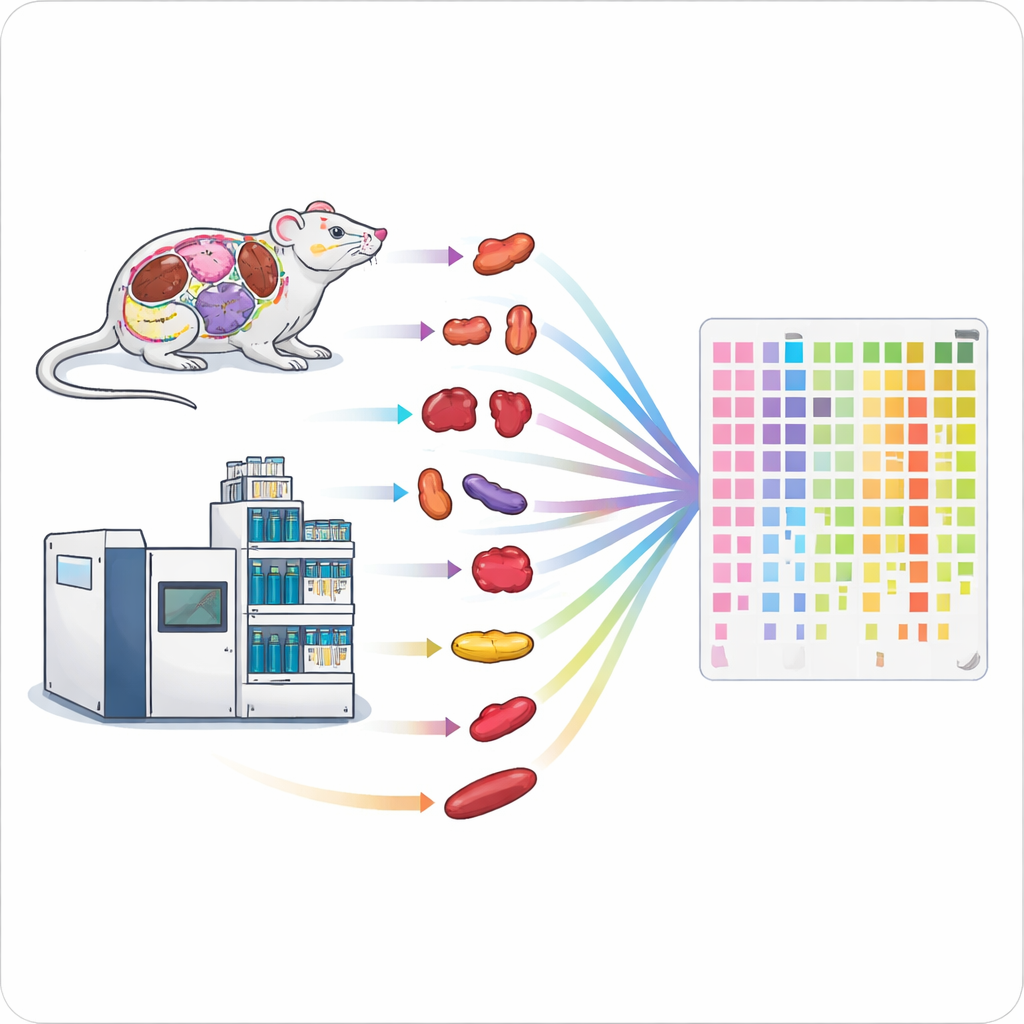
Protein Üretim Hattını Hızlandırmak
Geleneksel protein ölçüm yöntemleri yavaş ve emek yoğun olup tüm organizmaları veya geniş hasta gruplarını incelemeyi zorlaştırır. Yazarlar, yüksek performanslı iki teknolojiyi—hızlı bir kütle spektrometresi türü ve kısa sıvı kromatografisi çalıştırmalarını—tek bir sadeleştirilmiş iş akışında birleştirdi. İyonların ne kadar süre toplandığı ve hangi kütle aralıklarının tarandığı gibi ayarları dikkatle ayarlayarak her örnek için yalnızca bir ila iki dakikalık ölçüm süresinde derin protein kapsamı elde ettiler. Optimize edilmiş düzenekleri, bir dakikalık çalıştırmada yaklaşık 6.200 insan proteini ve iki dakikada yaklaşık 7.500 proteini tanımlayabilecekti; bu, önceki yüksek verimli yöntemleri önemli ölçüde geride bırakıyor.
Tek Günde Dokudan Veriye
Veriyi hızlı toplamak işin yarısıdır; örnek hazırlama çoğu zaman daha büyük bir darboğaz olabilir. Bunu çözmek için ekip, katı dokular için paralel bir örnek işleme hattı tasarladı. Aynı anda 24 doku parçasını açmak için otomatik boncuk bazlı homojenizatörler kullandılar, ardından 96 kuyucuklu plakalar içinde proteinleri peptidlere dönüştürmek için ultrason destekli sindirim ve özel uçlarla hızlı tuz giderme uyguladılar. Bu yüksek verimli hat, standart bir iş akışıyla birkaç gün süren işlemlere kıyasla yaklaşık beş saatte 96 dokunun işlenmesine izin verdi. Fare beyni, böbrek ve akciğerinde yapılan testler, hızlı yöntemin benzer sayıda protein geri kazandığını ve nicel sonuçların yüksek oranda karşılaştırılabilir olduğunu gösterdi; üstelik verim yaklaşık yedi kat daha yüksekti.
Bir Kanser İlacının Bütün Vücutta Nasıl Davrandığını İzlemek
Bu platformun neler ortaya koyabileceğini göstermek için araştırmacılar L-asparaginaz’a yöneldiler; çocukluk lösemisinde kullanılan ancak yan etkiler ve ilaç direnci nedeniyle yetişkinlere yeniden uygulaması zor olan bir enzim ilacı. Fareleri standart L-asparaginaz, ilişkili bir aminoaside daha düşük aktivite gösteren modifiye bir versiyon veya kontrol çözeltisi ile tedavi ettiler ve sekiz günlük süre boyunca 13 farklı organı topladılar. Toplamda 507 örnek üzerinden 11.000’den fazla protein nicelendi. Protein verilerindeki desenler beyin, karaciğer ve yağ dokuları gibi dokuları net şekilde ayırdı ve standart ilacın—mutant versiyon değil—birçok organda büyük protein düzeyi değişimleri tetiklediğini gösterdi. Kan ve dokulardaki küçük molekül ölçümleri, standart ilacın asparagin aminoasitini güçlü şekilde tükettiğini doğrularken, mutantın sadece kısa süreli değişiklikler yarattığını gösterdi; bu da onun neden daha az etkili olduğunu açıklamaya yardımcı oluyor.
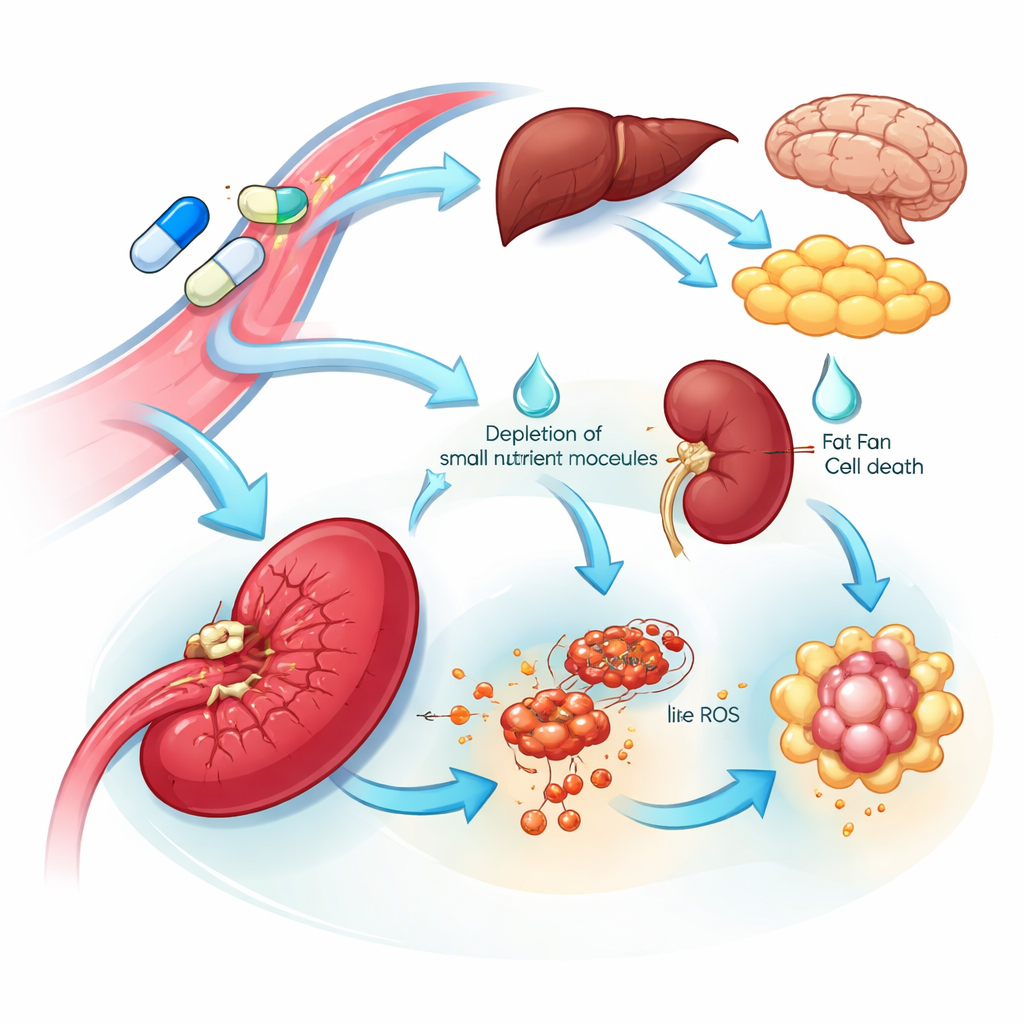
Organ Duyarlılığı ve Yan Etkiler İçin İpuçları
Çok-organ bakışı hem savunmasız hedefleri hem de toksisite potansiyeli taşıyan kaynakları ortaya çıkardı. Birçok doku L-asparaginaz’a, asparagin üreten enzimin seviyesini artırarak yanıt verdi; bu, besini yeniden sağlamak için yerleşik bir direnç programına işaret ediyor. Buna karşın dalak, bu enzimde çarpıcı bir çöküş ve ilgili aminoasitler ile DNA yapı taşlarında azalma gösterdi; buna ek olarak demir kaynaklı hücre ölümü ile uyumlu sinyaller gözlendi. Bu değişiklikler, dalakla ilişkili hücrelerin ilaca özellikle duyarlı olabileceğini öne sürüyor. Neredeyse tüm organlarda, standart ilaç—mutant değil—kan pıhtılaşmasının düzenlenmesi ve kolesterol yönetiminde görevli proteinleri baskıladı. Bu geniş, koordine düşüş, ilacın bilinen klinik sorunlarını—kan pıhtılaşma bozuklukları ve yüksek kan trigliseritleri de dahil—yansıtıyor ve bu riskleri azaltmak için izlenebilecek veya hedeflenebilecek belirli kan proteinlerine işaret ediyor.
Gelecek Tedaviler İçin Anlamı
Hızlı, ölçeklenebilir bir protein ölçüm hattını tüm vücut ilaç çalışmasıyla eşleştirerek yazarlar, L-asparaginaz için bir tür moleküler atlas oluşturdular: ilacın nerede etkin olduğu, organların nasıl uyum sağladığı veya uyum sağlayamadığı ve hangi yolakların yararlarını zararlarla bağladığı. Uzman olmayanlar için temel mesaj, artık binlerce proteini birçok organda yalnızca bir gün içinde taramanın mümkün olduğudur; bu sayede karmaşık ilaç etkileri ayrıntılı, test edilebilir haritalara dönüşüyor. Bu tür iş akışları daha güvenli kanser tedavilerinin tasarımını hızlandırabilir, doz ve zamanlama kararlarını yönlendirebilir ve antikanser gücü korurken tehlikeli yan etkileri azaltacak kombinasyon tedavilerini belirlemeye yardımcı olabilir.
Atıf: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
Anahtar kelimeler: proteomik, ilaç toksisitesi, kanser tedavisi, kütle spektrometrisi, sistem biyolojisi