Clear Sky Science · ja
薬効と毒性解析のための高スループット多臓器プロテオミクスワークフロー
医療においてより速いタンパク質マップが重要な理由
私たちの体は、病気や薬に応じて変化する何千もの異なるタンパク質で構成されています。複数の臓器にわたるこれらの変化を同時に読み取ることは、治療がなぜ効くのか、いつ失敗するのか、どのような副作用が生じるのかを理解するうえで重要です。本研究は、1日に何百もの組織サンプルでタンパク質を迅速に測定する手法を紹介し、小児白血病治療に用いられるL-アスパラギナーゼというがん薬を対象に適用することで、薬が体全体の生物学をどのように再形成するかを明らかにします。
タンパク質の組み立てラインを加速する
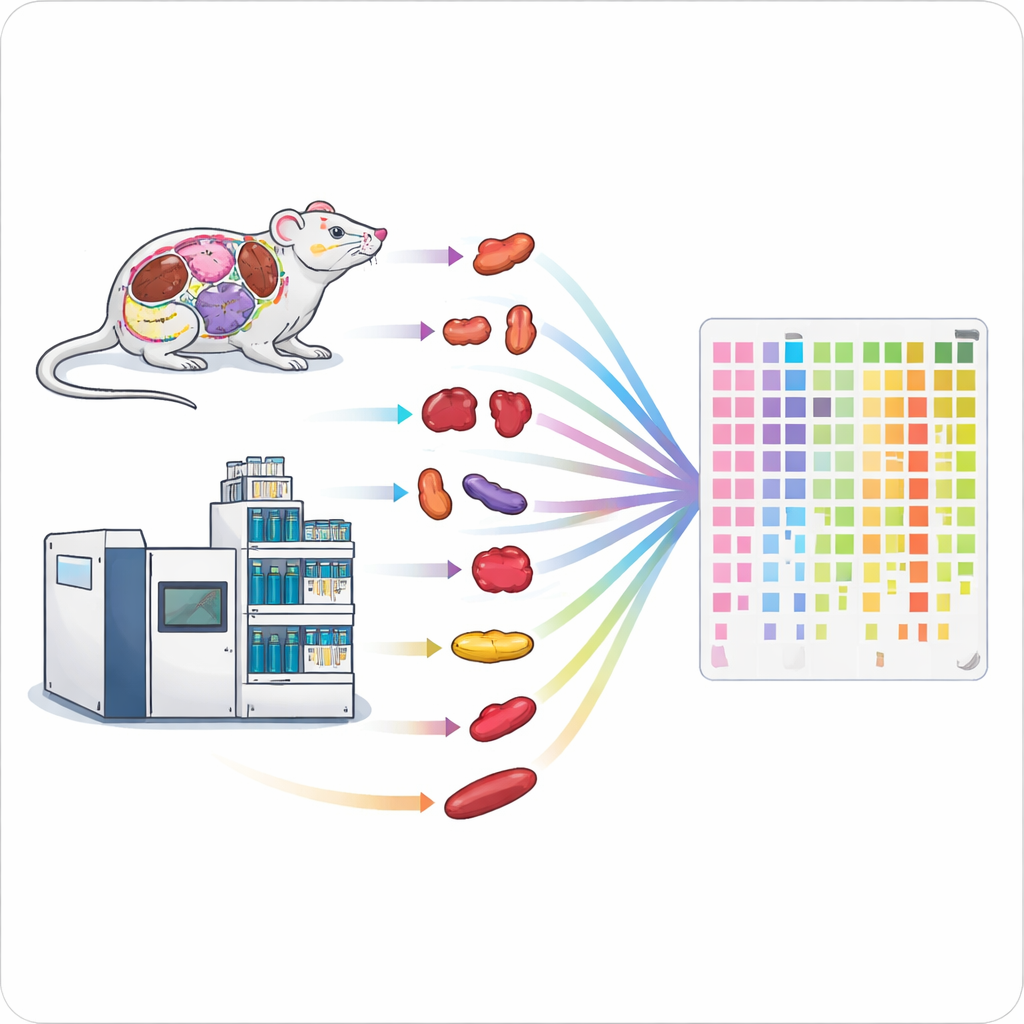
従来のタンパク質測定法は遅く手間がかかるため、生物全体や大規模な患者群の研究が困難でした。著者らは、高速なタイプの質量分析と短い液体クロマトグラフィー走行を組み合わせ、単一の効率的なワークフローに統合しました。イオンの収集時間やスキャンする質量範囲などの設定を慎重に調整することで、サンプルあたりわずか1〜2分の測定で深いタンパク質カバレッジを達成しました。最適化されたセットアップでは、1分間の走行で約6,200種類、2分間で約7,500種類のヒトタンパク質を同定でき、従来の高スループット法を大きく上回りました。
組織からデータへ、1日で完結
データ収集の迅速化は半分の戦いにすぎません。サンプル前処理がさらに大きなボトルネックになることがあります。これに対処するため、チームは固形組織の並列処理パイプラインを設計しました。自動ビーズベースのホモジナイザーで最大24個の組織片を同時に破砕し、その後96穴プレートで超音波支援消化によりタンパク質をペプチドに変換し、専用のチップで迅速に脱塩する手順を採用しました。この高スループットパイプラインにより、96検体を約5時間で処理でき、従来のワークフローで数日かかるのと比べて大幅に短縮されました。マウスの脳、腎臓、肺での試験では、迅速法は回収されるタンパク質の数が同等で、定量結果も高く相関していましたが、スループットは7倍以上向上していました。
がん薬の全身作用を観察する
このプラットフォームが何を明らかにできるかを示すため、研究者らはL-アスパラギナーゼに着目しました。これは小児白血病で用いられる酵素薬で、副作用や耐性のため成人への転用が難しい薬です。彼らはマウスに標準のL-アスパラギナーゼ、関連アミノ酸に対する活性を低下させた改変型、あるいは対照溶液を投与し、8日間にわたって13種の臓器を収集しました。合計で507サンプルを横断して11,000を超えるタンパク質を定量しました。タンパク質データのパターンは脳、肝臓、脂肪組織などの臓器を明瞭に分け、標準薬は改変型とは異なり多くの臓器で大規模なタンパク質レベルの変化を引き起こすことを示しました。血液と組織中の小分子の測定は、標準薬がアスパラギンを強く枯渇させる一方で、改変型は短時間の変化しか引き起こさないことを確認し、改変型の効果が弱い理由を説明しています。
臓器の脆弱性と副作用の手がかり
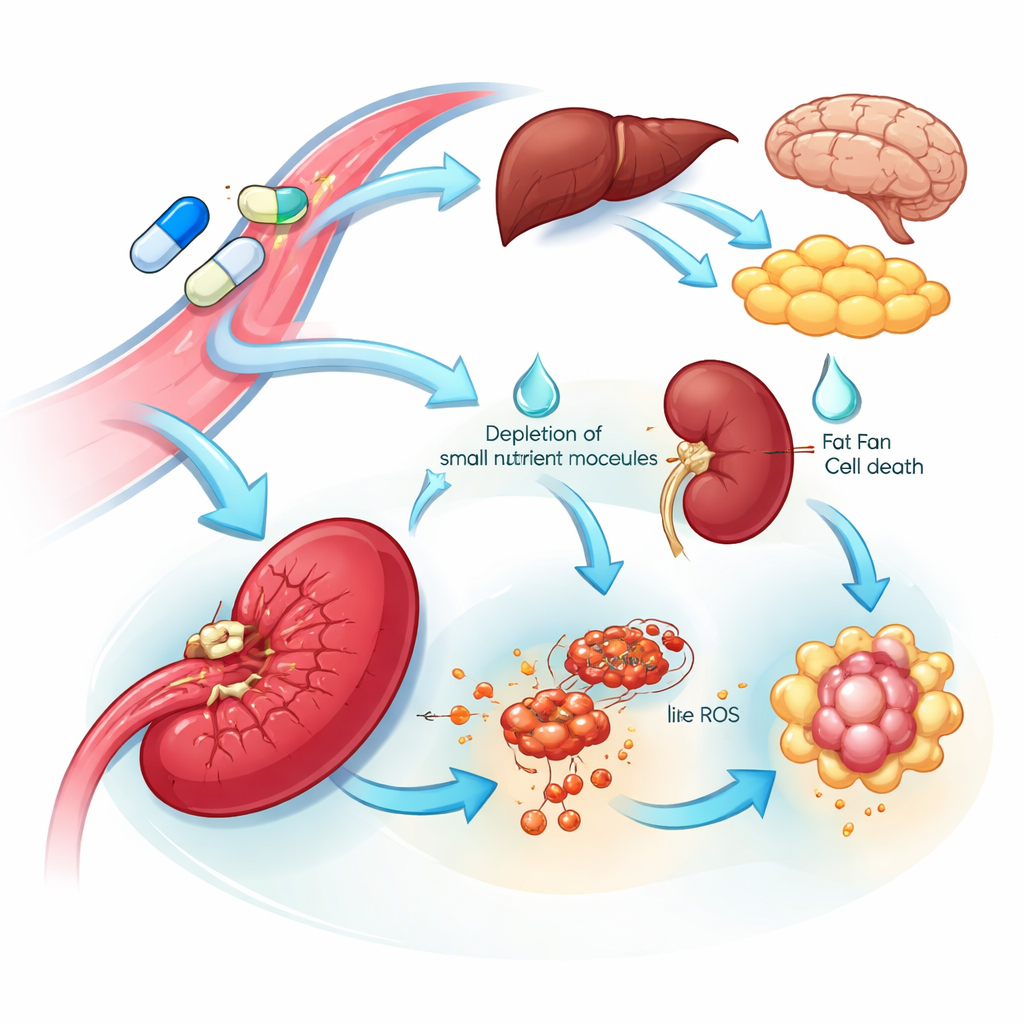
多臓器の視点は、脆弱な標的と毒性の潜在的な発生源の両方を明らかにしました。多くの組織はL-アスパラギナーゼに応答してアスパラギンを合成する酵素を増加させており、これはこの栄養素を回復するための内在的な耐性プログラムを示唆します。一方で脾臓ではこの酵素が著しく低下し、関連するアミノ酸やDNA合成の構成要素も減少し、鉄依存性の細胞死と整合するシグナルが観察されました。これらの変化は脾臓由来の細胞が薬に特に感受性が高い可能性を示しています。ほぼすべての臓器にわたり、標準薬は改変型と異なり血液凝固調節やコレステロール代謝に関与するタンパク質を抑制しました。この広範で協調的な低下は、血栓症や高トリグリセリド血症など薬に関連する既知の臨床問題を反映しており、これらのリスクを低減するために監視または標的化できる特定の血中タンパク質を示唆します。
将来の治療にとっての意味
高速でスケーラブルなタンパク質測定パイプラインと全身規模の薬物研究を組み合わせることで、著者らはL-アスパラギナーゼの分子アトラスのようなものを作成しました:どこで作用し、臓器がどのように適応または適応失敗するか、そしてその利益と有害性を結ぶ経路は何か。専門外の人に向けた主要なメッセージは、今や多数の臓器にまたがる何千ものタンパク質をわずか1日で走査し、複雑な薬効を詳細で検証可能な地図に変えることが可能になったという点です。このようなワークフローは、より安全ながん治療の設計を加速し、投与量や投与スケジュールの決定を導き、抗がん効果を保ちながら危険な副作用を和らげる併用療法の同定に役立つ可能性があります。
引用: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
キーワード: プロテオミクス, 薬物毒性, がん治療, 質量分析, システム生物学