Clear Sky Science · sv
Höghastighets-proteomik för flera organ: arbetsflöde för analys av läkemedelseffektivitet och toxicitet
Varför snabbare proteinkartor är viktiga för medicinen
Våra kroppar består av tusentals olika proteiner som förändras vid sjukdom och som svar på läkemedel. Att läsa dessa förändringar över många organ samtidigt är avgörande för att förstå varför en behandling fungerar, när den misslyckas och vilka biverkningar den kan orsaka. Den här studien presenterar ett snabbt sätt att mäta proteiner i hundratals vävnadsprover per dag och tillämpar det på ett cancerläkemedel kallat L‑asparaginas, vilket visar hur läkemedlet omformar biologin i hela kroppen.
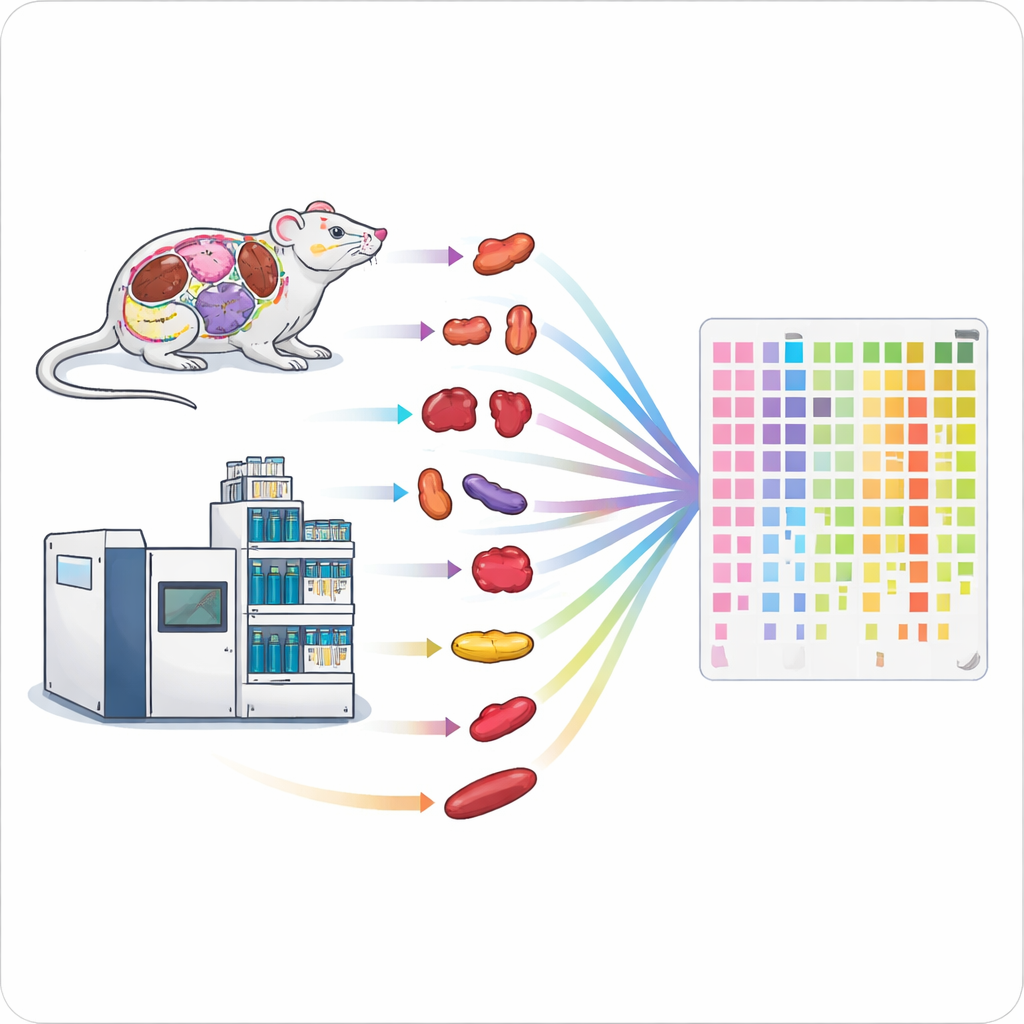
Påskyndar protein‑linan
Traditionella metoder för att mäta proteiner är långsamma och arbetsintensiva, vilket försvårar studier av hela organismer eller stora patientgrupper. Författarna kombinerade två högpresterande tekniker — en snabb typ av masspektrometri och korta kromatografilöpningar — till ett enda strömlinjeformat arbetsflöde. Genom noggrann finjustering av inställningar som hur länge joner samlas in och vilka massintervall som skannas uppnådde de djup täckning av proteomet på bara en till två minuter mätning per prov. Deras optimerade uppställning kunde identifiera ungefär 6 200 mänskliga proteiner i en ettminutskörning och cirka 7 500 på två minuter, långt över tidigare höghastighetsmetoder.
Från vävnad till data på en enda dag
Att samla in data snabbt är bara halva striden; att förbereda proven kan vara en ännu större flaskhals. För att lösa detta designade teamet en parallell provhanteringskedja för solida vävnader. De använde automatiserade pärlbaserade homogenisatorer för att öppna upp till 24 vävnadsbitar samtidigt, följt av ultraljudsassisterad digestion av proteiner till peptider i 96‑brunnsplattor och snabb avsaltning med specialiserade tips. Detta höghastighetsarbetsflöde möjliggjorde bearbetning av 96 vävnader på cirka fem timmar, jämfört med flera dagar med en standardmetod. Tester i musens hjärna, njure och lunga visade att den snabba metoden återvann liknande antal proteiner och gav mycket jämförbara kvantitativa resultat, men med mer än sju gånger högre genomströmning.
Observera ett cancerläkemedels verkan över hela kroppen
För att demonstrera vad denna plattform kan avslöja vände forskarna sig till L‑asparaginas, ett enzymläkemedel som används vid barnleukemi och som är svårt att återanvända för vuxna på grund av biverkningar och läkemedelsresistens. De behandlade möss med standard L‑asparaginas, en modifierad variant med minskad aktivitet mot en närbesläktad aminosyra, eller en kontrolllösning, och samlade sedan in 13 olika organ över en åttadagarsperiod. Totalt kvantifierade de mer än 11 000 proteiner i 507 prover. Mönster i proteindatan separerade tydligt vävnader som hjärna, lever och fettdepåer och visade att standardläkemedlet, men inte den muterade varianten, utlöste stora förändringar i proteinnivåer över många organ. Mätningar av småmolekyler i blod och vävnader bekräftade att standardläkemedlet kraftigt uttömde aminosyran asparagin, medan mutanten endast orsakade kortvariga förändringar, vilket bidrar till att förklara varför den är mindre effektiv.
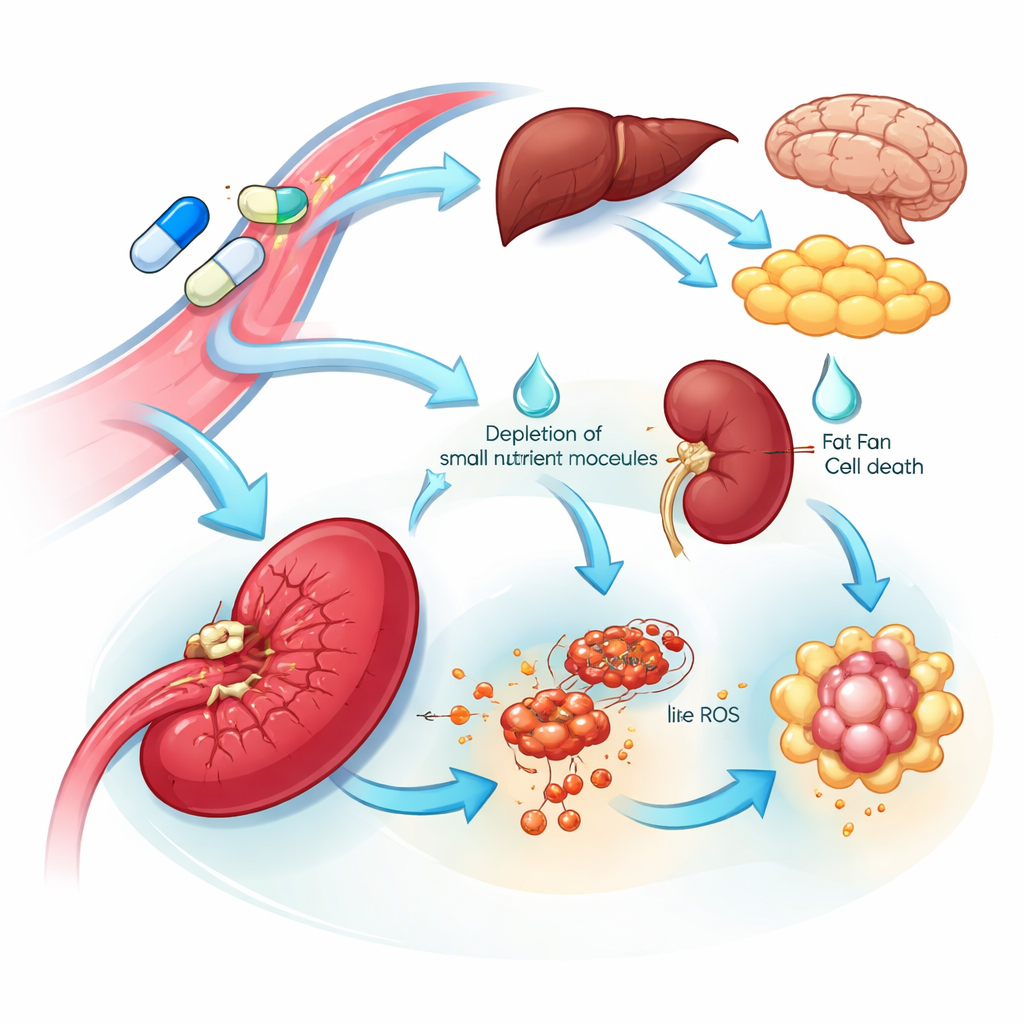
Ledtrådar till organsårbarhet och biverkningar
Flera organs samlade vy avslöjade både sårbara mål och potentiella källor till toxicitet. Många vävnader svarade på L‑asparaginas genom att öka enzymet som tillverkar asparagin, vilket tyder på ett inbyggt resistensprogram som hjälper till att återställa denna näringsämne. I kontrast visade mjälten en dramatisk kollaps i detta enzym och en minskning av relaterade aminosyror och DNA‑byggstenar, tillsammans med signaler förenliga med järn‑driven celldöd. Dessa förändringar tyder på att mjältrelaterade celler kan vara särskilt känsliga för läkemedlet. I nästan alla organ undertryckte standardläkemedlet — men inte mutanten — proteiner involverade i blodkoagulationsreglering och kolesterolhantering. Denna breda, koordinerade nedreglering speglar kända kliniska problem med läkemedlet, inklusive blodproppsbesvär och höga blodtriglycerider, och pekar på specifika blodproteiner som kan övervakas eller riktas mot för att minska dessa risker.
Vad detta betyder för framtida behandlingar
Genom att para ihop en snabb, skalbar pipeline för proteinmätning med en helkropps läkemedelsstudie skapade författarna en slags molekylär atlas för L‑asparaginas: var det verkar, hur organ anpassar sig eller misslyckas med att anpassa sig, och vilka vägar som länkar dess fördelar till dess skador. För icke‑specialister är huvudbudskapet att det nu är möjligt att skanna tusentals proteiner över många organ på bara en dag, vilket förvandlar komplexa läkemedelseffekter till detaljerade, testbara kartor. Sådana arbetsflöden kan påskynda utformningen av säkrare cancerterapier, vägleda doserings‑ och schema‑beslut och hjälpa till att identifiera kombinationsbehandlingar som bevarar anticancer‑effekt samtidigt som farliga biverkningar dämpas.
Citering: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
Nyckelord: proteomik, läkemedelstoxicitet, cancerterapi, masspektrometri, systembiologi