Clear Sky Science · ru
Высокопроизводительный мультиорганный протеомный рабочий процесс для анализа эффективности и токсичности лекарств
Почему быстрые «карты» белков важны для медицины
Наше тело состоит из тысяч различных белков, которые меняются в ответ на болезни и лекарства. Считывание этих изменений одновременно в нескольких органах — ключ к пониманию того, почему лечение работает, когда оно даёт сбой и какие побочные эффекты может вызывать. В этом исследовании представлен быстрый способ измерения белков в сотнях образцов тканей в день, который применили к противораковому препарату L‑аспарагиназе, показав, как лекарство перестраивает биологию по всему организму.
Ускорение «сборочной линии» белков
Традиционные методы измерения белков медленные и трудоёмкие, что затрудняет изучение целых организмов или больших групп пациентов. Авторы объединили две высокопроизводительные технологии — быстрый тип масс‑спектрометрии и короткие хроматографические прогонки — в единый оптимизированный рабочий процесс. Тонкая настройка параметров, таких как время накопления и сканируемые диапазоны масс, позволила получить глубокое покрытие белков всего за одну‑две минуты измерения на образец. Их оптимизированная система могла обнаружить примерно 6 200 белков человека за одну‑минутный прогон и около 7 500 за две минуты, что существенно превосходит ранние высокопроизводительные методы.
От ткани до данных за один день
Быстрый сбор данных — лишь половина задачи; подготовка образцов часто оказывается ещё большим узким местом. Чтобы решить эту проблему, команда разработала параллельный конвейер обработки твёрдых тканей. Они использовали автоматизированные гомогенизаторы на основе бусинок для разрушения до 24 фрагментов ткани одновременно, затем проводили ультразвуковую ферментативную расщепление белков до пептидов в 96‑луночных планшетах и быструю десалтировку с помощью специализированных наконечников. Этот высокопроизводительный конвейер позволял обработать 96 образцов тканей примерно за пять часов вместо нескольких дней при стандартном рабочем процессе. Испытания на мозге, почке и лёгком мышей показали, что быстрый метод восстанавливает сопоставимое число белков и даёт высоко соизмеримые количественные результаты, но с более чем семикратным повышением пропускной способности.
Наблюдая действие противоракового препарата по всему телу
Чтобы продемонстрировать возможности платформы, исследователи обратились к L‑аспарагиназе — ферментному препарату, применяемому при детской лейкемии и трудному к перепрофилированию для взрослых из‑за побочных эффектов и резистентности. Мышей лечили стандартной L‑аспарагиназой, модифицированной версией с пониженной активностью к родственной аминокислоте или контрольным раствором, и собирали 13 различных органов в течение восьми дней. В сумме они количественно охарактеризовали более 11 000 белков в 507 образцах. Шаблоны в данных белков чётко разделяли ткани, такие как мозг, печень и жировые депо, и показали, что стандартный препарат, но не мутант, вызывал значительные сдвиги уровней белков во многих органах. Измерения малых молекул в крови и тканях подтвердили, что стандартный препарат резко истощал аминокислоту аспарагин, тогда как мутант вызывал лишь кратковременные изменения, что помогает объяснить его меньшую эффективность.
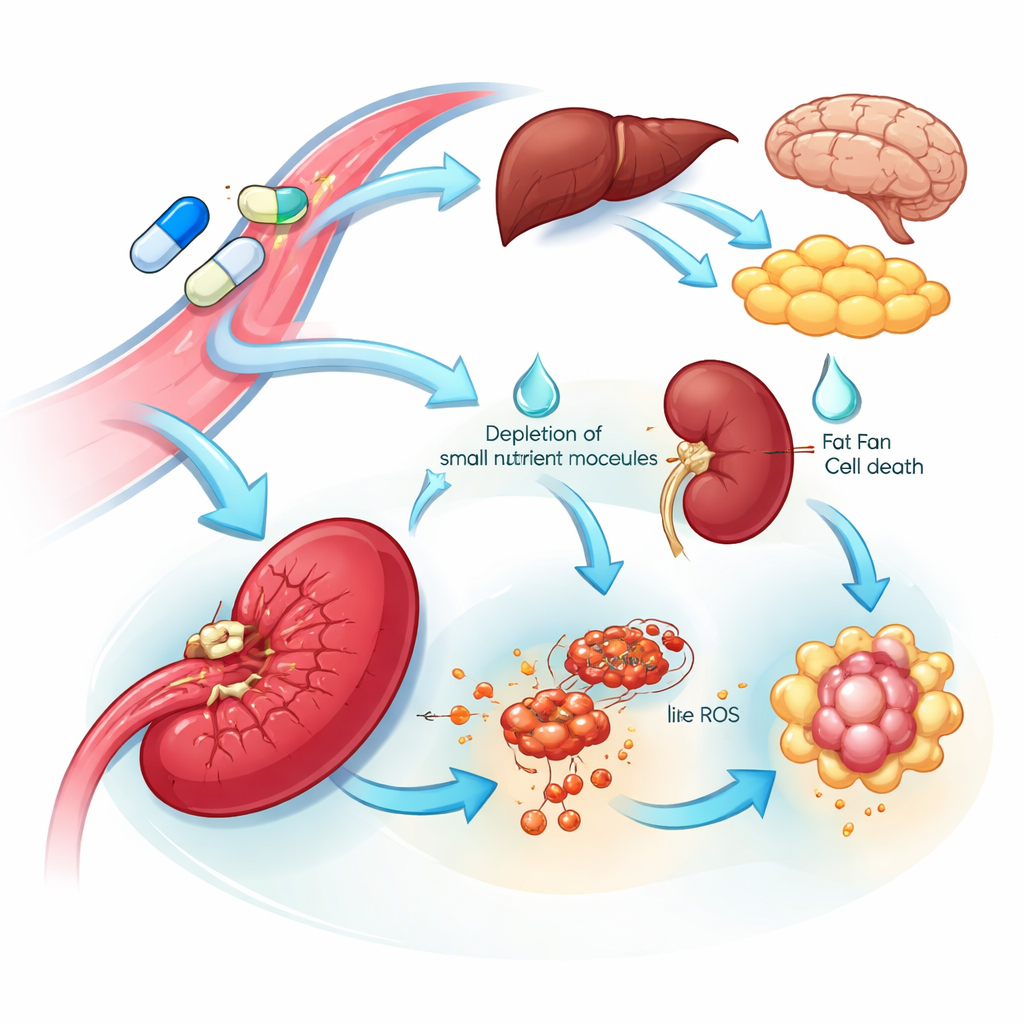
Подсказки об уязвимости органов и источниках побочных эффектов
Мультиорганный взгляд выявил как уязвимые мишени, так и потенциальные источники токсичности. Многие ткани реагировали на L‑аспарагиназу усилением фермента, синтезирующего аспарагин, что указывает на встроенную программу резистентности, помогающую восстановить этот нутриент. Напротив, селезёнка демонстрировала резкое падение этого фермента и снижение родственных аминокислот и строительных блоков ДНК, а также признаки, совместимые с железозависимой гибелью клеток. Эти изменения предполагают, что клетки, связанные с селезёнкой, могут быть особенно чувствительны к препарату. Почти во всех органах стандартный препарат — но не мутант — подавлял белки, вовлечённые в регуляцию свертывания крови и обращение холестерина. Это широкое, скоординированное понижение отражает известные клинические проблемы с препаратом, включая расстройства свертываемости и высокий уровень триглицеридов в крови, и указывает на конкретные белки крови, за которыми можно наблюдать или которые можно целенаправленно модифицировать, чтобы снизить эти риски.
Что это означает для будущих терапий
Сочетая быстрый масштабируемый конвейер измерения белков с исследованием воздействия препарата на весь организм, авторы создали нечто вроде молекулярного атласа для L‑аспарагиназы: где она действует, как органы адаптируются или не адаптируются и какие пути связывают её пользу с вредом. Для неспециалистов ключевое сообщение в том, что теперь возможно просканировать тысячи белков по многим органам всего за один день, превращая сложные эффекты лекарств в детализированные и проверяемые карты. Такие рабочие процессы могут ускорить разработку более безопасных противораковых терапий, помочь в выборе доз и режимов и содействовать выявлению комбинированных схем лечения, которые сохраняют противоопухолевую силу, одновременно смягчая опасные побочные эффекты.
Цитирование: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
Ключевые слова: протеомика, токсичность лекарств, терапия рака, масс-спектрометрия, системная биология