Clear Sky Science · de
Hochdurchsatz-Multi-Organ-Proteomik-Workflow für die Analyse von Wirkstoffwirksamkeit und -toxizität
Warum schnellere Proteinlandkarten für die Medizin wichtig sind
Unsere Körper bestehen aus Tausenden verschiedener Proteine, die sich als Reaktion auf Krankheiten und Medikamente verändern. Diese Veränderungen gleichzeitig in vielen Organen zu erfassen, ist entscheidend, um zu verstehen, warum eine Behandlung wirkt, wann sie versagt und welche Nebenwirkungen sie verursachen kann. Diese Studie stellt eine schnelle Methode vor, um Proteine in Hunderten von Gewebeproben pro Tag zu messen, und wendet sie auf ein Krebsmedikament namens L‑Asparaginase an, wobei aufgezeigt wird, wie das Medikament die Biologie im gesamten Körper umgestaltet.
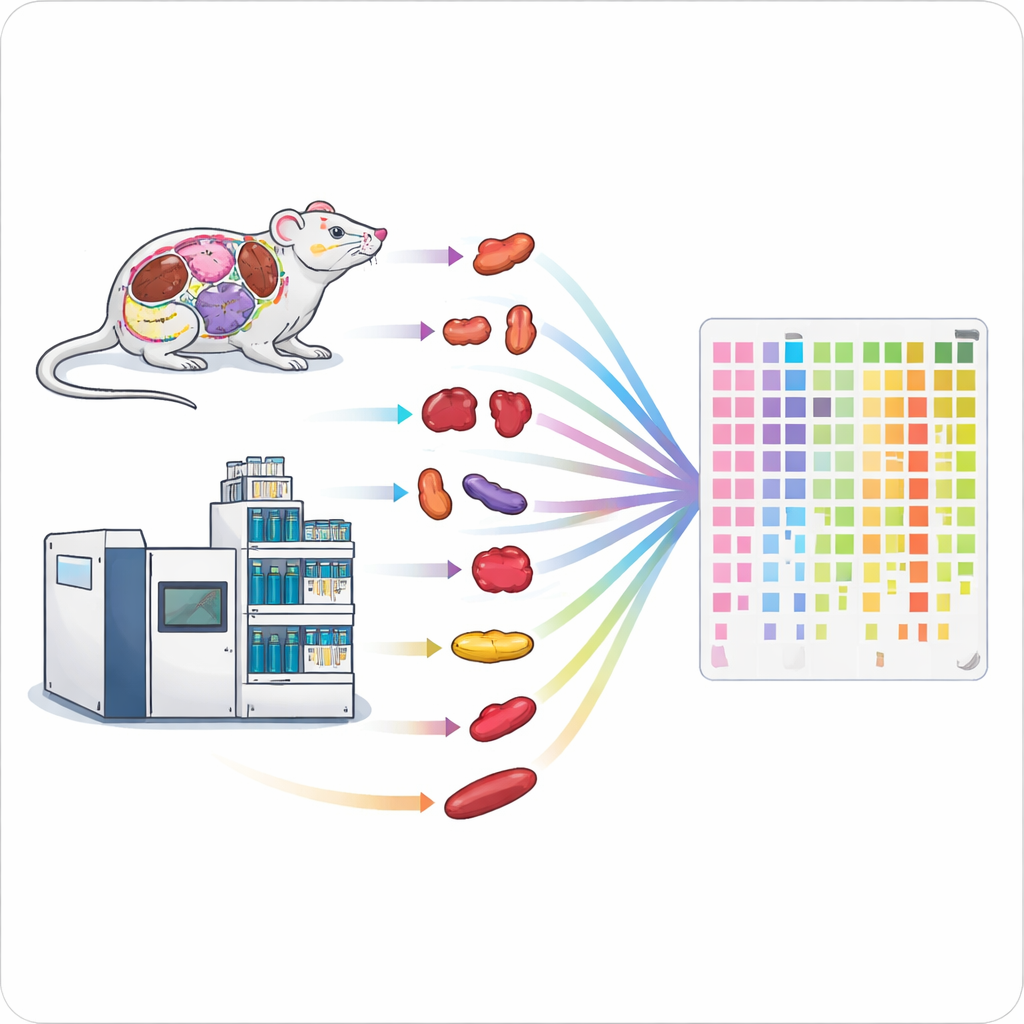
Beschleunigung der Protein-Fertigungsstraße
Traditionelle Methoden zur Messung von Proteinen sind langsam und arbeitsintensiv, was es schwierig macht, ganze Organismen oder große Patientengruppen zu untersuchen. Die Autoren kombinierten zwei leistungsstarke Technologien — eine schnelle Form der Massenspektrometrie und kurze Flüssigchromatographie‑Läufe — zu einem einzigen optimierten Workflow. Durch sorgfältiges Abstimmen von Parametern wie der Ionensammelzeit und den gescannten Massebereichen erreichten sie eine tiefe Proteindeckung in nur ein bis zwei Minuten Messzeit pro Probe. Ihre optimierte Einrichtung konnte in einem einminütigen Durchlauf etwa 6.200 humane Proteine und in zwei Minuten rund 7.500 identifizieren und übertraf damit frühere Hochdurchsatzmethoden deutlich.
Vom Gewebe zu Daten in einem einzigen Tag
Schnelle Datenerhebung ist nur die halbe Miete; die Probenvorbereitung kann ein noch größeres Nadelöhr darstellen. Um dem zu begegnen, entwarf das Team eine parallele Probenverarbeitungs‑Pipeline für festes Gewebe. Sie nutzten automatisierte, per Beads betriebene Homogenisierer, um bis zu 24 Gewebestücke gleichzeitig zu zerkleinern, gefolgt von ultraschallunterstützter Verdauung der Proteine zu Peptiden in 96‑Well‑Platten und schnellem Desalting mit spezialisierten Spitzen. Diese Hochdurchsatz‑Pipeline erlaubte die Verarbeitung von 96 Geweben in etwa fünf Stunden, verglichen mit mehreren Tagen bei einem Standardworkflow. Tests an Mausgehirn, Niere und Lunge zeigten, dass die schnelle Methode ähnliche Proteinanzahlen wiedergewann und hochvergleichbare quantitative Ergebnisse lieferte, jedoch mit mehr als siebenfach höherem Durchsatz.
Beobachtung der Wirkung eines Krebsmedikaments im ganzen Körper
Um zu demonstrieren, was diese Plattform aufdecken kann, untersuchten die Forscher L‑Asparaginase, ein Enzym‑Medikament, das bei Kinderleukämie eingesetzt wird und sich bei Erwachsenen wegen Nebenwirkungen und Arzneimittelresistenz nur schwer wiederverwenden lässt. Sie behandelten Mäuse mit standardmäßiger L‑Asparaginase, einer modifizierten Version mit verringerter Aktivität gegenüber einer verwandten Aminosäure, oder mit einer Kontrolllösung und entnahmen dann über einen Zeitraum von acht Tagen 13 verschiedene Organe. Insgesamt quantifizierten sie mehr als 11.000 Proteine in 507 Proben. Muster in den Protein‑Daten trennten Gewebe wie Gehirn, Leber und Fettdepots deutlich und zeigten, dass das Standardpräparat — nicht jedoch die mutierte Version — in vielen Organen große Verschiebungen der Proteinmengen auslöste. Messungen kleiner Moleküle in Blut und Geweben bestätigten, dass das Standardmedikament die Aminosäure Asparagin stark reduzierte, während die Mutante nur kurzzeitige Änderungen verursachte, was erklärt, warum sie weniger wirksam ist.
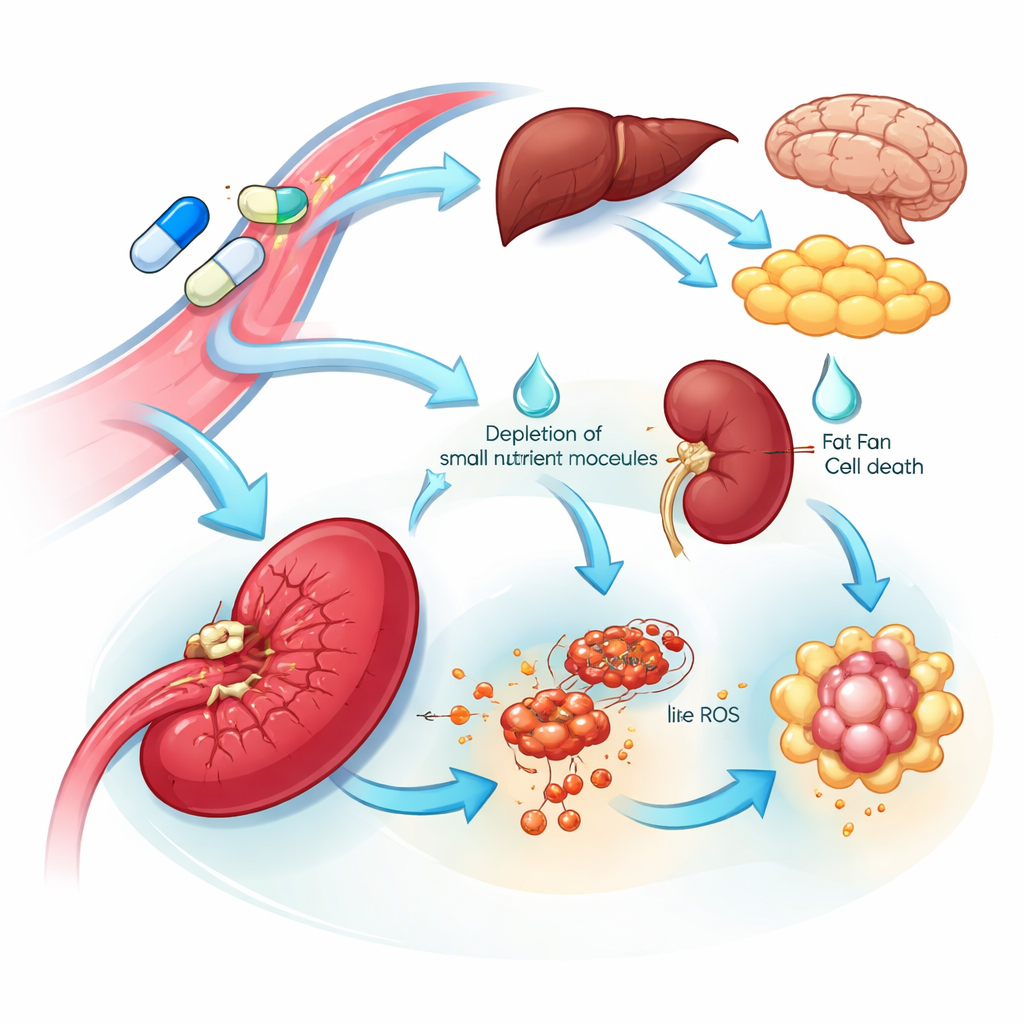
Hinweise auf Organverwundbarkeit und Nebenwirkungen
Die Multi‑Organ‑Sicht enthüllte sowohl verwundbare Ziele als auch mögliche Quellen von Toxizität. Viele Gewebe reagierten auf L‑Asparaginase mit einer Erhöhung des Enzyms, das Asparagin herstellt, was auf ein eingebautes Resistenzprogramm hindeutet, das hilft, diesen Nährstoff wiederherzustellen. Im Gegensatz dazu zeigte die Milz einen auffälligen Zusammenbruch dieses Enzyms sowie einen Rückgang verwandter Aminosäuren und DNA‑Bausteine, zusammen mit Signalen, die auf eisengetriebene Zellsterblichkeit hindeuten. Diese Veränderungen deuten darauf hin, dass milzbezogene Zellen besonders empfindlich gegenüber dem Medikament sein könnten. In nahezu allen Organen unterdrückte das Standardmedikament — nicht jedoch die Mutante — Proteine, die an der Blutgerinnungsregulation und dem Cholesterinstoffwechsel beteiligt sind. Dieser breite, koordinierte Rückgang spiegelt bekannte klinische Probleme des Medikaments wider, einschließlich Gerinnungsstörungen und hoher Blutfetttriglyceride, und weist auf spezifische Blutproteine hin, die überwacht oder gezielt werden könnten, um diese Risiken zu verringern.
Was das für künftige Behandlungen bedeutet
Durch die Kombination einer schnellen, skalierbaren Proteinmess‑Pipeline mit einer Ganzkörper‑Wirkstoffstudie schufen die Autoren eine Art molekularen Atlas für L‑Asparaginase: wo sie wirkt, wie Organe sich anpassen oder nicht anpassen und welche Signalwege Nutzen und Schaden verbinden. Für Nicht‑Spezialisten lautet die Kernbotschaft, dass es jetzt möglich ist, Tausende von Proteinen über viele Organe hinweg in nur einem Tag zu erfassen und komplexe Arzneimitteleffekte in detaillierte, prüfbare Karten zu verwandeln. Solche Workflows könnten die Entwicklung sichererer Krebstherapien beschleunigen, Dosierungs‑ und Zeitplanzuentscheidungen leiten und helfen, Kombinationstherapien zu identifizieren, die die krebsbekämpfende Wirkung erhalten und gleichzeitig gefährliche Nebenwirkungen abschwächen.
Zitation: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
Schlüsselwörter: Proteomik, Medikamententoxizität, Krebstherapie, Massenspektrometrie, Systembiologie