Clear Sky Science · pt
Fluxo de trabalho proteômico multiórganos de alto rendimento para análise de eficácia e toxicidade de fármacos
Por que mapas de proteínas mais rápidos importam para a medicina
Nossos corpos são formados por milhares de proteínas diferentes que se alteram em resposta a doenças e medicamentos. Ler essas mudanças em muitos órgãos ao mesmo tempo é fundamental para entender por que um tratamento funciona, quando falha e quais efeitos colaterais pode causar. Este estudo apresenta uma maneira rápida de medir proteínas em centenas de amostras de tecido por dia e a aplica a um medicamento contra o câncer chamado L‑asparaginase, revelando como o fármaco remodela a biologia por todo o corpo.
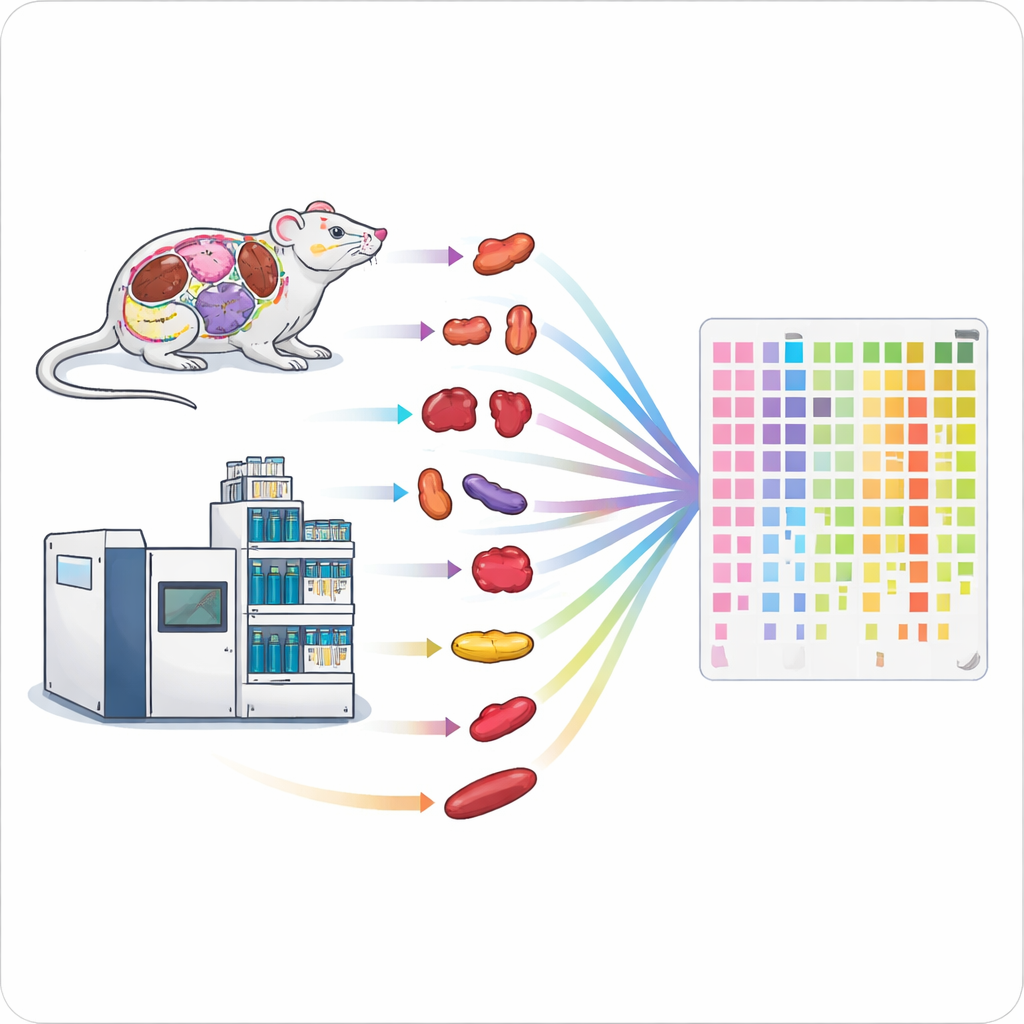
Acelerando a linha de montagem das proteínas
Os métodos tradicionais para medir proteínas são lentos e exigem muito trabalho, dificultando o estudo de organismos inteiros ou de grandes grupos de pacientes. Os autores combinaram duas tecnologias de alto desempenho — um tipo rápido de espectrometria de massa e corridas curtas de cromatografia líquida — em um fluxo de trabalho unificado. Ao ajustar cuidadosamente parâmetros como o tempo de acumulação de íons e as faixas de massa analisadas, conseguiram ampla cobertura proteica em apenas um a dois minutos de medição por amostra. A configuração otimizada pôde identificar cerca de 6.200 proteínas humanas em uma corrida de um minuto e cerca de 7.500 em duas minutos, superando amplamente métodos anteriores de alto rendimento.
Do tecido aos dados em um único dia
Coletar dados rapidamente é apenas metade da batalha; preparar as amostras pode ser um gargalo ainda maior. Para resolver isso, a equipe projetou um pipeline paralelo de manuseio de amostras para tecidos sólidos. Eles usaram homogenizadores automatizados baseados em esferas para romper até 24 pedaços de tecido ao mesmo tempo, seguidos por digestão assistida por ultrassom das proteínas em peptídeos em placas de 96 poços e dessorção rápida usando ponteiras especializadas. Esse pipeline de alto rendimento permitiu processar 96 tecidos em cerca de cinco horas, em comparação com vários dias usando um fluxo de trabalho padrão. Testes em cérebro, rim e pulmão de camundongo mostraram que o método rápido recuperou números semelhantes de proteínas e produziu resultados quantitativos altamente comparáveis, porém com mais de sete vezes maior rendimento.
Observando um medicamento contra o câncer agir por todo o corpo
Para demonstrar o que essa plataforma pode revelar, os pesquisadores se voltaram para a L‑asparaginase, uma enzima medicamentosa usada na leucemia infantil que é difícil de reaplicar em adultos devido a efeitos colaterais e resistência ao fármaco. Eles trataram camundongos com L‑asparaginase padrão, uma versão modificada com atividade reduzida sobre um aminoácido relacionado, ou uma solução controle, e então coletaram 13 órgãos diferentes ao longo de um curso de oito dias. No total, quantificaram mais de 11.000 proteínas em 507 amostras. Padrões nos dados proteicos separaram claramente tecidos como cérebro, fígado e depósitos de gordura e mostraram que o fármaco padrão, mas não a versão mutante, desencadeou grandes mudanças nos níveis de proteínas em muitos órgãos. Medições de pequenas moléculas no sangue e nos tecidos confirmaram que o fármaco padrão esgotou fortemente o aminoácido asparagina, enquanto o mutante causou apenas alterações breves, ajudando a explicar por que é menos eficaz.
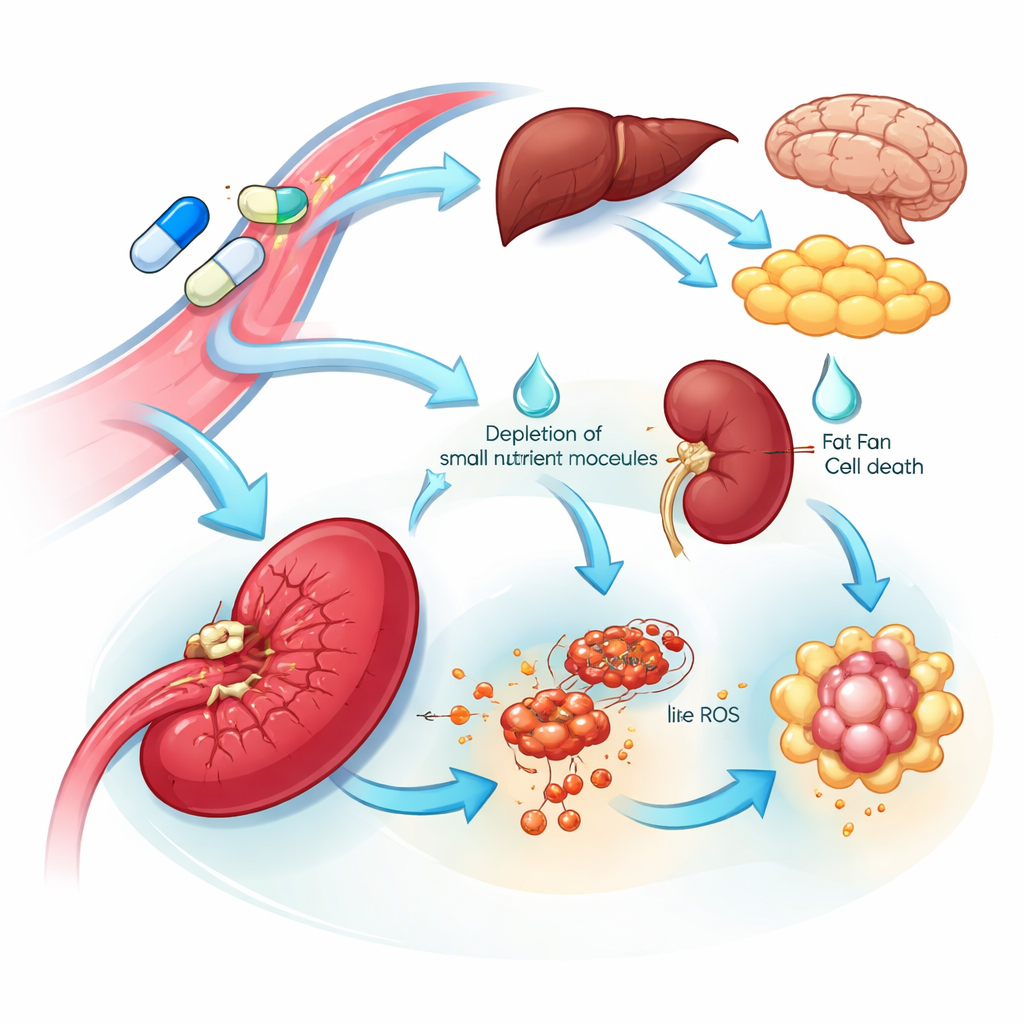
Pistas sobre vulnerabilidade de órgãos e efeitos colaterais
A visão multiórganos revelou tanto alvos vulneráveis quanto potenciais fontes de toxicidade. Muitos tecidos responderam à L‑asparaginase aumentando a enzima que sintetiza asparagina, sugerindo um programa de resistência intrínseco que ajuda a restaurar esse nutriente. Em contraste, o baço mostrou um colapso marcante dessa enzima e uma queda em aminoácidos relacionados e blocos de construção do DNA, junto com sinais consistentes com morte celular mediada por ferro. Essas alterações sugerem que células ligadas ao baço podem ser particularmente sensíveis ao fármaco. Em quase todos os órgãos, o fármaco padrão — mas não o mutante — suprimiu proteínas envolvidas na regulação da coagulação sanguínea e no manejo do colesterol. Essa redução ampla e coordenada reflete problemas clínicos conhecidos do fármaco, incluindo distúrbios de coagulação e triglicerídeos elevados, e aponta para proteínas sanguíneas específicas que poderiam ser monitoradas ou alvo de intervenções para reduzir esses riscos.
O que isso significa para tratamentos futuros
Ao emparelhar um pipeline de medição proteica rápido e escalável com um estudo de fármaco em todo o corpo, os autores criaram uma espécie de atlas molecular para a L‑asparaginase: onde ela age, como os órgãos se adaptam ou não, e quais vias ligam seus benefícios aos danos. Para não especialistas, a mensagem principal é que agora é possível escanear milhares de proteínas em muitos órgãos em apenas um dia, transformando efeitos complexos de medicamentos em mapas detalhados e testáveis. Esses fluxos de trabalho poderiam acelerar o desenvolvimento de terapias contra o câncer mais seguras, orientar decisões de dose e cronograma e ajudar a identificar tratamentos combinados que preservem o poder anticâncer ao mesmo tempo em que atenuem efeitos colaterais perigosos.
Citação: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
Palavras-chave: proteômica, toxicidade de medicamentos, terapia do câncer, espectrometria de massa, biologia de sistemas