Clear Sky Science · ar
سير عمل بروتيومي عالي الإنتاجية لقياس فعالية الأدوية وسميتها عبر أعضاء متعددة
لماذا تهم خرائط البروتين الأسرع الطبّ
أجسامنا مكوّنة من آلاف البروتينات المختلفة التي تتغير استجابة للأمراض والأدوية. قراءة تلك التغيرات عبر أعضاء متعددة في آن واحد أساسية لفهم لماذا ينجح علاج ما، ومتى يفشل، وما الآثار الجانبية التي قد يسببها. تقدم هذه الدراسة طريقة سريعة لقياس البروتينات في مئات عينات الأنسجة يوميًا وتطبّقها على دواء سرطان يُدعى إل‑أسباراجيناز، كاشفةً كيف يعيد الدواء تشكيل العمليات البيولوجية في الجسم بأكمله.
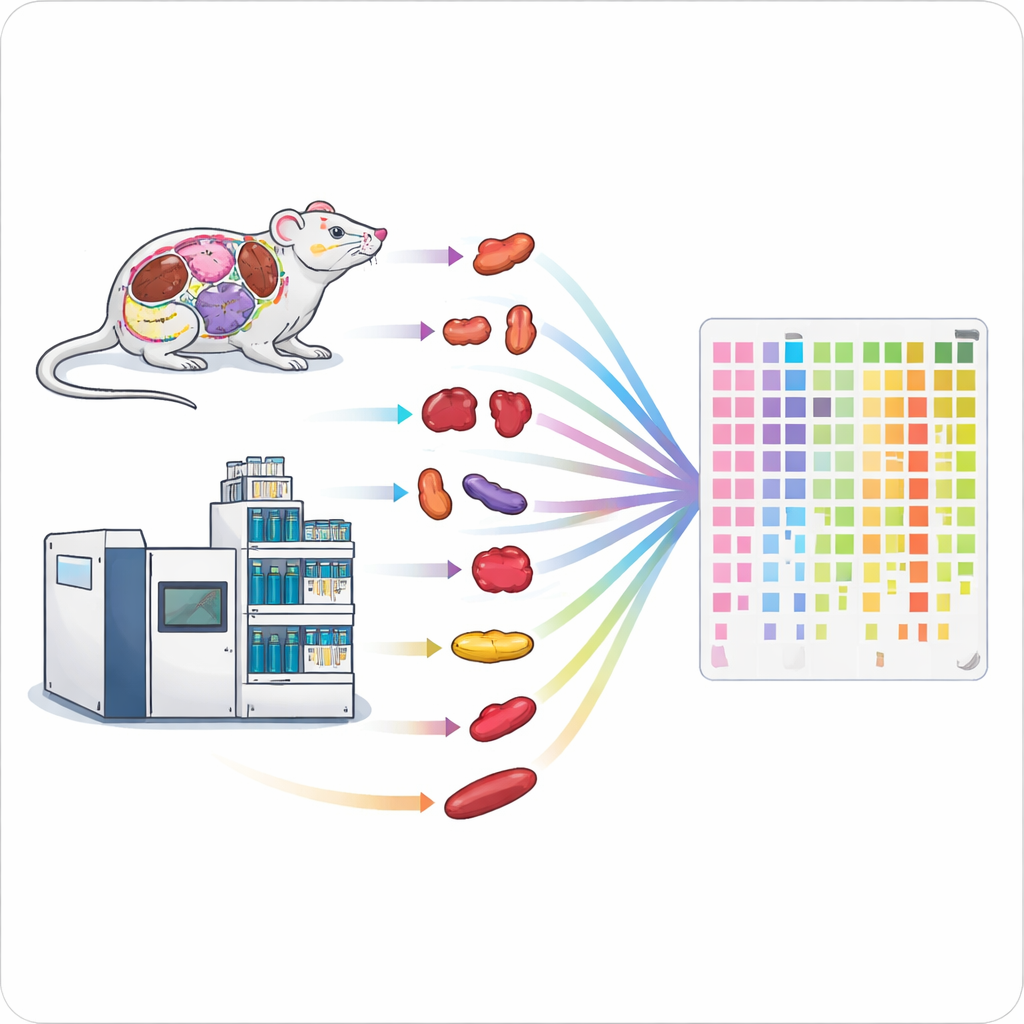
تسريع خط تجميع البروتين
الطرق التقليدية لقياس البروتينات بطيئة وتتطلب جهداً يدويًا كبيرًا، مما يصعّب دراسة الكائن الحي بأكمله أو مجموعات كبيرة من المرضى. جمع المؤلفون بين تقنيتين عاليتي الأداء — نوع سريع من مطيافية الكتلة وتشغيلات مطيافة سائلة قصيرة — ضمن سير عمل واحد مبسّط. من خلال ضبط إعدادات بعناية مثل زمن جمع الأيونات ونطاقات الكتلة الممسوحة، وصلوا إلى تغطية بروتينية عميقة في دقيقة إلى دقيقتين من القياس لكل عينة. أتاح إعدادهم المُحسّن تحديد نحو 6,200 بروتين بشري في تشغيل مدته دقيقة واحدة وحوالي 7,500 في دقيقتين، متفوقًا بكثير على طرق الإنتاجية العالية السابقة.
من النسيج إلى البيانات في يوم واحد
جمع البيانات بسرعة ليس سوى نصف المعركة؛ تحضير العينات قد يكون عنق زجاجة أكبر. لمعالجة ذلك، صمّم الفريق خط معالجة عينات متوازي للأنسجة الصلبة. استخدموا مفككات أنسجة آلية تعتمد على حبيبات لكسر ما يصل إلى 24 قطعة نسيج في الوقت نفسه، تلاها هضم البروتينات إلى ببتيدات بمساعدة الموجات فوق الصوتية في صفائح 96‑بئر وتنقية سريعة باستخدام أطراف متخصصة لإزالة الأملاح. سمح هذا الخط عالي الإنتاجية بمعالجة 96 نسيجًا في حوالي خمس ساعات، مقارنةً بعدة أيام باستخدام سير العمل القياسي. أظهرت الاختبارات في أدمغة الكائنات، والكلى، والرئتين أن الطريقة السريعة استرجعت أعدادًا مشابهة من البروتينات وأنتجت نتائج كمية متقاربة للغاية، لكن بمعدل إنتاجية أعلى بأكثر من سبع مرات.
مراقبة تأثير دواء السرطان في أنحاء الجسم
لإظهار ما يمكن أن يكشفه هذا النظام، توجّه الباحثون إلى إل‑أسباراجيناز، إنزيم علاجي يُستخدم في سرطان الدم عند الأطفال ويصعب إعادة توجيهه للبالغين بسبب الآثار الجانبية ومقاومة الدواء. عالجوا الفئران بإل‑أسباراجيناز القياسي، أو نسخة معدّلة مع نشاط منخفض على حمض أميني ذي صلة، أو بمحلول تحكّم، ثم جمعوا 13 عضوًا مختلفًا على مدار ثمانية أيام. إجمالًا، قاموا بقياس أكثر من 11,000 بروتين عبر 507 عينات. فرّق نمط البروتينات الأنسجة بوضوح مثل الدماغ والكبد وطبقات الدهون، وأظهر أن الدواء القياسي — وليس النسخة المعدّلة — أحدث تحولات كبيرة في مستويات البروتين عبر العديد من الأعضاء. أكدت قياسات الجزيئات الصغيرة في الدم والأنسجة أن الدواء القياسي استنزف حمض الأسباراجين بشكل قوي، بينما تسبب النسخة المعدّلة بتغيرات عابرة فقط، ما يساهم في تفسير سبب قلة فعاليتها.
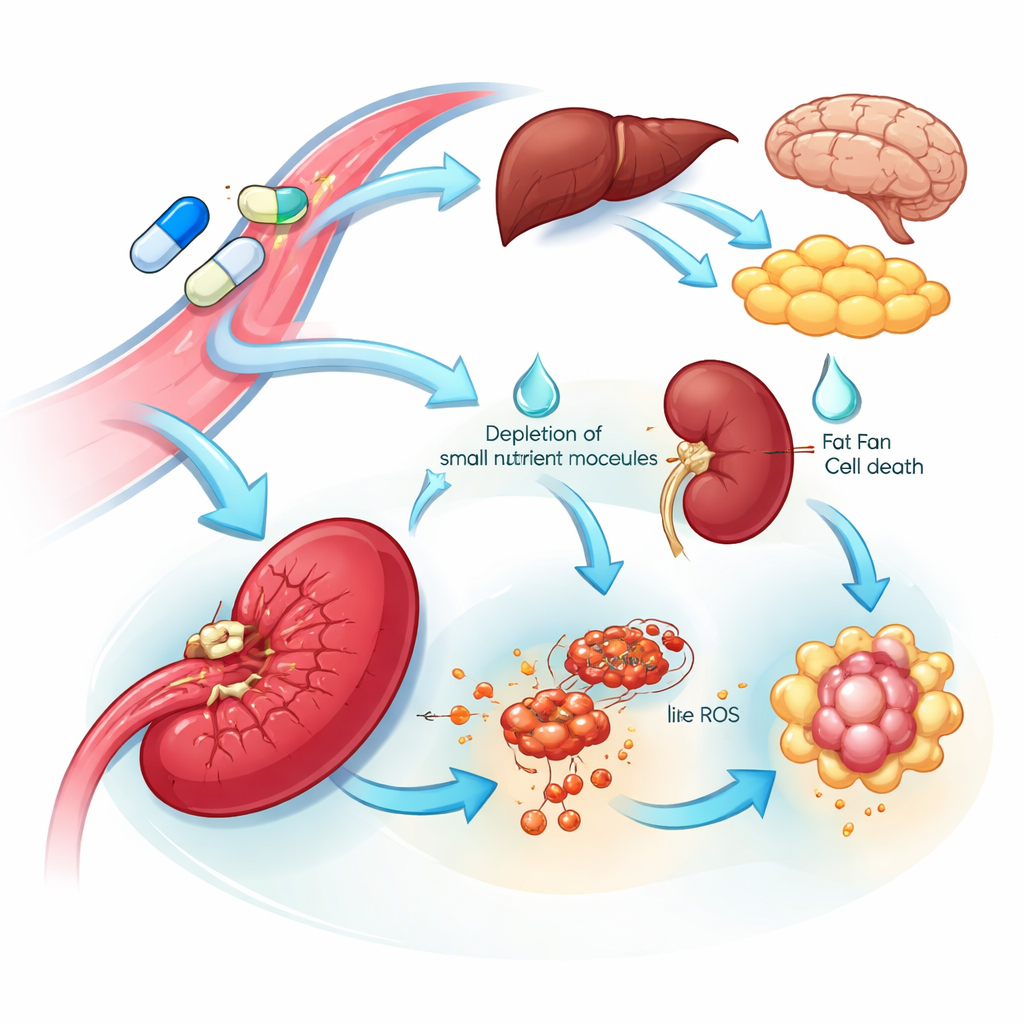
دلائل على هشاشة الأعضاء ومصادر السمّية
كشف المنظور متعدد الأعضاء عن كلٍ من الأهداف الضعيفة ومصادر محتملة للسمّية. استجابت العديد من الأنسجة لإل‑أسباراجيناز بزيادة الإنزيم الذي يصنّع الأسباراجين، مما يشير إلى برنامج مقاومة داخلي يساعد على استعادة هذا المغذّي. بالمقابل، أظهر الطحال انهيارًا لافتًا في هذا الإنزيم وانخفاضًا في الأحماض الأمينية ذات الصلة ولبنات بناء الـDNA، إلى جانب إشارات تتوافق مع موت خلوي مدفوع بالحديد. تشير هذه التغيرات إلى أن خلايا مرتبطة بالطحال قد تكون حساسة بشكل خاص للدواء. في غالبية الأعضاء تقريبًا، قام الدواء القياسي — وليس المعدّل — بكبح البروتينات المشاركة في تنظيم تجلّط الدم والتعامل مع الكوليسترول. هذا الانخفاض الواسع والمنسق يعكس مشاكل سريرية معروفة للدواء، بما في ذلك اضطرابات التخثر وارتفاع ثلاثي الغليسريدات في الدم، ويوجه إلى بروتينات دموية محددة قد تُراقب أو تُستهدف لتقليل هذه المخاطر.
ماذا يعني هذا للعلاجات المستقبلية
بدمج خط قياس بروتينات سريع وقابل للتوسع مع دراسة دوائية شاملة للجسم، أنشأ المؤلفون نوعًا من الأطلس الجزيئي لإل‑أسباراجيناز: أين يعمل، كيف تتكيف الأعضاء أو تفشل في التكيف، وأي المسارات تربط فوائده بأضراره. للقراء غير المتخصصين، الرسالة الأساسية هي أنه أصبح بالإمكان الآن مسح آلاف البروتينات عبر أعضاء متعددة في يوم واحد فقط، وتحويل تأثيرات الدواء المعقدة إلى خرائط مفصلة وقابلة للاختبار. يمكن أن تسرّع مثل هذه سير العمل تصميم علاجات سرطانية أكثر أمانًا، وتوجّه قرارات الجرعة والجدول الزمني، وتساعد في تحديد علاجات مركبة تحفظ الفعالية المضادة للسرطان مع تقليل الآثار الجانبية الخطيرة.
الاستشهاد: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
الكلمات المفتاحية: بروتيوميكس, سمية الدواء, علاج السرطان, مطيافية الكتلة, علم الأنظمة البيولوجية