Clear Sky Science · he
זרימת עבודה פרוטאומיקה רב-אורגנית בקצב גבוה לניתוח יעילות ורעילות של תרופות
מדוע מיפויים חלבוניים מהירים חשובים לרפואה
גופינו מורכב מאלפי חלבונים שונים שמשתנים בתגובה למחלות ולתרופות. קריאה של השינויים האלה במספר איברים במקביל היא המפתח להבנת מדוע טיפול עובד, מתי הוא נכשל ומה תופעות הלוואי שהוא עשוי לגרום. המחקר הזה מציג שיטה מהירה למדידת חלבונים במאות דגימות רקמה ביום ומיישם אותה על תרופת סרטן בשם L-אספרגנאז, חושף כיצד התרופה משנה את הביולוגיה ברחבי הגוף.
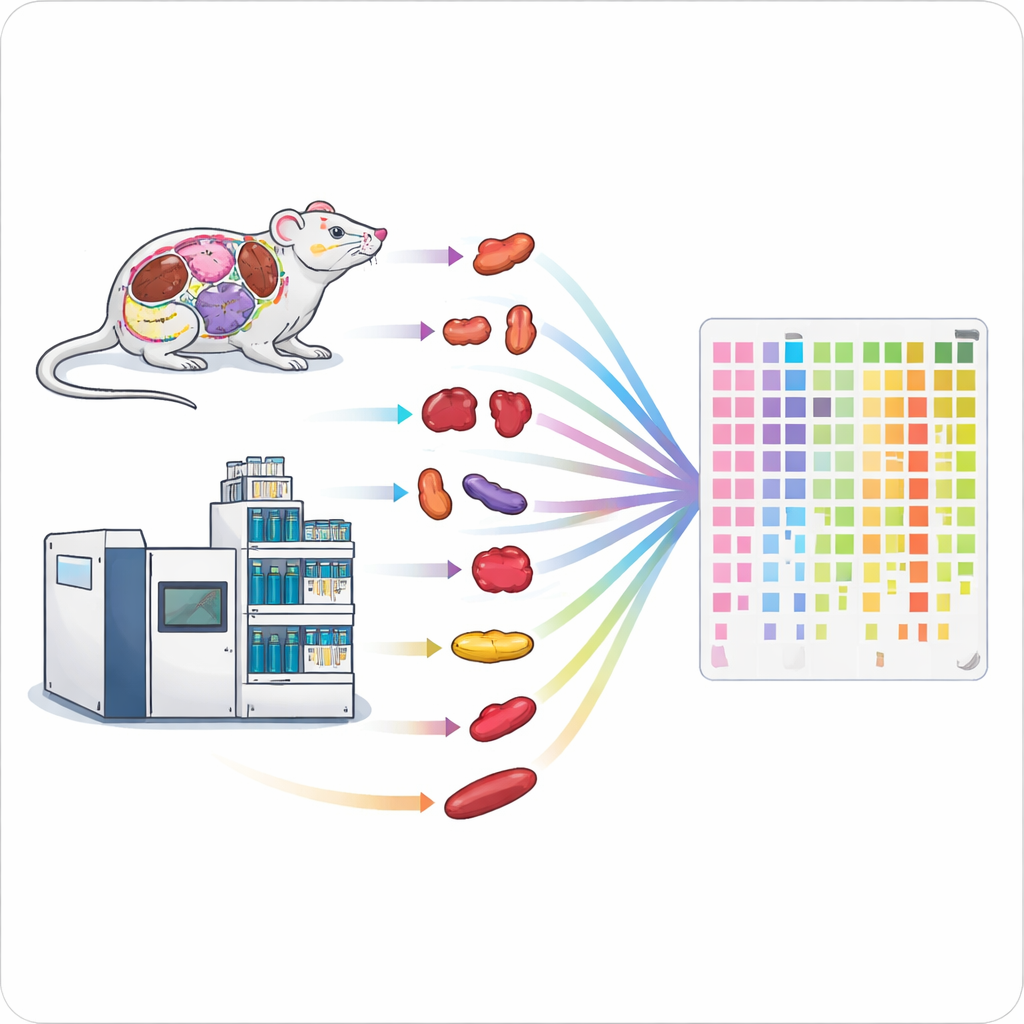
מהירות בקו הייצור החלבוני
שיטות מסורתיות למדידת חלבונים איטיות ודורשות עבודה רבה, מה שמקשה על חקר אורגניזמים שלמים או קבוצות מטופלים גדולות. המחברים שילבו שתי טכנולוגיות ביצועים גבוהים — סוג מהיר של ספקטרומטריה מסה וריצויי כרומטוגרפיה נוזלית קצרים — לזרימת עבודה אחת מלוטשת. על‑ידי כיוונון מדוקדק של פרמטרים כמו משך איסוף היונים וטווחי המסה הנסרקים, הם השיגו כיסוי חלבוני עמוק בתוך דקה עד שתי דקות מדידה לאפשרות. ההגדרה הממוטבת שלהם זיהתה כ-6,200 חלבוני אדם בריצה של דקה אחת וכ-7,500 בשתי דקות, הרבה מעל לשיטות מהירות קודמות.
מרקמה אל נתונים באותו יום
איסוף הנתונים במהירות הוא רק חצי מהמאבק; הכנת הדגימות יכולה להיות צוואר בקבוק גדול אף יותר. כדי להתמודד עם זה, הצוות תכנן קו טיפול בדגימות מקביל לרקמות מוצקות. הם השתמשו במערכות הומוגניזציה מבוססות חרוזים אוטומטיות כדי לפרק עד 24 חתיכות רקמה בו‑זמנית, ואחריה עיכול חלבונים בעזרת אולטרסאונד לפפטידים בצלחות 96 בארים וניקוי מהיר באמצעות טיפים מיוחדים. צינור ייצור בקצב גבוה זה איפשר עיבוד של 96 רקמות בכחמש שעות, לעומת כמה ימים בעבודה שגרתית. בדיקות במוח עכבר, כליה וריאה הראו שהשיטה המהירה שחזרה מספר דומה של חלבונים וסיפקה תוצאות כמותיות תואמות מאוד, אך עם תפוקה הגבוהה ביותר ביותר משבעה מקומות.
צפייה בפעולת תרופת סרטן ברחבי הגוף
כדי להדגים מה הפלטפורמה יכולה לחשוף, החוקרים פנו ל‑L‑אספרגנאז, תרופה אנזימטית המשמשת ללוקמיה בילדים שקשה להפנות למבוגרים בגלל תופעות לוואי והתפתחות עמידות. הם טיפלו בעכברים ב‑L‑אספרגנאז סטנדרטי, בגרסה משוננת עם פעילות מופחתת על חומצת אמינו קשורה, או בתמיסת בקרה, ולאחר מכן אספו 13 איברים שונים לאורך קורס של שמונה ימים. בסך הכול הם כינו יותר מ‑11,000 חלבונים ב‑507 דגימות. דפוסים בנתוני החלבון הפרידו בצורה ברורה רקמות כגון מוח, כבד ומאגרי שומן והראו שהתרופה הסטנדרטית, אך לא הגרסה המוטנטית, גרמה לשינויים גדולים ברמות חלבון בעשרות איברים. מדידות של מולקולות קטנות בדם וברקמות אישרו שהתרופה הסטנדרטית שידדה בחוזקה את חומצת האמינו אספרגין, בעוד שהמוטנטית גרמה לשינויים קצרים בלבד, מה שעוזר להסביר מדוע היא פחות יעילה.
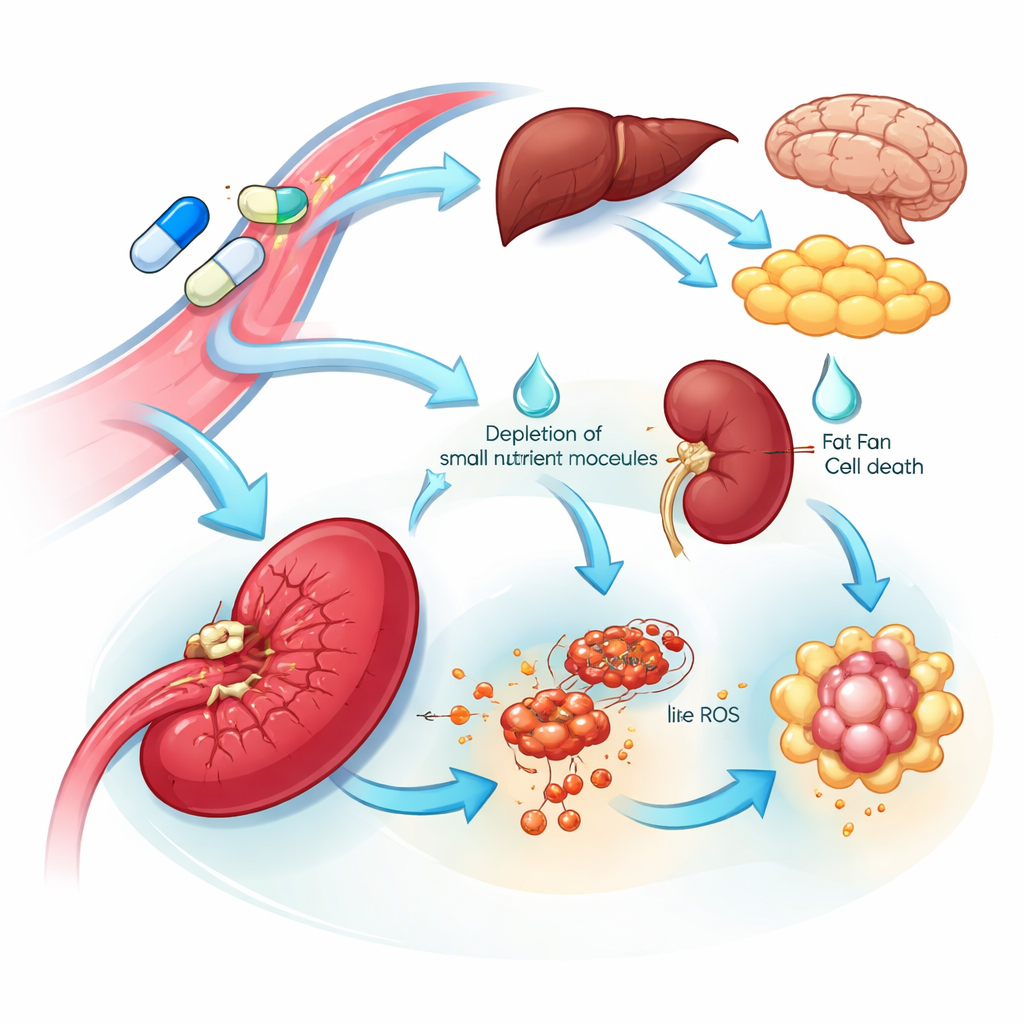
רמזים לפגיעות איבר ותופעות לוואי
המבט הרב‑אורגני חשף גם מטרות פגיעות וגם מקורות פוטנציאליים לרעילות. רקמות רבות הגיבו ל‑L‑אספרגנאז בהגברה של האנזים שמייצר אספרגין, מעידה על תוכנית עמידות פנימית שעוזרת לשקם את המזון הזה. לעומת זאת, הטחול הראה קריסה בולטת באנזים זה וירידה בחומצות אמינו קשורות ובאבני בניין ל‑DNA, יחד עם אותות התואמות למוות תאי מונע על‑ידי ברזל. שינויים אלה מצביעים על כך שתרכיבים הקשורים לטחול עשויים להיות רגישים במיוחד לתרופה. כמעט בכל האיברים, התרופה הסטנדרטית — ולא המוטנטית — השתקה חלבונים מעורבים בוויסות קרישת הדם ובטיפול בכולסטרול. השחיקה הרחבה והמתואמת הזו משקפת בעיות קליניות ידועות הקשורות לתרופה, כולל הפרעות קרישה וטריגליצרידים גבוהים בדם, ומצביעה על חלבוני דם ספציפיים שניתן לנטר או ליעד כדי להפחית סיכונים אלה.
מה משמעות הדבר לטיפולים עתידיים
על‑ידי שילוב צינור מדידה חלבוני מהיר וניתן להרחבה עם מחקר תרופתי על גוף שלם, המחברים יצרו מעין אטלס מולקולרי ל‑L‑אספרגנאז: היכן הוא פועל, כיצד איברים מסתגלים או נכשלם להסתגל, ואילו מסלולים מקשרים בין תועלתו לנזקיו. לקהל שאינו מומחה, המסר המרכזי הוא שעכשיו ניתן לסרוק אלפי חלבונים ברחבי איברים רבים בתוך יום אחד, ולהפוך השפעות תרופתיות מורכבות למפות מפורטות הניתנות לבדיקה. זרימות עבודה כאלה עשויות להאיץ את עיצוב טיפולים בטוחים יותר לסרטן, לכוון החלטות על מינון ולוחות זמנים, ולעזור לזהות טיפולים משולבים שישמרו על עוצמת האנטי‑סרטן תוך הפחתת תופעות לוואי מסוכנות.
ציטוט: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
מילות מפתח: פרוטאומיקה, רעילות של תרופות, טיפולים בסרטן, מסה ספקטרומטריה, ביולוגיה מערכתית