Clear Sky Science · it
Workflow proteomico multi-organo ad alto rendimento per l’analisi dell’efficacia e della tossicità dei farmaci
Perché mappe proteiche più veloci sono importanti per la medicina
I nostri corpi sono costituiti da migliaia di proteine diverse che cambiano in risposta a malattie e farmaci. Leggere questi cambiamenti attraverso molti organi contemporaneamente è fondamentale per capire perché un trattamento funziona, quando fallisce e quali effetti collaterali può causare. Questo studio presenta un metodo rapido per misurare le proteine in centinaia di campioni di tessuto al giorno e lo applica a un farmaco antitumorale chiamato L‑asparaginasi, rivelando come il farmaco rimodella la biologia in tutto il corpo.
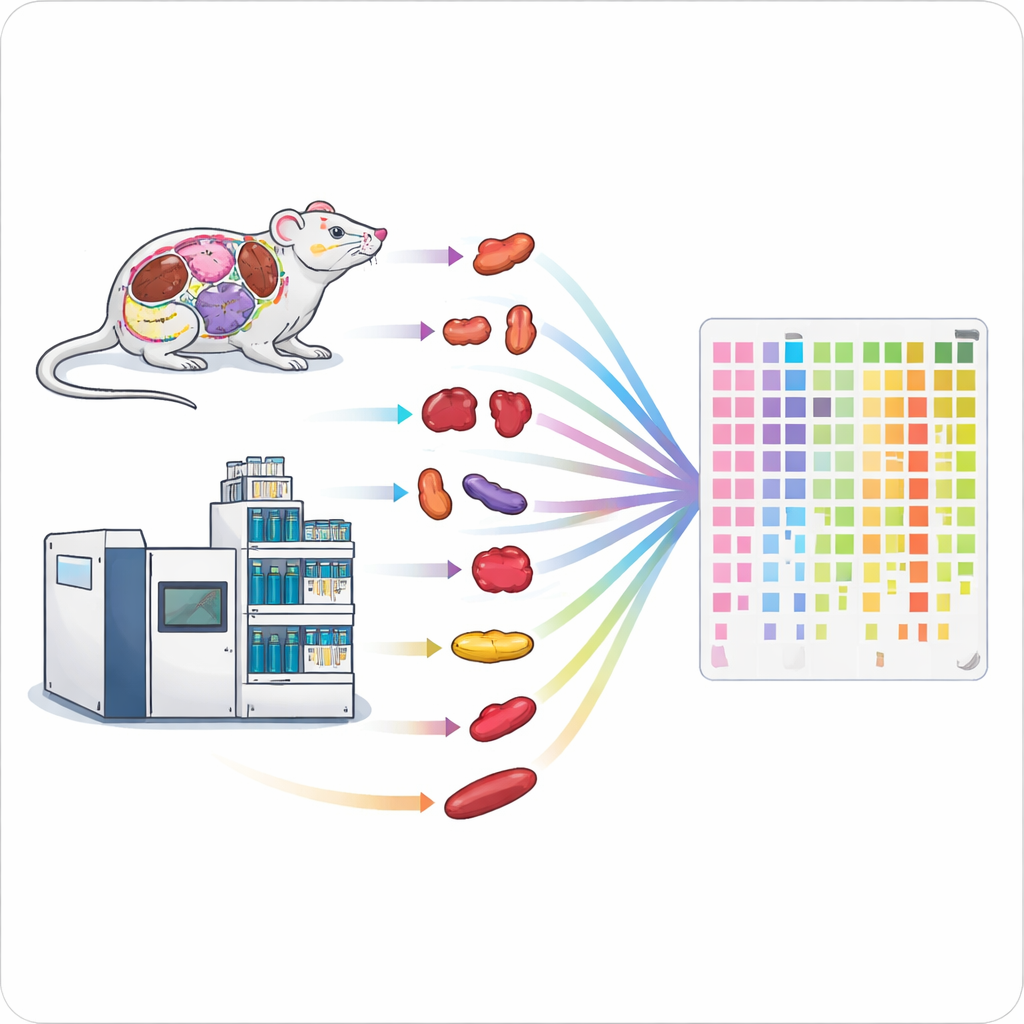
Accelerare la linea di produzione delle proteine
I metodi tradizionali per misurare le proteine sono lenti e richiedono molto lavoro, rendendo difficile studiare organismi interi o ampi gruppi di pazienti. Gli autori hanno combinato due tecnologie ad alte prestazioni — un tipo veloce di spettrometria di massa e corse di cromatografia liquida molto brevi — in un unico flusso di lavoro snello. Regolando con cura parametri come il tempo di accumulo degli ioni e gli intervalli di massa analizzati, hanno ottenuto una copertura proteica profonda con appena uno‑due minuti di misurazione per campione. Il loro assetto ottimizzato ha potuto identificare circa 6.200 proteine umane in una corsa di un minuto e circa 7.500 in due minuti, superando di gran lunga i precedenti metodi ad alto rendimento.
Dal tessuto ai dati in una sola giornata
Raccogliere i dati rapidamente è solo metà della battaglia; preparare i campioni può rappresentare un collo di bottiglia ancora maggiore. Per risolvere questo problema il team ha progettato una pipeline parallela per la gestione dei campioni solidi. Hanno utilizzato omogeneizzatori automatizzati a sfere per rompere fino a 24 pezzi di tessuto contemporaneamente, seguiti da una digestione assistita a ultrasuoni delle proteine in peptidi in piastre a 96 pozzetti e da una desalinizzazione rapida con puntali specializzati. Questa pipeline ad alto rendimento ha consentito di processare 96 tessuti in circa cinque ore, rispetto ai diversi giorni richiesti da un workflow standard. Test su cervello, rene e polmone di topo hanno mostrato che il metodo rapido recupera un numero di proteine simile e produce risultati quantitativi altamente confrontabili, ma con una produttività oltre sette volte superiore.
Osservare l’azione di un farmaco antitumorale in tutto il corpo
Per dimostrare cosa può rivelare questa piattaforma, i ricercatori si sono concentrati sulla L‑asparaginasi, un enzima terapeutico usato per la leucemia infantile che è difficile da riutilizzare per gli adulti a causa di effetti collaterali e resistenza farmacologica. Hanno trattato topi con L‑asparaginasi standard, una versione modificata con attività ridotta su un amminoacido correlato, o con una soluzione di controllo, quindi hanno raccolto 13 diversi organi nel corso di otto giorni. Nel complesso hanno quantificato più di 11.000 proteine su 507 campioni. Gli schemi nei dati proteici hanno distinto nettamente tessuti come cervello, fegato e depositi adiposi e hanno mostrato che il farmaco standard, ma non la versione mutante, ha innescato ampi spostamenti nei livelli proteici in molti organi. Misurazioni di piccole molecole nel sangue e nei tessuti hanno confermato che il farmaco standard depleta fortemente l’amminoacido asparagina, mentre il mutante provoca solo cambiamenti temporanei, spiegando in parte la sua minore efficacia.
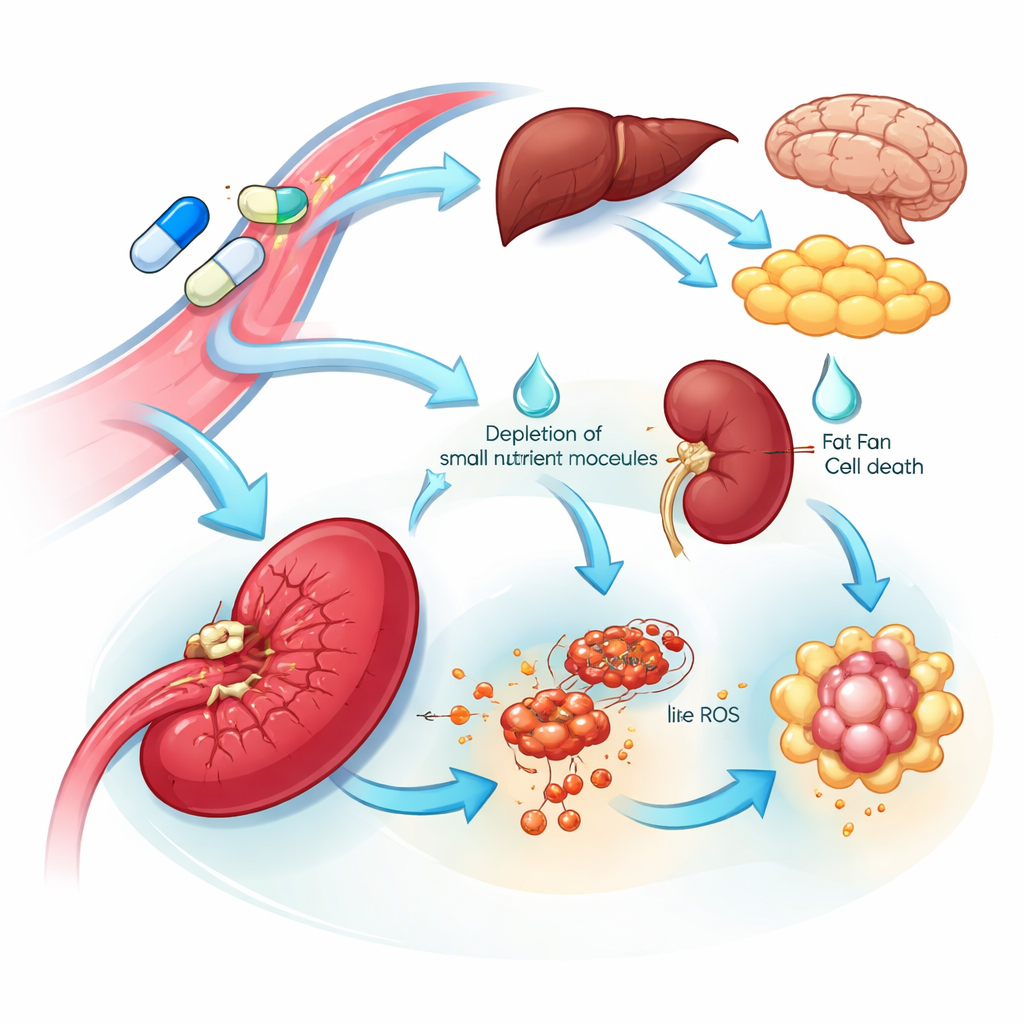
Indizi sulla vulnerabilità degli organi e sugli effetti collaterali
La visione multi‑organo ha scoperto sia bersagli vulnerabili sia potenziali fonti di tossicità. Molti tessuti hanno risposto alla L‑asparaginasi aumentando l’enzima che sintetizza l’asparagina, suggerendo un programma di resistenza intrinseco che aiuta a ristabilire questo nutriente. Al contrario, la milza ha mostrato un notevole crollo di questo enzima e una diminuzione degli amminoacidi correlati e dei precursori del DNA, insieme a segnali coerenti con una morte cellulare mediata dal ferro. Questi cambiamenti suggeriscono che le cellule legate alla milza potrebbero essere particolarmente sensibili al farmaco. In quasi tutti gli organi, il farmaco standard — ma non il mutante — ha soppresso proteine coinvolte nella regolazione della coagulazione e del metabolismo del colesterolo. Questo calo ampio e coordinato rispecchia problemi clinici noti associati al farmaco, inclusi disturbi della coagulazione e trigliceridi elevati, e indica specifiche proteine ematiche che potrebbero essere monitorate o bersagliate per ridurre questi rischi.
Cosa significa per i trattamenti futuri
Accoppiando una pipeline rapida e scalabile per la misurazione delle proteine con uno studio farmacologico sull’intero organismo, gli autori hanno creato una sorta di atlante molecolare della L‑asparaginasi: dove agisce, come gli organi si adattano o non riescono ad adattarsi, e quali vie collegano i suoi benefici ai danni. Per i non specialisti, il messaggio chiave è che ora è possibile analizzare migliaia di proteine attraverso molti organi in un solo giorno, trasformando effetti farmacologici complessi in mappe dettagliate e verificabili. Tali workflow potrebbero accelerare la progettazione di terapie antitumorali più sicure, guidare decisioni su dosi e schemi di somministrazione e aiutare a identificare trattamenti combinati che preservino l’efficacia anticancro riducendo gli effetti collaterali pericolosi.
Citazione: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
Parole chiave: proteomica, tossicità dei farmaci, terapia del cancro, spettrometria di massa, biologia dei sistemi