Clear Sky Science · es
Flujo de trabajo proteómico multiórgano de alto rendimiento para el análisis de eficacia y toxicidad de fármacos
Por qué importan los mapas de proteínas más rápidos para la medicina
Nuestros cuerpos están formados por miles de proteínas distintas que cambian en respuesta a enfermedades y medicamentos. Leer esos cambios en muchos órganos a la vez es clave para entender por qué un tratamiento funciona, cuándo falla y qué efectos secundarios puede causar. Este estudio presenta una forma rápida de medir proteínas en cientos de muestras de tejido por día y la aplica a un fármaco contra el cáncer llamado L‑asparaginasa, revelando cómo el fármaco reconfigura la biología en todo el cuerpo.
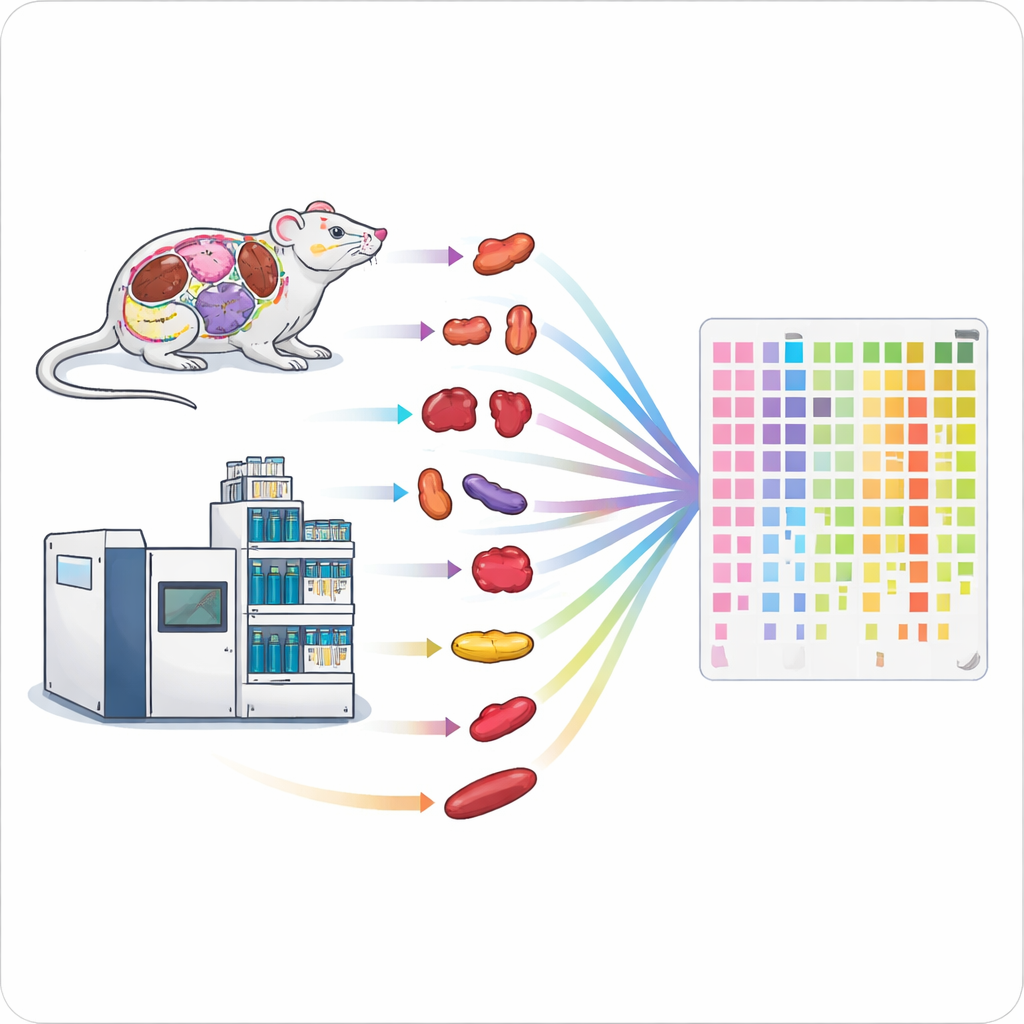
Acelerando la línea de ensamblaje de proteínas
Los métodos tradicionales para medir proteínas son lentos y laboriosos, lo que dificulta estudiar organismos enteros o grandes cohortes de pacientes. Los autores combinaron dos tecnologías de alto rendimiento —un tipo rápido de espectrometría de masas y corridas cortas de cromatografía líquida— en un flujo de trabajo unificado y optimizado. Ajustando con cuidado parámetros como el tiempo de acumulación de iones y los rangos de masa escaneados, lograron una cobertura profunda de proteínas en apenas uno o dos minutos de medición por muestra. Su configuración optimizada pudo identificar aproximadamente 6.200 proteínas humanas en una corrida de un minuto y alrededor de 7.500 en dos minutos, superando con creces los métodos previos de alto rendimiento.
Del tejido a los datos en un solo día
Recoger datos rápidamente es solo la mitad de la batalla; la preparación de las muestras puede ser un cuello de botella aún mayor. Para resolverlo, el equipo diseñó una línea paralela de procesamiento de muestras para tejidos sólidos. Usaron homogeneizadores automatizados con perlas para lisar hasta 24 piezas de tejido a la vez, seguidos de digestión asistida por ultrasonidos de las proteínas en péptidos en placas de 96 pocillos y desalinización rápida con puntas especializadas. Este flujo de trabajo de alto rendimiento permitió procesar 96 tejidos en unas cinco horas, frente a varios días con un protocolo estándar. Ensayos en cerebro, riñón y pulmón de ratón mostraron que el método rápido recuperaba números de proteínas similares y producía resultados cuantitativos altamente comparables, pero con más de siete veces mayor rendimiento.
Viendo cómo actúa un fármaco contra el cáncer en todo el cuerpo
Para demostrar lo que esta plataforma puede revelar, los investigadores estudiaron la L‑asparaginasa, una enzima fármaco usada en leucemia infantil que es difícil de reutilizar en adultos por efectos secundarios y resistencia. Trataron ratones con L‑asparaginasa estándar, con una versión modificada con actividad reducida sobre un aminoácido relacionado, o con una solución control, y luego recogieron 13 órganos diferentes a lo largo de un curso de ocho días. En total, cuantificaron más de 11.000 proteínas en 507 muestras. Los patrones en los datos proteómicos separaron claramente tejidos como cerebro, hígado y depósitos de grasa y mostraron que el fármaco estándar, pero no la variante mutante, provocó grandes cambios en los niveles de proteínas en muchos órganos. Mediciones de pequeñas moléculas en sangre y tejidos confirmaron que el fármaco estándar agotó fuertemente el aminoácido asparagina, mientras que la versión mutante causó solo cambios breves, lo que ayuda a explicar por qué es menos eficaz.
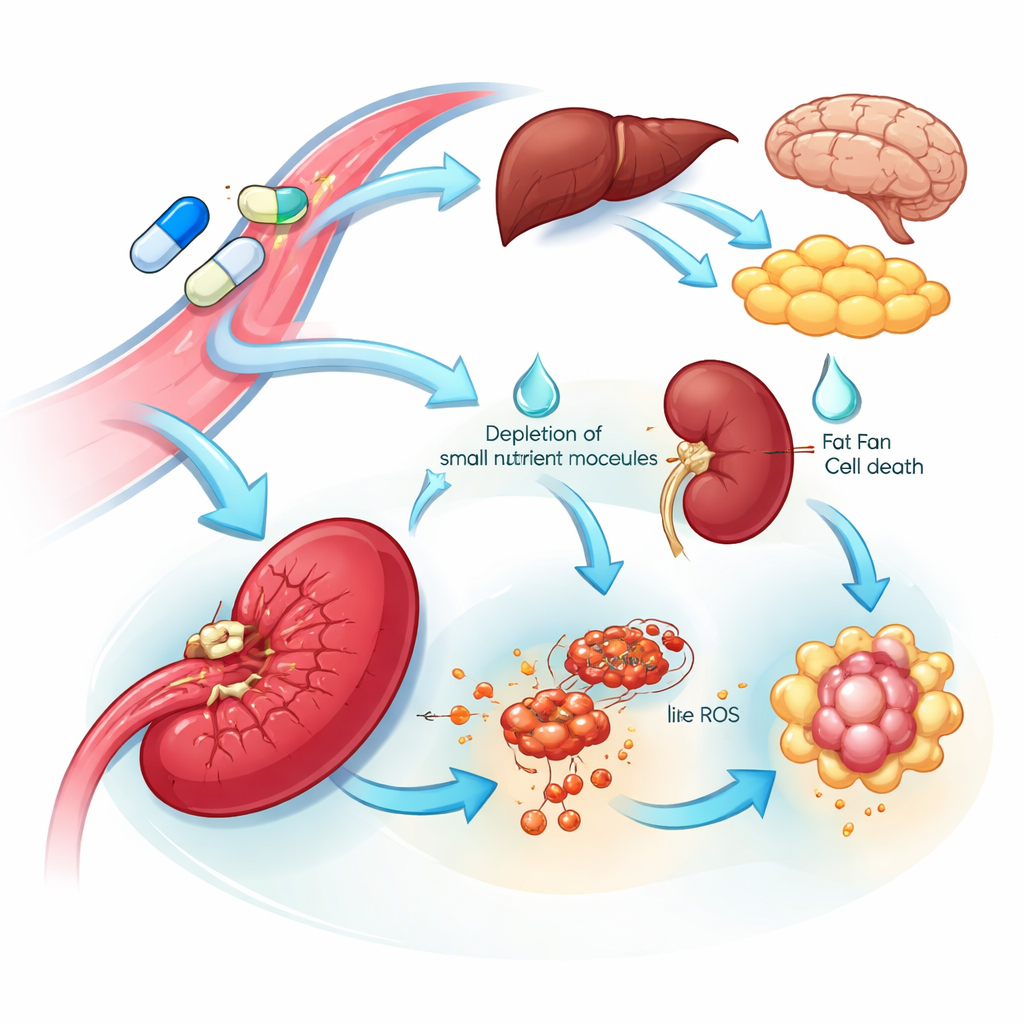
Pistas sobre vulnerabilidad de órganos y efectos secundarios
La visión multiórgano descubrió tanto objetivos vulnerables como posibles fuentes de toxicidad. Muchos tejidos respondieron a la L‑asparaginasa aumentando la enzima que sintetiza asparagina, lo que sugiere un programa de resistencia intrínseco que ayuda a restaurar este nutriente. En contraste, el bazo mostró un colapso llamativo de esta enzima y una caída en aminoácidos relacionados y componentes para la síntesis de ADN, junto con señales coherentes con muerte celular inducida por hierro. Estos cambios sugieren que las células relacionadas con el bazo pueden ser particularmente sensibles al fármaco. En casi todos los órganos, el fármaco estándar —pero no el mutante— suprimió proteínas implicadas en la regulación de la coagulación sanguínea y el manejo del colesterol. Este descenso amplio y coordinado refleja problemas clínicos conocidos del fármaco, incluidos trastornos de coagulación y triglicéridos sanguíneos elevados, y apunta a proteínas específicas en la sangre que podrían monitorearse o dirigirse para reducir estos riesgos.
Qué significa esto para tratamientos futuros
Al emparejar una tubería rápida y escalable de medición de proteínas con un estudio del fármaco a escala corporal, los autores crearon una especie de atlas molecular de la L‑asparaginasa: dónde actúa, cómo los órganos se adaptan o no se adaptan, y qué vías vinculan sus beneficios con sus daños. Para el público no especializado, el mensaje clave es que ahora es posible escanear miles de proteínas en muchos órganos en solo un día, convirtiendo efectos complejos de fármacos en mapas detallados y comprobables. Tales flujos de trabajo podrían acelerar el diseño de terapias oncológicas más seguras, guiar decisiones de dosis y calendario, y ayudar a identificar tratamientos combinados que mantengan el poder antitumoral mientras atenúan efectos secundarios peligrosos.
Cita: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
Palabras clave: proteómica, toxicidad de fármacos, terapia contra el cáncer, espectrometría de masas, biología de sistemas