Clear Sky Science · pl
Szybki wielonarządowy przepływ pracy proteomiki do analizy skuteczności i toksyczności leków
Dlaczego szybsze mapy białkowe mają znaczenie dla medycyny
Nasze ciało składa się z tysięcy różnych białek, które zmieniają się w odpowiedzi na choroby i leki. Odczytywanie tych zmian równocześnie w wielu narządach jest kluczowe, by zrozumieć, dlaczego terapia działa, kiedy zawodzi i jakie może powodować skutki uboczne. W tym badaniu wprowadzono szybki sposób pomiaru białek w setkach próbek tkanek dziennie i zastosowano go do leku przeciwnowotworowego o nazwie L‑asparaginaza, ujawniając, jak lek przekształca biologię w całym organizmie.
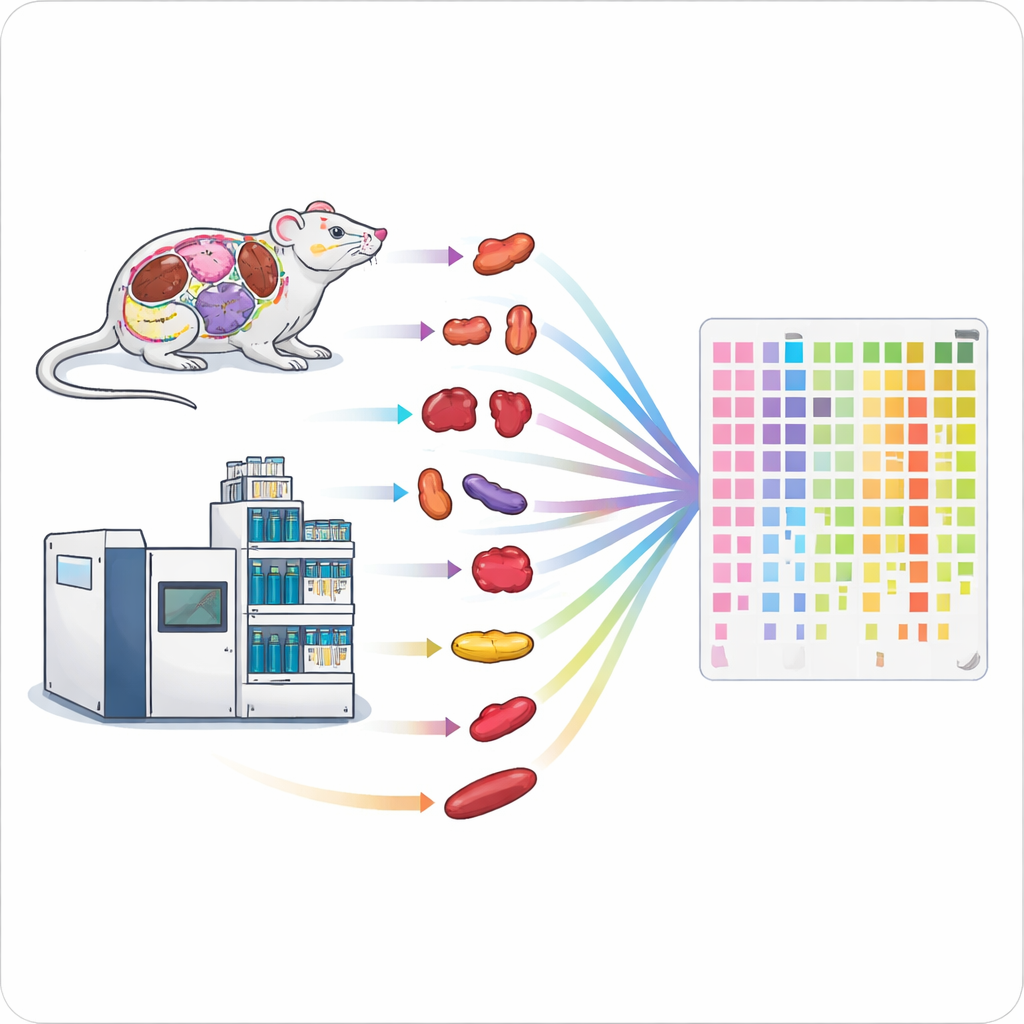
Przyspieszanie linii montażowej białek
Tradycyjne metody pomiaru białek są wolne i pracochłonne, co utrudnia badanie całych organizmów lub dużych grup pacjentów. Autorzy połączyli dwie wydajne technologie — szybki typ spektrometrii mas oraz krótkie rozdziały chromatograficzne — w jeden usprawniony przepływ pracy. Poprzez staranne dostrojenie ustawień, takich jak czas zbierania jonów czy zakresy mas skanowane, osiągnęli dogłębne pokrycie białkowe przy zaledwie jednej do dwóch minut pomiaru na próbkę. Ich zoptymalizowane ustawienie mogło zidentyfikować około 6 200 białek ludzkich w jednominutowym przebiegu i około 7 500 w dwóch minutach, przewyższając wcześniejsze metody wysokoprzepustowe.
Z tkanki do danych w jeden dzień
Szybkie zbieranie danych to tylko połowa problemu; przygotowanie próbek może stanowić jeszcze większe wąskie gardło. Aby to rozwiązać, zespół zaprojektował równoległą linię obsługi próbek dla tkanek stałych. Użyli zautomatyzowanych homogenizatorów na kulki do rozbijania nawet 24 kawałków tkanki jednocześnie, a następnie trawienia białek ultradźwiękami do peptydów w płytach 96-dołkowych oraz szybkiego odsalania za pomocą wyspecjalizowanych końcówek. Ten wysokoprzepustowy proces pozwolił przetworzyć 96 tkanek w około pięć godzin, w porównaniu z kilkoma dniami w standardowym przepływie. Testy na mózgu, nerkach i płucach myszy wykazały, że szybka metoda odzyskiwała podobną liczbę białek i dawała wysoce porównywalne wyniki ilościowe, lecz przy ponad siedmiokrotnie wyższej przepustowości.
Obserwowanie działania leku przeciwnowotworowego w całym ciele
Aby zademonstrować, co ta platforma może ujawnić, badacze zwrócili się ku L‑asparaginazie, enzymatycznemu lekowi stosowanemu w białaczce dziecięcej, trudnemu do ponownego zastosowania u dorosłych z powodu skutków ubocznych i oporności. Leczyli myszy standardową L‑asparaginazą, zmodyfikowaną wersją o zmniejszonej aktywności wobec powiązanego aminokwasu lub roztworem kontrolnym, a następnie pobierali 13 różnych narządów w ciągu ośmiodniowego kursu. W sumie zmierzyli ponad 11 000 białek w 507 próbkach. Wzorce w danych białkowych jasno rozdzielały tkanki takie jak mózg, wątroba i depozyty tłuszczu oraz wykazały, że standardowy lek, w przeciwieństwie do formy mutantowej, wywołał duże zmiany poziomów białek w wielu narządach. Pomiary małych cząsteczek we krwi i tkankach potwierdziły, że standardowy lek silnie wyczerpywał aminokwas asparaginę, podczas gdy mutant powodował tylko krótkotrwałe zmiany, co pomaga wyjaśnić, dlaczego jest mniej skuteczny.
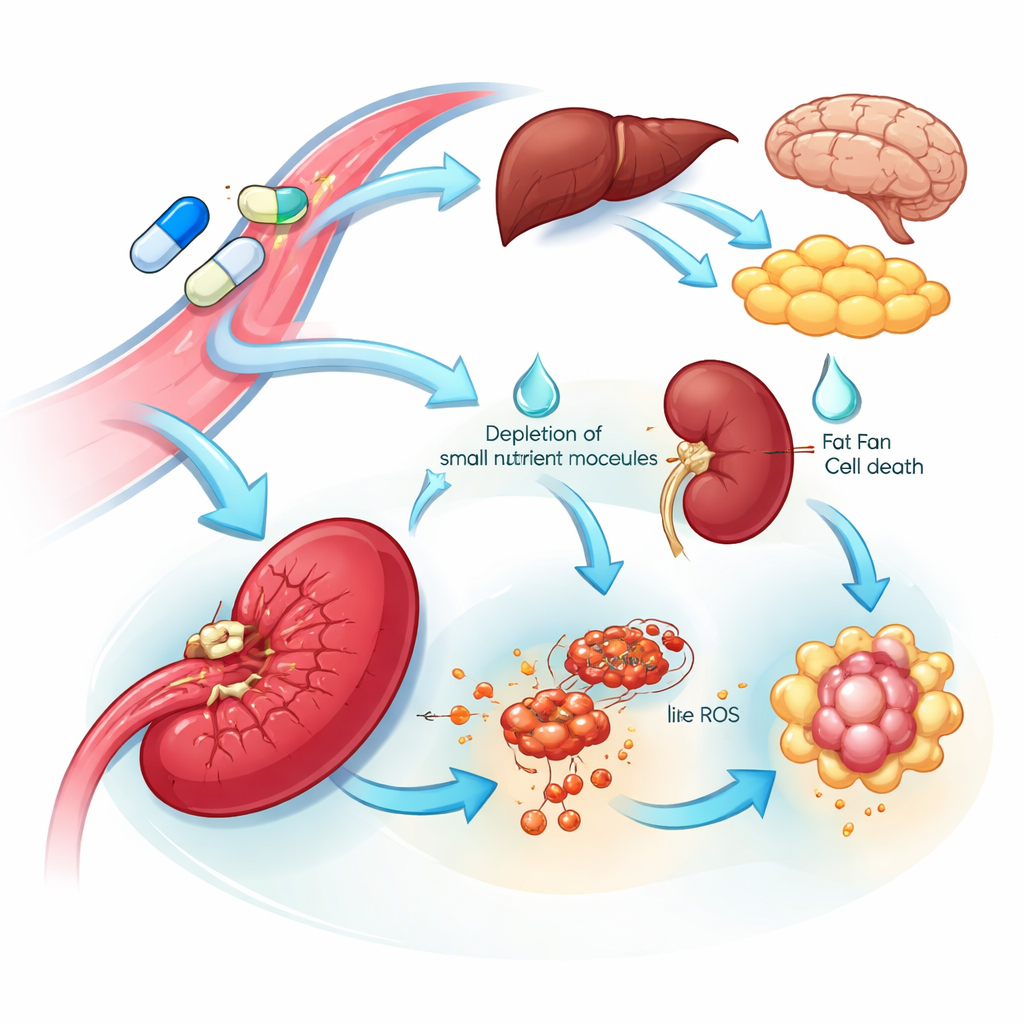
Wskazówki dotyczące wrażliwości narządów i skutków ubocznych
Wielonarządowy widok ujawnił zarówno podatne cele, jak i potencjalne źródła toksyczności. Wiele tkanek reagowało na L‑asparaginazę zwiększeniem enzymu wytwarzającego asparaginę, co sugeruje wbudowany program oporności pomagający przywrócić ten składnik odżywczy. W przeciwieństwie do tego śledziona wykazała uderzający spadek tego enzymu oraz obniżenie powiązanych aminokwasów i składników budulcowych DNA, wraz z sygnałami zgodnymi z żelazozależną śmiercią komórkową. Zmiany te sugerują, że komórki związane ze śledzioną mogą być szczególnie wrażliwe na lek. W prawie wszystkich narządach standardowy lek — ale nie mutant — tłumił białka zaangażowane w regulację krzepnięcia krwi i metabolizm cholesterolu. Ten szeroki, skoordynowany spadek odzwierciedla znane kliniczne problemy związane z lekiem, w tym zaburzenia krzepnięcia i podwyższone triglicerydy we krwi, oraz wskazuje konkretne białka krwi, które można monitorować lub na które można skierować interwencję, aby zmniejszyć te ryzyka.
Co to oznacza dla przyszłych terapii
Łącząc szybki, skalowalny pipeline pomiaru białek z badaniem leku obejmującym cały organizm, autorzy stworzyli rodzaj molekularnego atlasu L‑asparaginazy: gdzie działa, jak narządy adaptują się lub zawodzą w adaptacji oraz które szlaki łączą korzyści z jej szkodami. Dla osób niebędących specjalistami kluczowy przekaz jest taki, że teraz można przeskanować tysiące białek w wielu narządach w ciągu jednego dnia, zamieniając złożone efekty leku w szczegółowe, testowalne mapy. Takie przepływy pracy mogą przyspieszyć projektowanie bezpieczniejszych terapii przeciwnowotworowych, kierować decyzjami dotyczącymi dawek i harmonogramów oraz pomóc zidentyfikować terapie łączone, które zachowują siłę przeciwnowotworową przy jednoczesnym ograniczaniu niebezpiecznych skutków ubocznych.
Cytowanie: Xiong, Y., Tan, L., Chan, Wk. et al. High-throughput multi-organ proteomics workflow for drug efficacy and toxicity analysis. Nat Commun 17, 3505 (2026). https://doi.org/10.1038/s41467-026-69471-4
Słowa kluczowe: proteomika, toksyczność leków, terapia przeciwnowotworowa, spektrometria mas, biologia systemów