Clear Sky Science · zh
分裂酵母磷酸盐外排蛋白 SpXpr1 开关机制的结构学洞见
为何微小的磷酸门道至关重要
每个细胞都必须精确平衡磷酸盐,这是构成 DNA、膜以及细胞能量货币等分子的微小但不可或缺的成分。磷酸盐不足会阻碍生长;过多则可能有毒。本研究考察了分裂酵母(一个模式真菌)如何通过称为 SpXpr1 的分子通道将多余的磷酸盐排出细胞。通过揭示该通道的三维结构以及其开合方式,这项工作阐明了从真菌到人类等不同生物体如何利用相关蛋白维持磷酸盐平衡,对理解脑部疾病、肾脏健康、农业以及抗真菌策略具有重要启示。
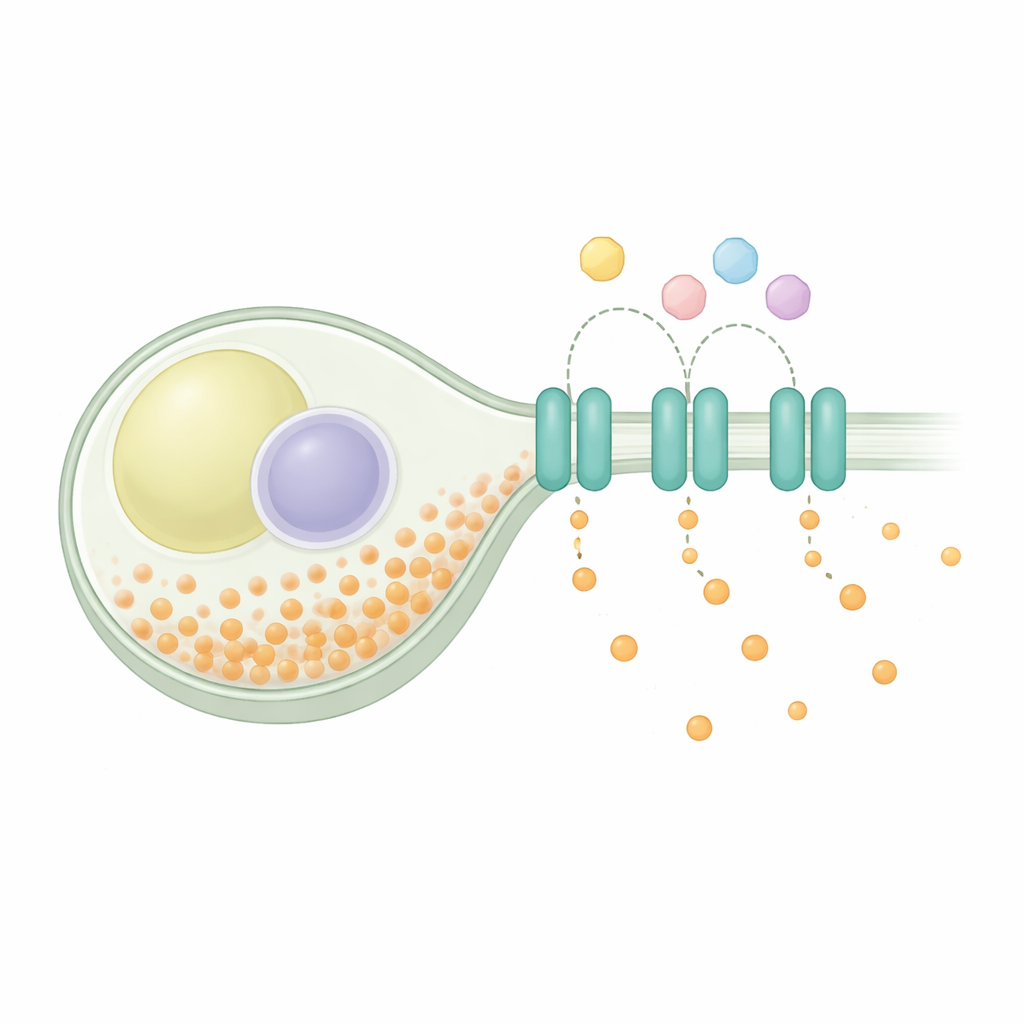
维持细胞内的平衡
磷酸盐稳态是一个普遍问题:细胞必须摄取磷酸盐以满足代谢和构建需要,安全储存一部分,并将多余部分排出。在分裂酵母中,匮乏时摄入系统会被激活,而在磷酸盐充足时被关闭,同时一种储存复合物会将多余磷酸以长链形式打包。遗传学研究曾表明,一种名为 SpXpr1 的蛋白充当专门的外排器,在储存通路受损时帮助防止有害的过载。SpXpr1 属于遍布真核生物(包括植物和人类)的 XPR1 外排蛋白家族,相关蛋白与脑部钙化和肾功能障碍等疾病有关。尽管存在家族背景,但之前尚不清楚酵母版本是否以与人类蛋白相同的方式工作。
观察蛋白并证明它是通道
研究者首先验证 SpXpr1 是否确实将磷酸盐跨膜转运。他们将酵母蛋白插入已去除自身 XPR1 的人类细胞中,然后测量有多少磷酸盐渗入周围溶液。携带 SpXpr1 的细胞比对照细胞排出更多磷酸盐,确认了其外排活性,尽管效率低于人类外排蛋白。通过电生理记录,团队进一步显示,表达 SpXpr1 的细胞在存在小型信号分子肌醇六磷酸(InsP6)时产生依赖磷酸的电流增加。这确立了 SpXpr1 为一真实的通道,允许磷酸离子通过,并可被含肌醇的信号分子调节。
沿着共同通路的两道门
为了解 SpXpr1 在原子层面的工作机制,作者利用冷冻电子显微镜解析了其在无 InsP6 与有 InsP6 条件下的结构。每个 SpXpr1 单元在膜中组成一对装配体,包含外部的运输核心和内部的调节域。在中央通路上,他们观察到两个不同的位置可供磷酸停驻,由带正电的氨基酸协调;这些位点在人类和植物同源蛋白中保守,突显了识别磷酸的共同蓝图。然而,不同于其同类,酵母蛋白在这一路径上构建了两道物理门。内侧由一个称为 N-loop 的柔性片段构成,受附近短螺旋及一条跨膜螺旋伸长端的支撑,折入孔口阻断磷酸进入;外侧则由两螺旋之间的一小段环形成塞子,封闭出口。对任一门进行突变或截短都会导致通道更多磷酸泄漏,证实这些结构通常将蛋白维持在自我抑制的闭合状态。
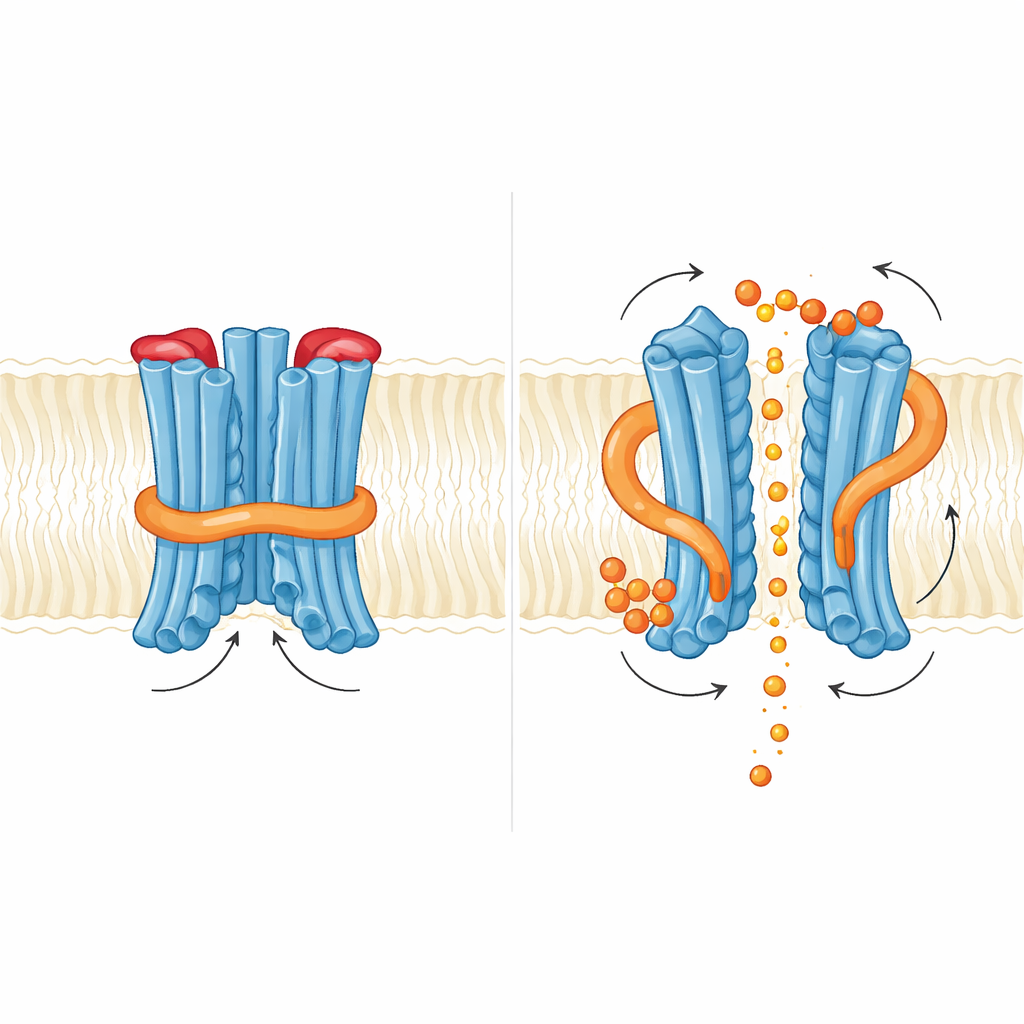
小型信使如何推动门的开合
团队接着研究了 InsP6 结合时发生的变化。他们发现两个富含碱性残基的结合口:一个位于调节域与膜核心相接处,另一个位于二聚体中两个调节域的接口处。InsP6 结合引起调节区域的细微旋转并使支撑 N-loop 的短螺旋变得不稳定,但在捕获到的结构中该环仍然位于阻挡磷酸的位置。在功能上,加入 InsP6 会增加磷酸电流,但削弱 InsP6 结合的突变并未完全消除外排,有时甚至增强了外排活性。这表明在酵母中,肌醇类信号分子更像是松动内部锁的微调器,而非简单的开/关开关。作者提出,更高带电的肌醇焦磷酸盐(如 InsP7 或 InsP8)可能才是真正的生理触发物,能够完全推动内侧 N-loop 门和外侧塞子移开。
超越酵母的意义
这些结构与功能实验共同支持一个工作模型:SpXpr1 通常处于双重上锁状态,内门与外门一道守护磷酸通路。在磷酸过剩时产生的肌醇基信号逐渐释放这些锁,让磷酸外流以保护细胞。与人类外排蛋白使用不同可动片段来堵塞和打开孔道相比,酵母的解决方案展示了进化如何在相同的基本骨架上进行改造以适应不同的生活方式——真菌中趋于严格保守,而哺乳动物则倾向于快速外排。理解这些设计原理可帮助研究者调整作物的磷酸利用、设计破坏真菌磷酸控制的靶向抗真菌药物,以及更好地解读人类 XPR1 蛋白致病变异的影响。
引用: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
关键词: 磷酸盐稳态, 离子通道, 冷冻电镜结构, 肌醇多磷酸盐, 膜运输