Clear Sky Science · pl
Wgląd w mechanizm zamykania i otwierania eksportera fosforanów SpXpr1 drożdży podziałowych
Dlaczego małe bramki dla fosforanów mają znaczenie
Każda komórka musi ostrożnie regulować poziom fosforanów — małego, lecz niezbędnego składnika cząsteczek takich jak DNA, błony czy waluta energetyczna komórki. Zbyt mało fosforanów zatrzymuje wzrost; zbyt dużo może być toksyczne. W pracy tej zbadano, jak drożdże podziałowe, modelowy grzyb, wypychają nadmiar fosforanów przez komórkowy „drzwiowy” białkowy kanał zwany SpXpr1. Ujawniając trójwymiarową strukturę tego kanału i mechanizm jego otwierania oraz zamykania, badanie wyjaśnia, w jaki sposób bardzo różne organizmy — od grzybów po ludzi — używają spokrewnionych białek do utrzymania równowagi fosforanowej, z implikacjami dla chorób mózgu, funkcji nerek, rolnictwa i strategii przeciwgrzybiczych.
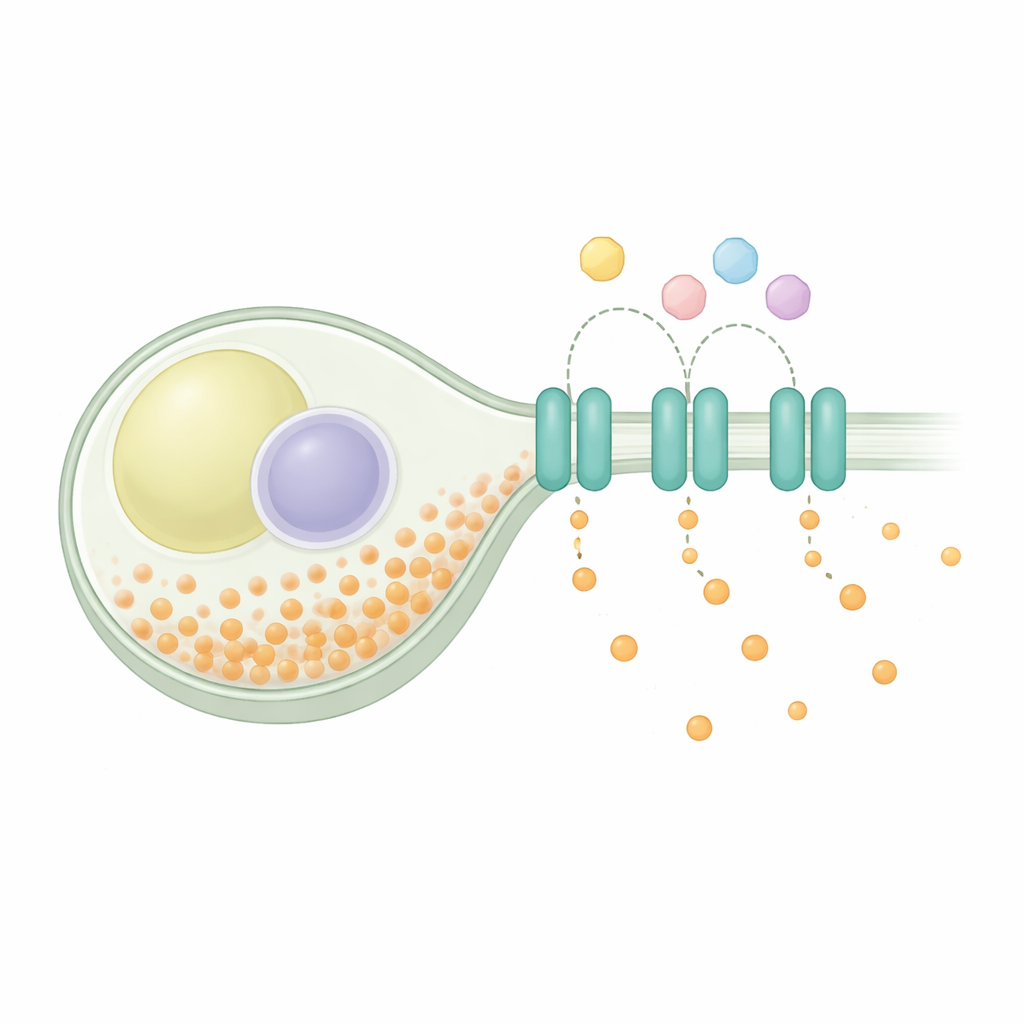
Utrzymanie równowagi wewnątrz komórki
Homeostaza fosforanów to uniwersalny problem: komórki muszą importować fosforany do metabolizmu i syntezy budulca, bezpiecznie przechowywać ich część i eksportować nadmiar. U drożdży systemy pobierania włączają się w warunkach niedoboru i wyłączają, gdy fosforanów jest dużo, podczas gdy kompleks magazynujący pakuje nadmiar w długie łańcuchy. Badania genetyczne sugerowały, że białko SpXpr1 działa jako wyspecjalizowany eksporter, chroniąc przed niebezpiecznym przeciążeniem, gdy szlaki magazynowania zawodzą. SpXpr1 należy do rodziny XPR1 obecnej u eukariontów, w tym roślin i ludzi, gdzie spokrewnione białka wiążą się z zaburzeniami takimi jak zwapnienia mózgu czy dysfunkcja nerek. Pomimo wspólnego pokrewieństwa nie było jasne, czy wersja drożdżowa działa tak samo jak ludzka.
Obserwacja białka i dowód, że jest kanałem
Badacze najpierw sprawdzili, czy SpXpr1 rzeczywiście przenosi fosforany przez błony. Wstawili drożdżowe białko do komórek ludzkich, z których usunięto własne XPR1, a następnie zmierzyli, ile fosforanów przedostało się do otaczającego roztworu. Komórki zawierające SpXpr1 eksportowały więcej fosforanów niż komórki kontrolne, co potwierdziło jego aktywność, choć było mniej wydajne niż u ludzkiego eksportera. Za pomocą pomiarów elektrycznych zespół wykazał następnie, że komórki obdarzone SpXpr1 wykazywały prądy zależne od fosforanów, które nasilały się w obecności małej cząsteczki sygnałowej inozytol heksofosforanu (InsP6). To ustaliło, że SpXpr1 jest prawdziwym kanałem umożliwiającym przejście jonów fosforanowych i że jego aktywność może być modulowana przez sygnały zawierające inozytol.
Dwa zamki wzdłuż wspólnej ścieżki
Aby zrozumieć działanie SpXpr1 na poziomie atomowym, autorzy użyli krio‑elektronowej mikroskopii do określenia jego struktury w obecności i braku InsP6. Każda jednostka SpXpr1 tworzy część parowej struktury w membranie i zawiera zewnętrzne jądro transportowe oraz wewnętrzną domenę regulacyjną. Wzdłuż centralnej drogi zaobserwowali dwa odrębne miejsca, gdzie może siedzieć fosforan, koordynowane przez reszty dodatnio naładowanych aminokwasów; te miejsca są zachowane u ludzkich i roślinnych odpowiedników, co podkreśla wspólny plan rozpoznawania samego fosforanu. Jednak w odróżnieniu od krewniaków, białko drożdżowe zbudowało dwie fizyczne bramy w tej ścieżce. Od wewnątrz giętki fragment zwany pętlą N (N-loop), wspierany przez pobliską krótką helisę i wydłużony koniec jednej helisy przezbłonowej, składa się w wejściu poru i blokuje dostęp fosforanów. Na zewnątrz mała pętla między dwiema helisami tworzy korek zamykający wyjście. Mutacje lub przycięcie którejkolwiek z tych bram powodowały większe przecieki fosforanów, co potwierdziło, że zwykle utrzymują one białko w samohamującym, zamkniętym stanie.
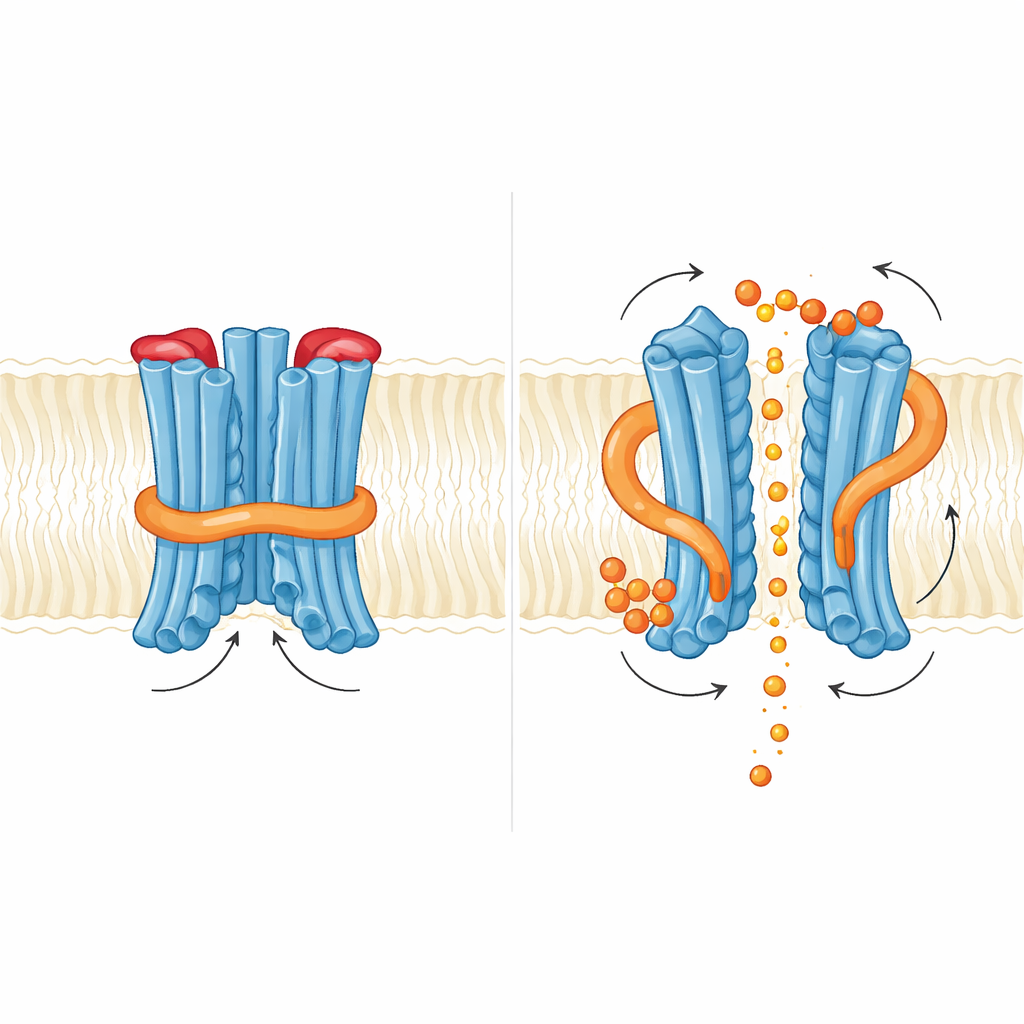
Jak mały przekaźnik porusza zamkami
Zespół następnie zbadał, co się dzieje po związaniu InsP6. Znaleźli dwa miejsca wiążące bogate w zasadowe reszty: jedno tam, gdzie domena regulacyjna styka się z rdzeniem błonowym, i drugie na styku między dwiema domenami regulacyjnymi w dimerze. Związanie InsP6 spowodowało subtelny obrót regionu regulacyjnego i destabilizację krótkiej helisy podpierającej pętlę N, ale sama pętla w zarejestrowanych strukturach nadal blokowała dostęp fosforanowi. Funkcjonalnie dodanie InsP6 zwiększyło prądy fosforanowe, lecz mutacje osłabiające wiązanie InsP6 nie eliminowały eksportu, a czasem nawet go wzmagały. Sugeruje to, że u drożdży inozytolowy przekaźnik działa raczej jak precyzyjne narzędzie poluzowujące wewnętrzną blokadę niż jako przełącznik włącz/wyłącz. Autorzy proponują, że wysoko naładowane inozytolowe pirofosforany, takie jak InsP7 lub InsP8, mogą być fizjologicznymi wyzwalaczami zdolnymi do pełnego odchylenia zarówno wewnętrznej pętli N, jak i zewnętrznego korka z drogi.
Co to znaczy poza drożdżami
Razem te eksperymenty strukturalne i funkcjonalne wspierają model roboczy, w którym SpXpr1 zazwyczaj znajduje się w stanie z dwuetapowym zablokowaniem — z wewnętrzną i zewnętrzną bramą chroniącymi ścieżkę fosforanową. Wzrastające poziomy sygnałów inozytolowych powstających przy nadmiarze fosforanów stopniowo zwalniają te blokady, pozwalając na wypływ fosforanów i ochronę komórki. W porównaniu z ludzkim eksporterem, który używa innego ruchomego elementu do zatykania i odtykania poru, rozwiązanie drożdżowe pokazuje, jak ewolucja może przekształcić ten sam podstawowy szkielet, by dopasować go do różnych trybów życia — ścisła konserwacja u grzybów versus szybki eksport u ssaków. Zrozumienie tych zasad projektowych może pomóc badaczom w regulacji wykorzystania fosforanów w uprawach, projektowaniu ukierunkowanych leków przeciwgrzybiczych zaburzających kontrolę fosforanów w grzybach oraz lepszej interpretacji zmian chorobotwórczych w ludzkim białku XPR1.
Cytowanie: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
Słowa kluczowe: homeostaza fosforanów, kanały jonowe, struktura cryo-EM, inozytolowe polifosforany, transport przez błonę