Clear Sky Science · ar
رؤى بنيوية في آلية الفتح والإغلاق لمُصدر الفوسفات في خميرة الانشطار SpXpr1
لماذا تهم البوابات الصغيرة للفوسفات
كل خلية مضطرة لتحقيق توازن دقيق للفوسفات، وهو مكوّن صغير لكنه لا غنى عنه في جزيئات مثل الحمض النووي، والأغشية، والعملات الطاقية للخلية. قِلّة الفوسفات توقف النمو؛ والكثرة قد تكون سامة. تبحث هذه الدراسة كيف تدفع خميرة الانشطار، كنموذج للفطريات، الفوسفات الزائدة خارج الخلية عبر باب جزيئي يسمى SpXpr1. بكشف البنية ثلاثية الأبعاد لهذا الباب وكيفية فتحه وإغلاقه، يلقي العمل ضوءاً على كيفية استخدام كائنات مختلفة—من الفطريات إلى البشر—لبروتينات ذات صلة للحفاظ على مستويات الفوسفات، مع تبعات لأمراض الدماغ، وصحة الكلى، والزراعة، واستراتيجيات مضادة للفطريات.
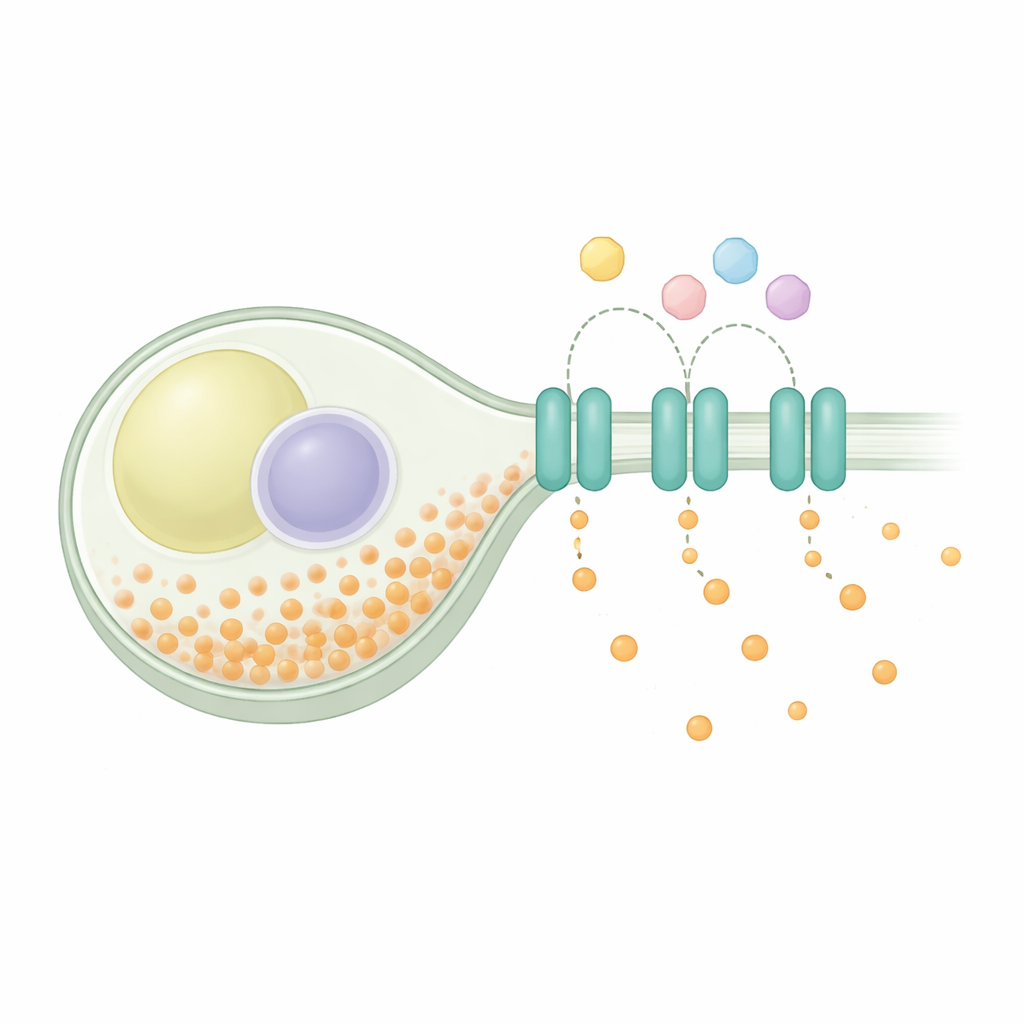
الحفاظ على التوازن داخل الخلية
الاتزان الفوسفاتي مشكلة عالمية: يجب على الخلايا استيراد الفوسفات للأيض وبناء المكونات، وتخزين جزء منها بأمان، وتصدير الفائض. في خميرة الانشطار تُفعَّل أنظمة الامتزاز عند النَّدرة وتُغلق عندما يتوفر الفوسفات بكثرة، بينما تعبئ مركبات التخزين الفوسفات الزائد في سلاسل طويلة. أشارت دراسات وراثية إلى أن بروتينًا يُدعى SpXpr1 يعمل كمصدر مخصص، مساهماً في منع التحميل الخطير عندما تتعطل مسارات التخزين. ينتمي SpXpr1 إلى عائلة XPR1 من المُصدّرات الموجودة عبر حقيقيات النوى، بما في ذلك النباتات والبشر، حيث ترتبط بروتينات مماثلة باضطرابات مثل تكلس الدماغ وضعف وظائف الكلى. رغم هذا الأصل العائلي المشترك، لم يكن واضحًا ما إذا كان نسخة الخميرة تعمل بالطريقة نفسها كما في البروتين البشري.
رؤية البروتين وإثبات أنه قناة
اختبر الباحثون أولاً ما إذا كان SpXpr1 ينقل الفوسفات فعلاً عبر الأغشية. أدخلوا بروتين الخميرة في خلايا بشرية أزيل منها XPR1 الخاص بها، ثم قاسوا مقدار الفوسفات المتسرب إلى الوسط المحيط. صدّرَت الخلايا التي تحتوي على SpXpr1 فوسفات أكثر من الخلايا الضابطة، مؤكدين فعاليته، على الرغم من أنه كان أقل كفاءة من المصدر البشري. باستخدام تسجيلات كهربائية، أظهر الفريق أن الخلايا التي تحمل SpXpr1 تظهر تيارات معتمدة على الفوسفات تزداد عند وجود الجزيء الإشارِي الصغير إنوزيتول هيكسافوسفات (InsP6). هذا أثبت أن SpXpr1 قناة حقيقية تسمح بمرور أيونات الفوسفات ويمكن تعديلها بواسطة رُسُل محتوِية على إنوزيتول.
بوابتان على طول ممر مشترك
لفهم كيفية عمل SpXpr1 على المستوى الذري، استخدم المؤلفون المجهر الإلكتروني بالتبريد لتحديد بنيته بغياب ووجود InsP6. يشكل كل وحدة من SpXpr1 جزءًا من تجميع ثنائي في الغشاء ويحتوي على لب نقل خارجي ومجال تنظيمي داخلي. على طول المسار المركزي، رصدوا موضعين متميزين يمكن للفوسفات أن يستقرا فيهما، منسقين بأحماض أمينية مشحونة موجبة؛ هذه المواقع محافظة في النُّسخ البشرية والنباتية، مما يبرز مخططًا مشتركًا لكيفية التعرف على الفوسفات نفسها. ومع ذلك، وعلى خلاف أقربائه، يبني بروتين الخميرة بوابتيْن ماديتيْن داخل هذا الممر. من الداخل، يقبّع مقطع مرن يُدعى حلقة N، مدعومًا بواسطة لولب قصير قريب ونهاية ممتدة لأحد الحلقات العبر غشائية، مدخل المسام ويمنع دخول الفوسفات. من الخارج، تشكل حلقة صغيرة بين حلزونيْن قُطعة تغلق المخرج. تسببت طفرات أو اقتطاع أيٍّ من هاتين البوابتين في تسرب الفوسفات من القناة أكثر، مؤكدة أنها عادة تحافظ على البروتين في حالة مثبطة ذاتية ومغلقة.
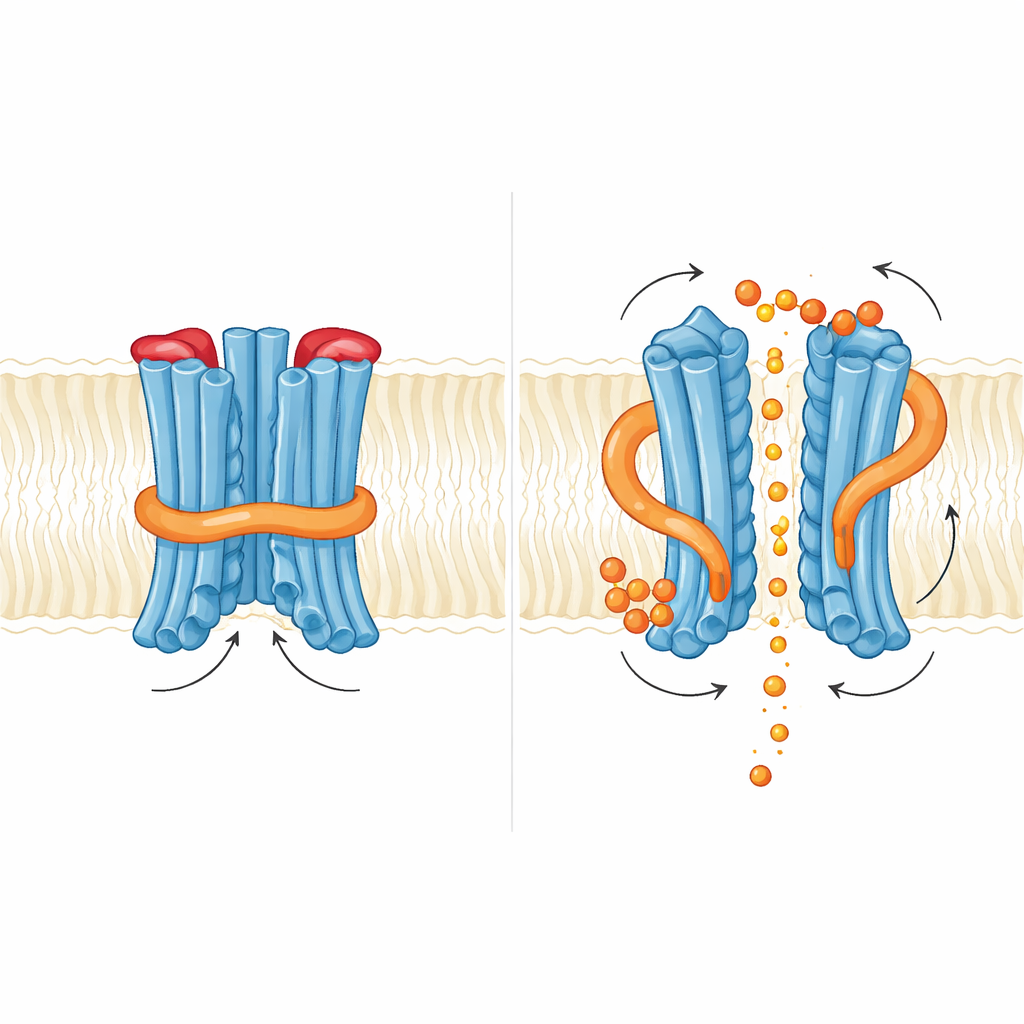
كيف يدفع رسول صغير البوابات
فحص الفريق بعد ذلك ما يحدث عند ارتباط InsP6. وجدوا جيوب ارتباط غنيّة بالبقايا القاعدية: واحدة عند لقاء المجال التنظيمي بنواة الغشاء، وأخرى عند الواجهة بين المجالين التنظيميين في الثنائي. تسبب ارتباط InsP6 في دوران طفيف للمنطقة التنظيمية وزعزعة اللولب القصير الذي يدعم حلقة N، لكن الحلقة نفسها ظلت في طريق الفوسفات في البُنى الملتقطة. وظيفيًا، أدى إضافة InsP6 إلى زيادة تيارات الفوسفات، لكن الطفرات التي أضعفت ارتباط InsP6 لم تُلغِ التصدير وأحيانًا حسّنته. هذا يوحي أنه في الخميرة يعمل رسول الإنوزيتول كضابط دقيق يرخّي قفلًا داخليًا بدل أن يكون مفتاح تشغيل/إيقاف. يقترح المؤلفون أن الإنوزيتول متعدد الفوسفات الأعلى شحنة، مثل InsP7 أو InsP8، قد يكون المحفز الفسيولوجي الحقيقي القادر على دفع كل من بوابة حلقة N الداخلية والقطعة الخارجية بالكامل جانبًا.
ماذا يعني هذا خارج عالم الخميرة
معًا، تدعم هذه التجارب البنيوية والوظيفية نموذجًا عمليًا يكون فيه SpXpr1 عادة في حالة مقفلة مزدوجة، مع بوابة داخلية وخارجية تحرسان ممر الفوسفات. تسمح المستويات المتصاعدة للإشارات القائمة على الإنوزيتول الناتجة أثناء فائض الفوسفات بفك هذه الأقفال تدريجيًا، مما يتيح تدفق الفوسفات للخارج وحماية الخلية. مقارنة بالمصدر البشري، الذي يستخدم مقطعًا متحركًا مختلفًا لسدّ وفتح مسامه، تُظهر حلَّة الخميرة كيف يمكن للتطور إعادة توصيل نفس الهيكل الأساسي ليتلاءم مع أنماط حياة مختلفة—حفظ صارم في الفطريات مقابل تصدير سريع في الثدييات. قد يساعد فهم هذه مبادئ التصميم الباحثين على ضبط استخدام الفوسفات في المحاصيل، وتصميم أدوية مضادة للفطريات تستهدف التحكم الفطري بالفوسفات، وتفسير التغيرات المسببة للأمراض في بروتين XPR1 البشري بشكل أفضل.
الاستشهاد: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
الكلمات المفتاحية: الاتزان الفوسفاتي, قنوات الأيونات, بنية التجميد-الإلكترون, الإنوزيتول متعدد الفوسفات, نقل عبر الغشاء