Clear Sky Science · ja
出芽酵母のリン酸排出体 SpXpr1 のゲーティング機構に関する構造的知見
なぜ小さなリン酸の通路が重要なのか
すべての細胞は、DNA、膜、そして細胞のエネルギー通貨などの分子に不可欠な小さな成分であるリン酸を厳密に管理する必要があります。リン酸が不足すると成長が停滞し、過剰だと毒性を示します。本研究は、モデル菌である分裂酵母が余剰のリン酸を細胞外へ押し出す分子通路 SpXpr1 のしくみを調べます。この通路の三次元構造と開閉の様子を明らかにすることで、菌類からヒトに至るさまざまな生物が関連タンパク質を用いてリン酸濃度を制御する方法に光を当て、脳の石灰化、腎機能、農業、抗真菌戦略に関する示唆を与えます。
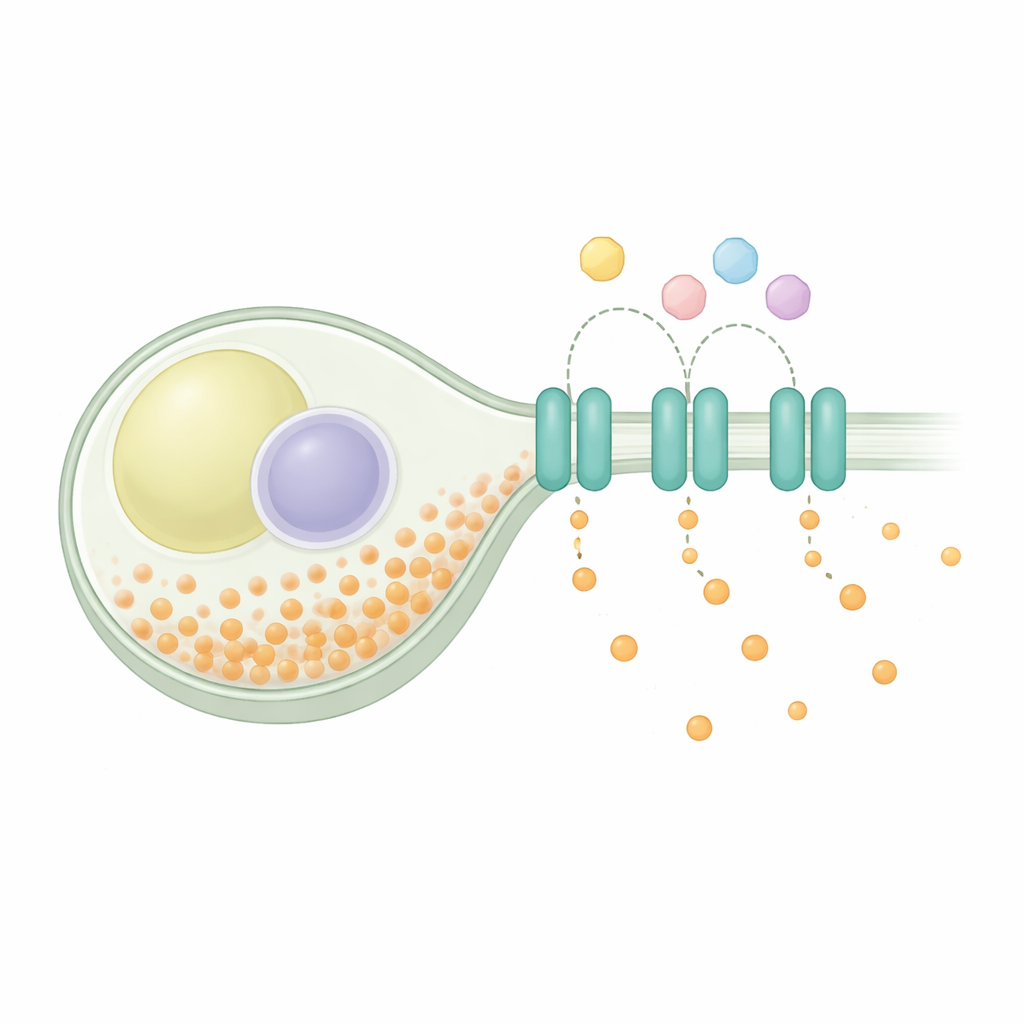
細胞内のバランスを保つ
リン酸恒常性は普遍的な課題です:細胞は代謝や構成要素のためにリン酸を取り込み、余剰を安全に貯蔵し、過剰分を排出する必要があります。分裂酵母では、欠乏時に取り込みシステムが作動し、リン酸が豊富なときには停止します。一方で、余剰リン酸は長鎖にして貯蔵されます。遺伝学的研究は、SpXpr1 と呼ばれるタンパク質が専用の排出体として働き、貯蔵経路が損なわれた場合に有害な過負荷を防ぐのに寄与することを示唆していました。SpXpr1 は広く真核生物に存在する XPR1 ファミリーに属し、植物やヒトにも対応タンパク質があり、脳の石灰化や腎障害と関連付けられています。にもかかわらず、酵母のバージョンがヒトタンパク質と同じ仕組みで働くかは不明でした。
タンパク質の可視化とチャネルであることの証明
研究者らはまず SpXpr1 が本当に膜を横切ってリン酸を移動させるかを検証しました。酵母タンパク質を自前の XPR1 を欠くヒト細胞に発現させ、どれだけリン酸が周囲の溶液へ流出するかを測定しました。SpXpr1 を持つ細胞はコントロールよりもリン酸を多く排出し、その活性が確認されましたが、ヒト由来の排出体より効率は低いことが分かりました。電気記録を用いて、SpXpr1 を有する細胞はイノシトールヘキサキシホスフェート(InsP6)という小さなシグナル分子が存在するとリン酸依存性の電流が増加することも示しました。これにより、SpXpr1 がリン酸イオンを通す真正のチャネルであり、イノシトール含有メッセンジャーによって調節され得ることが確立されました。
共通経路に沿った二つの扉
SpXpr1 の原子レベルでの働きを理解するため、著者らはクライオ電子顕微鏡を用いて InsP6 の有無でその構造を決定しました。各 SpXpr1 ユニットは膜中で対をなす構造の一部を形成し、外側に輸送コア、内側に調節ドメインを持ちます。中心経路に沿って、リン酸が位置しうる二つの明瞭な座を観察し、それらは正に荷電したアミノ酸で配置されていました。これらの部位はヒトや植物の対応体でも保存されており、リン酸自体の認識に共通の設計図があることを示しています。しかし、類縁タンパク質とは異なり、酵母タンパク質はこの経路に二つの物理的なゲートを備えています。内側では、Nループと呼ばれる柔軟なセグメントが、近傍の短いヘリックスと一つの膜貫通ヘリックスの伸長末端によって支えられ、孔の入口に折り込まれてリン酸の侵入を遮断します。外側では、二つのヘリックス間の小さなループが出口を塞ぐ栓の役割を果たします。これらのゲートを変異させるか切り詰めるとチャネルからのリン酸リークが増え、通常はこれらが自己抑制された閉鎖状態を保持していることが確認されました。
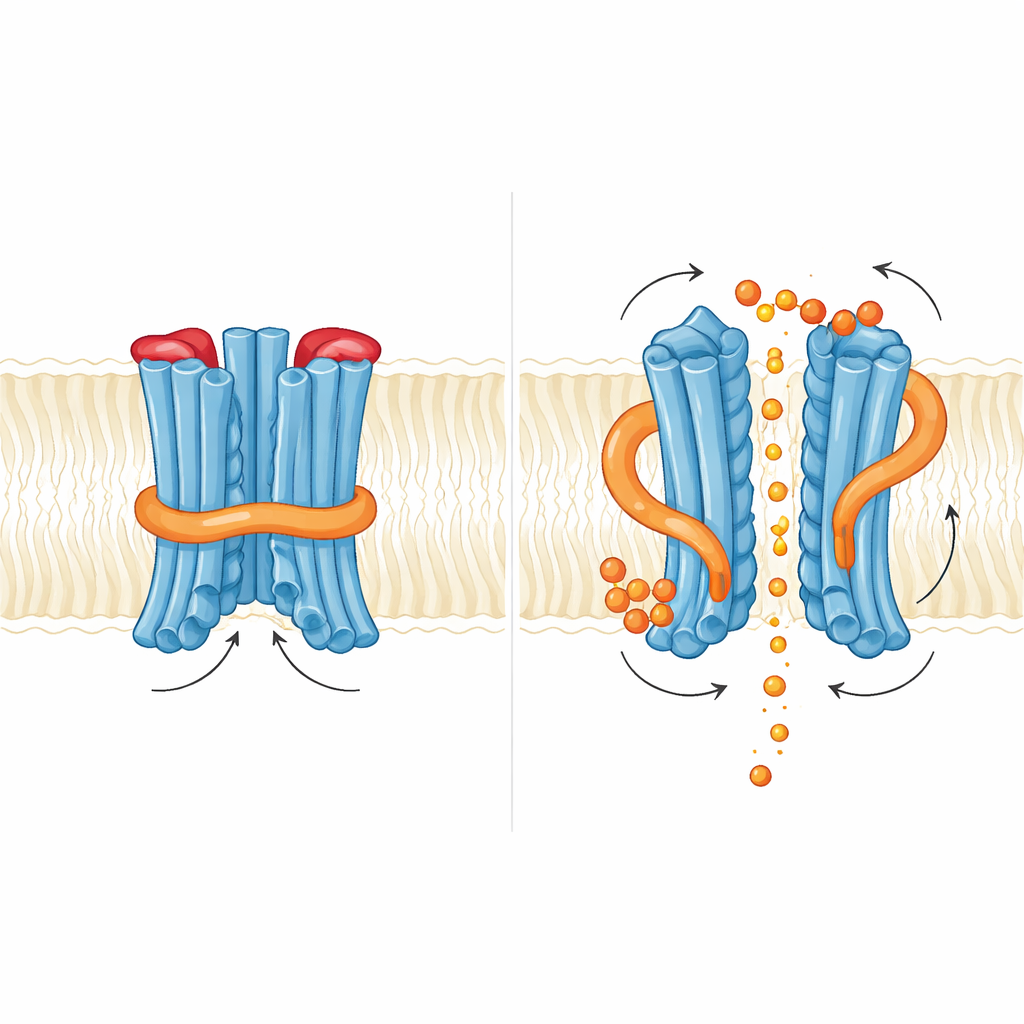
小さなメッセンジャーが扉をどう押すか
次に InsP6 が結合したときに何が起きるかを調べました。調節ドメインが膜コアに接する部位と、二量体中で二つの調節ドメインの界面に位置する部位の二つの結合ポケットが見つかり、どちらも塩基性残基に富んでいました。InsP6 の結合は調節領域のわずかな回転と Nループを支える短いヘリックスの不安定化を引き起こしましたが、捕捉された構造ではループ自体は依然としてリン酸の道を塞いだままでした。機能的には、InsP6 の添加はリン酸電流を増加させましたが、InsP6 結合を弱める変異は輸出を完全には消さず、場合によっては増強することもありました。これらのことから、酵母ではイノシトールのメッセンジャーは内部のロックを緩める精密な調整役であり、単純なオン・オフスイッチではないと考えられます。著者らは、InsP7 や InsP8 のようなより高荷電のイノシトールピロリン酸が、内側の N ループゲートと外側のプラグの両方を完全に開放できる生理的なトリガーである可能性を提案しています。
酵母を越えた意義
これらの構造的および機能的実験は、SpXpr1 が通常は内側と外側の二重ロック状態にあり、リン酸経路を守っているという作業モデルを支持します。リン酸過剰時に産生されるイノシトール系シグナルの上昇はこれらのロックを徐々に解除し、リン酸を流出させて細胞を保護します。ヒトの排出体は異なる可動セグメントを用いて孔を塞いだり開けたりするのに対し、酵母は同じ基本骨格を進化的に書き換えて異なるライフスタイルに適応させていることが示されます—菌類では厳密な保存、哺乳類では迅速な輸出。これらの設計原理の理解は、作物のリン酸利用を調整する研究、真菌のリン酸制御を破壊する標的型抗真菌薬の設計、そしてヒト XPR1 タンパク質の病的変化の解釈に役立つ可能性があります。
引用: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
キーワード: リン酸恒常性, イオンチャネル, クライオ電顕構造, イノシトール多リン酸, 膜輸送