Clear Sky Science · es
Perspectivas estructurales sobre el mecanismo de apertura del exportador de fosfato SpXpr1 de la levadura de fisión
Por qué importan las pequeñas puertas para el fosfato
Cada célula debe equilibrar cuidadosamente el fosfato, un ingrediente pequeño pero indispensable en moléculas como el ADN, las membranas y la moneda energética de la célula. Muy poco fosfato frena el crecimiento; demasiado puede ser tóxico. Este estudio analiza cómo la levadura de fisión, un hongo modelo, expulsa el fosfato en exceso fuera de la célula mediante una puerta molecular llamada SpXpr1. Al revelar la estructura tridimensional de esta puerta y cómo se abre y se cierra, el trabajo aclara cómo organismos muy distintos —desde hongos hasta humanos— usan proteínas relacionadas para mantener el nivel de fosfato bajo control, con implicaciones para enfermedades cerebrales, la salud renal, la agricultura y estrategias antifúngicas.
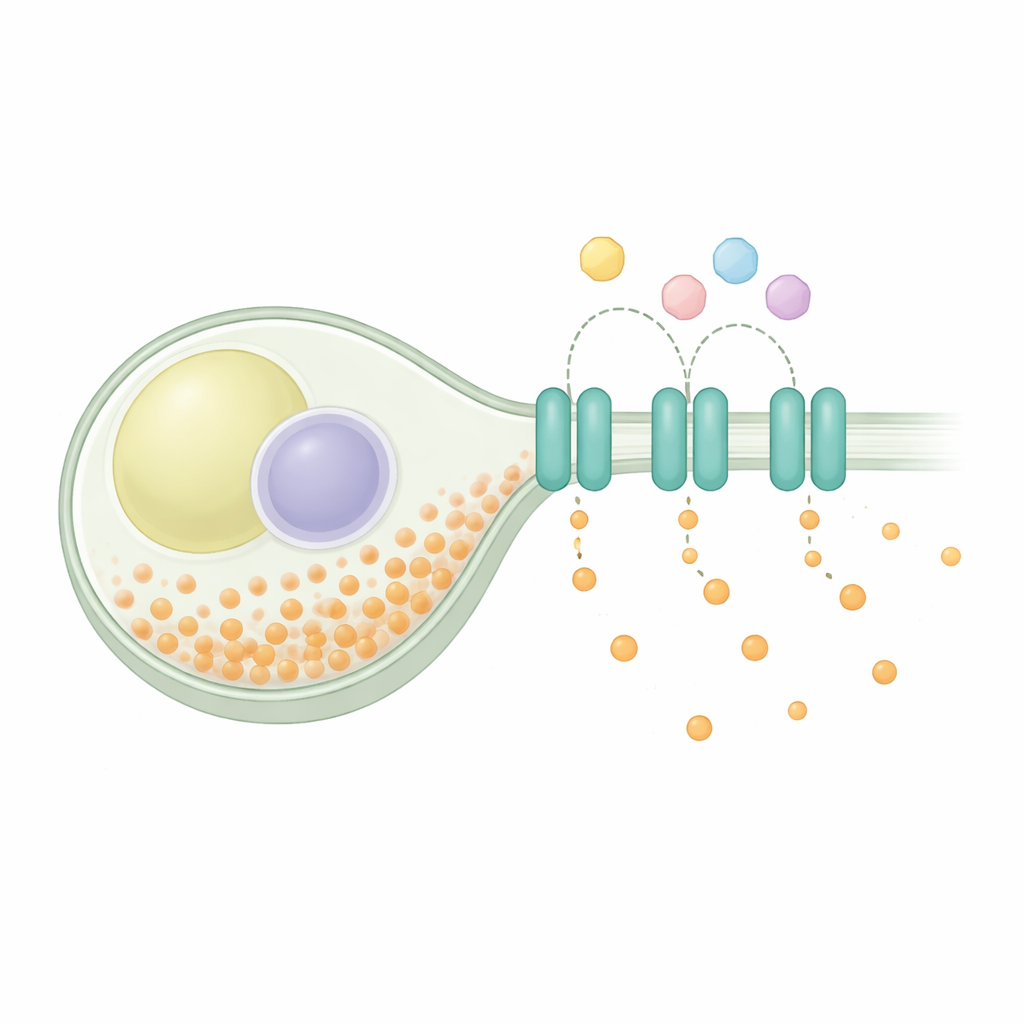
Mantener el equilibrio dentro de la célula
La homeostasis del fosfato es un problema universal: las células deben importar fosfato para el metabolismo y los bloques de construcción, almacenar parte de forma segura y exportar el excedente. En la levadura de fisión, los sistemas de captación se activan bajo escasez y se apagan cuando el fosfato es abundante, mientras que un complejo de almacenamiento empaqueta el exceso en cadenas largas. Estudios genéticos sugerían que una proteína llamada SpXpr1 actúa como exportador dedicado, ayudando a prevenir una sobrecarga peligrosa cuando las vías de almacenamiento están comprometidas. SpXpr1 pertenece a la familia XPR1 de exportadores presente en eucariotas, incluidas plantas y humanos, donde proteínas relacionadas se asocian a trastornos como la calcificación cerebral y la disfunción renal. A pesar de este origen familiar compartido, no estaba claro si la versión de levadura funcionaba de la misma manera que la proteína humana.
Ver la proteína y demostrar que es un canal
Los investigadores primero comprobaron si SpXpr1 realmente transporta fosfato a través de membranas. Insertaron la proteína de levadura en células humanas a las que se había eliminado su propio XPR1 y, a continuación, midieron cuánto fosfato se filtraba al medio circundante. Las células con SpXpr1 exportaron más fosfato que las de control, confirmando su actividad, aunque con menor eficiencia que el exportador humano. Mediante registros eléctricos, el equipo mostró que las células que portaban SpXpr1 presentaban corrientes dependientes de fosfato que aumentaban cuando estaba presente la pequeña molécula señal Inositol hexakisfosfato (InsP6). Esto estableció a SpXpr1 como un canal genuino que permite el paso de iones fosfato y que puede modularse mediante mensajeros que contienen inositol.
Dos puertas a lo largo de una vía compartida
Para entender cómo funciona SpXpr1 a nivel atómico, los autores usaron criomicroscopía electrónica para determinar su estructura en ausencia y en presencia de InsP6. Cada unidad de SpXpr1 forma parte de un ensamblaje pareado en la membrana y contiene un núcleo de transporte externo y un dominio regulador interno. A lo largo de la vía central observaron dos puntos distintos donde el fosfato puede alojarse, coordinado por aminoácidos con carga positiva; estos sitios se conservan en las contrapartes humanas y vegetales, lo que subraya un diseño compartido para el reconocimiento del propio fosfato. Sin embargo, a diferencia de sus parientes, la proteína de levadura integra dos compuertas físicas en esta vía. En el interior, un segmento flexible llamado bucle N, sostenido por una hélice corta cercana y por un extremo extendido de una de las hélices transmembrana, se pliega en la entrada del poro y bloquea la entrada del fosfato. En el exterior, un pequeño lazo entre dos hélices forma un tapón que cierra la salida. Mutar o recortar cualquiera de estas compuertas provocó que el canal filtrara más fosfato, confirmando que normalmente mantienen la proteína en un estado auto-inhibido y cerrado.
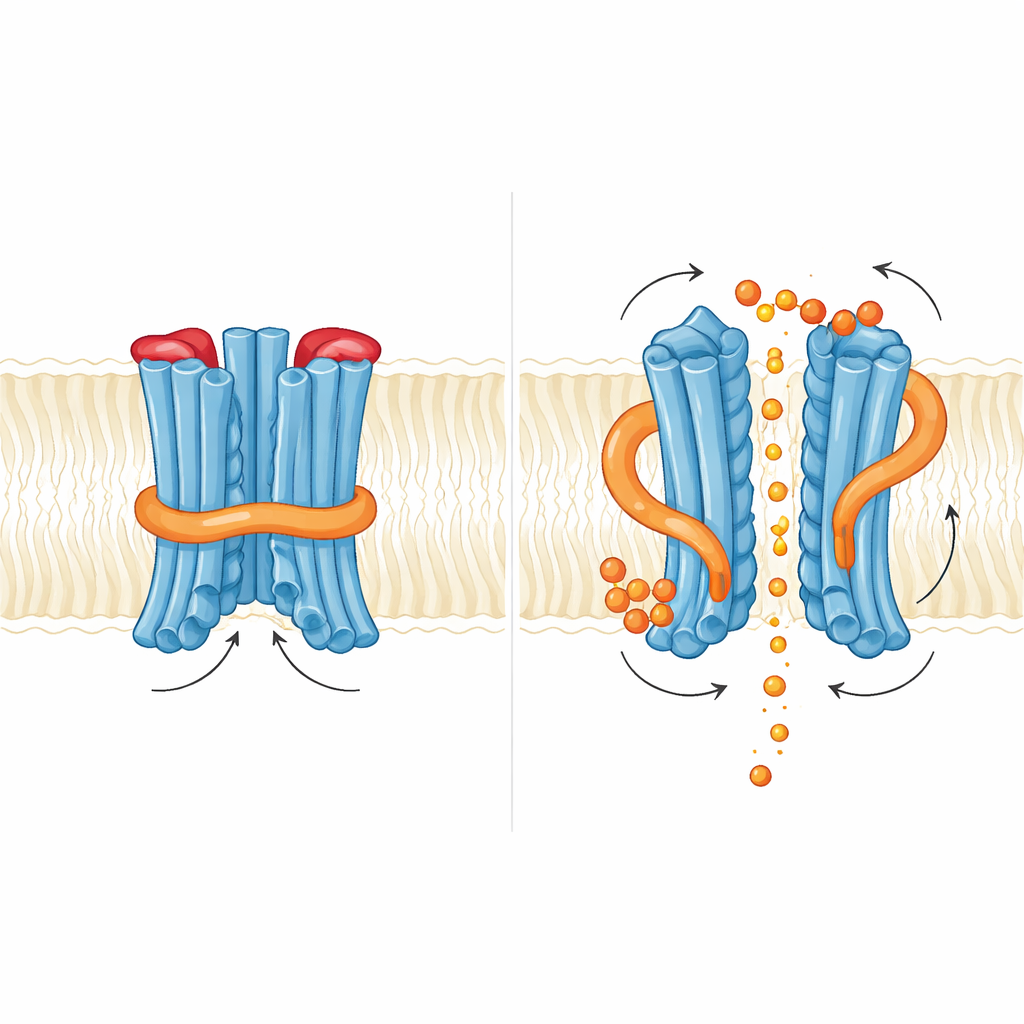
Cómo un pequeño mensajero empuja las compuertas
El equipo examinó luego qué ocurre cuando se une InsP6. Encontraron dos bolsillos de unión ricos en residuos básicos: uno donde el dominio regulador se encuentra con el núcleo de membrana, y otro en la interfase entre los dos dominios reguladores del dímero. La unión de InsP6 provocó una rotación sutil de la región reguladora y desestabilizó la hélice corta que refuerza el bucle N, pero el propio bucle seguía ocupando el paso del fosfato en las estructuras capturadas. Funcionalmente, la adición de InsP6 aumentó las corrientes de fosfato, pero las mutaciones que debilitaban la unión a InsP6 no abolieron la exportación e incluso en ocasiones la aumentaron. Esto sugiere que, en la levadura, el mensajero de inositol actúa más como un regulador fino que afloja un cerrojo interno que como un interruptor de encendido/apagado. Los autores proponen que los inositol pirofosfatos con mayor carga, como InsP7 o InsP8, podrían ser los desencadenantes fisiológicos reales capaces de abrir completamente tanto la compuerta interior del bucle N como el tapón exterior.
Qué significa esto más allá de la levadura
En conjunto, estos experimentos estructurales y funcionales apoyan un modelo operativo en el que SpXpr1 normalmente se encuentra en un estado de doble cierre, con una compuerta interna y otra externa que protegen la vía del fosfato. El aumento de señales basadas en inositol producidas durante el exceso de fosfato libera gradualmente estos cierres, permitiendo que el fosfato fluya hacia fuera y proteja a la célula. En comparación con el exportador humano, que usa un segmento móvil diferente para taponar y destaponar su poro, la solución de la levadura muestra cómo la evolución puede reconducir el mismo andamiaje básico para adaptarlo a distintos modos de vida —conservación estricta en hongos frente a exportación más rápida en mamíferos. Comprender estos principios de diseño podría ayudar a los investigadores a ajustar el uso del fosfato en cultivos, diseñar fármacos antifúngicos dirigidos que alteren el control fúngico del fosfato y a interpretar mejor los cambios patogénicos en la proteína humana XPR1.
Cita: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
Palabras clave: homeostasis del fosfato, canales iónicos, estructura por criomicroscopía electrónica, inositol polifosfatos, transporte de membrana