Clear Sky Science · nl
Structurele inzichten in het klepmechanisme van de fission-gist fosfaatexporter SpXpr1
Waarom kleine doorgangen voor fosfaat ertoe doen
Elke cel moet fosfaat zorgvuldig in balans houden: een klein maar onmisbaar bestanddeel van moleculen zoals DNA, membraanlipiden en de energievaluta van de cel. Te weinig fosfaat remt groei; te veel kan giftig zijn. Deze studie bekijkt hoe fission-gist, een modelschimmel, overtollig fosfaat uit de cel dringt via een moleculaire deuropening genaamd SpXpr1. Door de driedimensionale structuur van deze opening te onthullen en te laten zien hoe ze opengaat en sluit, werpt het werk licht op hoe sterk verschillende organismen — van schimmels tot mensen — verwante eiwitten gebruiken om fosfaatniveaus te reguleren, met implicaties voor hersenziekten, niergezondheid, landbouw en antischimmelstrategieën.
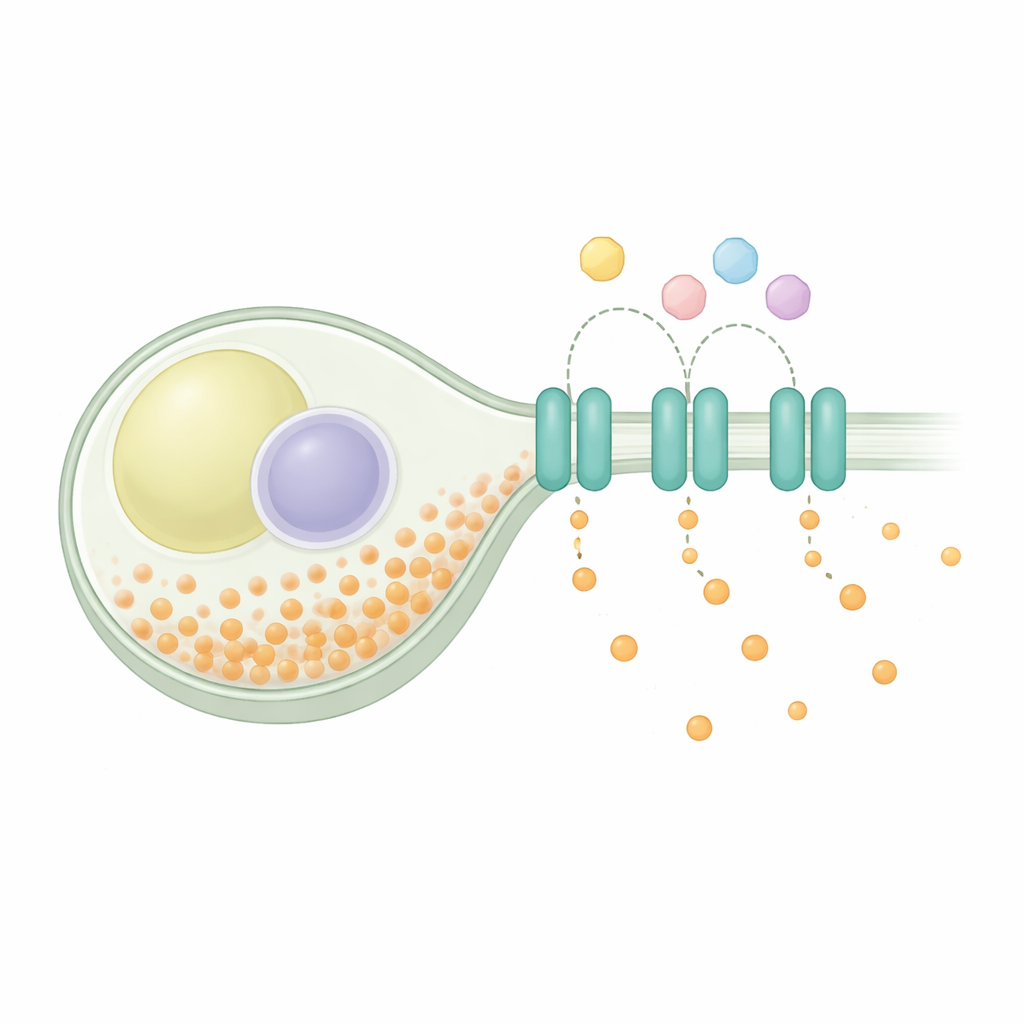
Het evenwicht binnen een cel bewaren
Fosfaathomeostase is een universeel probleem: cellen moeten fosfaat opnemen voor de stofwisseling en bouwstenen, een deel veilig opslaan en overtollig exporteren. Bij fission-gist worden opnamesystemen ingeschakeld bij schaarste en uitgeschakeld bij overvloed, terwijl een opslagcomplex overtollig fosfaat in lange ketens verpakt. Genetisch onderzoek suggereerde dat een eiwit genaamd SpXpr1 fungeert als een toegewijde exporter, die voorkomt dat de cel gevaarlijk overbelast raakt wanneer opslagroutes verstoord zijn. SpXpr1 behoort tot de XPR1-familie van exporters die in eukaryoten voorkomen, inclusief planten en mensen, waar verwante eiwitten in verband worden gebracht met aandoeningen zoals hersencalcificatie en nierfunctiestoornissen. Ondanks deze gemeenschappelijke familieachtergrond was onduidelijk of de gistversie op dezelfde manier werkte als het menselijke eiwit.
Het eiwit zien en bewijzen dat het een kanaal is
De onderzoekers testten eerst of SpXpr1 daadwerkelijk fosfaat door membranen verplaatst. Ze brachten het gist-eiwit in menselijke cellen in waarvan het eigen XPR1 was verwijderd, en maten vervolgens hoeveel fosfaat in de omliggende oplossing weglekte. Cellen met SpXpr1 exporteerden meer fosfaat dan controlecellen, wat de activiteit bevestigde, hoewel het minder efficiënt was dan de menselijke exporter. Met elektrische opnamen liet het team zien dat cellen met SpXpr1 fosfaat-afhankelijke stromen voerden die toenamen wanneer het kleine signaalmolecuul inositolhexakisfosfaat (InsP6) aanwezig was. Dit stelde SpXpr1 vast als een echt kanaal dat fosfaationen doorlaat en dat afgesteld kan worden door inositol-bevattende boodschappers.
Twee deuren langs een gedeeld pad
Om te begrijpen hoe SpXpr1 op atomaire schaal werkt, bepaalden de auteurs de structuur met cryo-elektronenmicroscopie in afwezigheid en aanwezigheid van InsP6. Elke SpXpr1-eenheid maakt deel uit van een gepaarde assemblage in het membraan en bevat een extern transportcore en een interne regulatoire domein. Langs het centrale pad zagen ze twee verschillende plekken waar fosfaat kan zitten, gecoördineerd door positief geladen aminozuren; deze sites zijn geconserveerd in menselijke en plantaardige tegenhangers, wat wijst op een gedeeld ontwerp voor herkenning van fosfaat zelf. Toch bouwt het gist-eiwit, in tegenstelling tot verwanten, twee fysieke poorten in dit pad. Aan de binnenkant vouwt een flexibele segment, de zogenaamde N-lus, ondersteund door een nabijgelegen korte helix en door een verlengd uiteinde van een membraan-helix, zich in de poreningang en blokkeert fosfaattoegang. Aan de buitenkant vormt een kleine lus tussen twee helixen een stop die de uitgang afsluit. Het muteren of afkappen van een van deze poorten liet het kanaal meer fosfaat lekken, wat bevestigt dat ze het eiwit normaal in een zelfgeïnhibeerde, gesloten toestand houden.
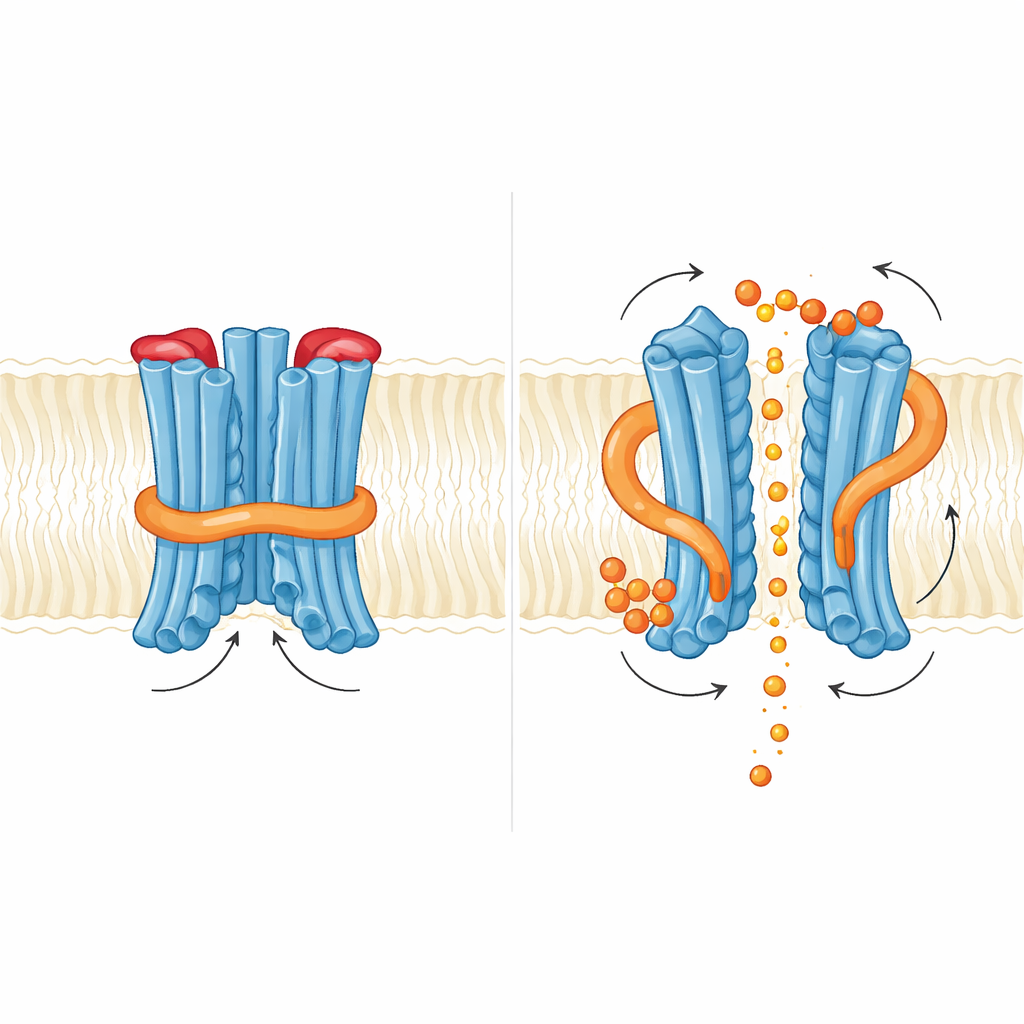
Hoe een kleine boodschapper de poorten verzet
Het team onderzocht vervolgens wat er gebeurt wanneer InsP6 bindt. Ze vonden twee bindingspockets rijk aan basische residuen: één waar het regulatoire domein het membraankern ontmoet, en een andere op het raakvlak tussen de twee regulatoire domeinen in het dimer. InsP6-binding veroorzaakte een subtiele rotatie van het regulatoire gebied en destabiliseerde de korte helix die de N-lus ondersteunt, maar de lus zelf bleef in de vastgelegde structuren nog steeds de weg van fosfaat blokkeren. Functioneel verhoogde toevoeging van InsP6 de fosfaatstromen, maar mutaties die de InsP6-binding verzwakten deden de export niet teniet en verhoogden die soms zelfs. Dit suggereert dat in gist de inositolboodschapper meer fungeert als een fijnafsteller die een intern slot versoepelt dan als een aan/uit-schakelaar. De auteurs stellen dat hoger geladen inositol-pyrofosfaten, zoals InsP7 of InsP8, mogelijk de werkelijke fysiologische triggers zijn die beide—de binnenste N-luspoort en de buitenste stop—volledig uit de weg kunnen zetten.
Wat dit betekent buiten gist
Gezamenlijk ondersteunen deze structurele en functionele experimenten een werkmodel waarin SpXpr1 normaal in een dubbel-vergrendelde toestand zit, met een binnenste en een buitenste poort die het fosfaatpad bewaken. Stijgende niveaus van inositol-gebaseerde signalen, geproduceerd tijdens fosfaatovervloed, lossen deze sloten geleidelijk, waardoor fosfaat kan uitstromen en de cel beschermt. Vergeleken met de menselijke exporter, die een ander beweegbaar segment gebruikt om zijn porie te sluiten en openen, toont de gistoplossing hoe evolutie hetzelfde basale geraamte kan herbedraden om aan verschillende levenswijzen te voldoen—strikte conservatie bij schimmels versus snelle export bij zoogdieren. Inzicht in deze ontwerppatronen kan onderzoekers helpen het fosfaatgebruik in gewassen bij te sturen, gerichte antischimmelmiddelen te ontwerpen die de schimmelcontrole van fosfaat verstoren, en ziekteveroorzakende veranderingen in het menselijke XPR1-eiwit beter te interpreteren.
Bronvermelding: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
Trefwoorden: fosfaathomeostase, ionkanalen, cryo-EM-structuur, inositolpolyfosfaten, membraantransport