Clear Sky Science · he
תובנות מבניות במנגנון הסגירה של מאייד הפוספט בשמר הפיצול SpXpr1
מדוע שערים זעירים לפוספט חשובים
כל תא חייב לאזן בקפידה את רמת הפוספט — מרכיב קטן אך חיוני במולקולות כמו DNA, ממברנות ומטבע האנרגיה של התא. עודף פוספט יכול להיות רעיל; חסרונו עוצר גידול. המחקר הזה בוחן איך שמר הפיצול, פטרייה מודלית, מוציא עודפי פוספט החוצה דרך «פתח מולקולרי» שנקרא SpXpr1. באמצעות גילוי המבנה התלת־ממדי של הפתח והאופן שבו הוא נפתח ונסגר, העבודה מבהירה כיצד אורגניזמים שונים — מפטריות ועד בני אדם — משתמשים בחלבונים קרובים לשמירה על איזון הפוספט, עם השלכות על מחלות מוחיות, בריאות הכליה, חקלאות ואסטרטגיות אנטיפטרייתיות.
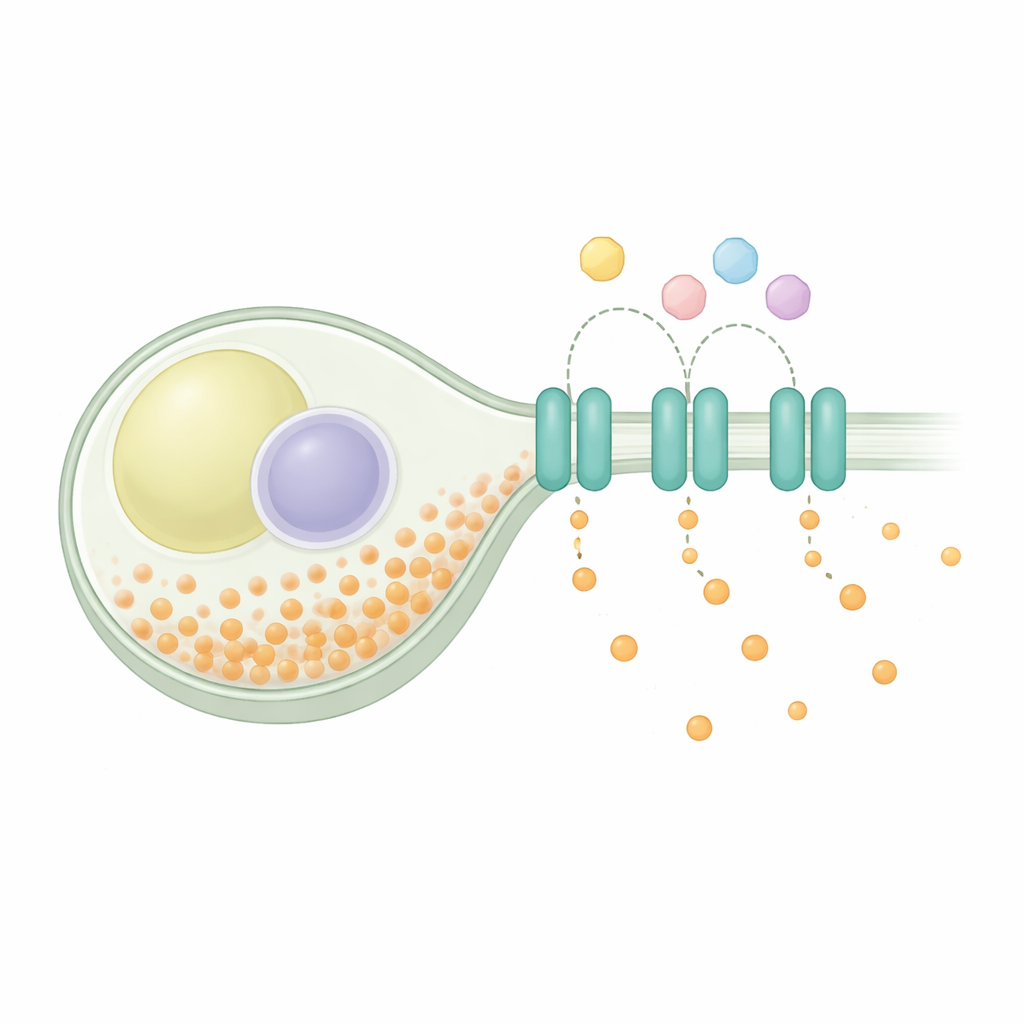
שמירה על איזון בתוך התא
הומאוסטזיס של פוספט הוא בעיה אוניברסלית: תאים צריכים לייבא פוספט למטרות מטבוליות ובניית רכיבים, לאחסן חלק ממנו בצורה בטוחה, ולייצא עודפים. בשמר הפיצול מערכות הייבוא מופעלות בתנאי מחסור ומכובות כשיש שפע, בעוד שמכלול אחסון אורז עודפי פוספט לשרשראות ארוכות. מחקרים גנטיים הציעו שחלבון בשם SpXpr1 פועל כמעביר מייצא ייעודי, ומסייע למנוע עומס מסוכן כאשר נתיבי האחסון מנותקים. SpXpr1 שייך למשפחת XPR1 של מייצאים הנמצאת בכל האוקריוטים, כולל צמחים ובני אדם, ושחלבונים קרובים קשורים להפרעות כמו הסתיידות מוחית ולתפקוד כלייתי לקוי. למרות שברקעם משפחתי משותף זה, לא היה ברור האם הגרסה השמרית פועלת באותו האופן כמו החלבון האנושי.
לצפות בחלבון ולהוכיח שמדובר בתעלה
החוקרים בקשו תחילה לבדוק אם SpXpr1 אכן מועבר פוספט דרך ממברנות. הם השרותו את החלבון השמרי לתאים אנושיים שממנו הוסר ה־XPR1 הטבעי, ואז מדדו כמה פוספט דלף לתמיסה סביבם. תאים שנשאו SpXpr1 ייצאו יותר פוספט מאשר תאים בבקרה, ואישרו את פעילותו, אם כי ביעילות נמוכה יותר מהמייצא האנושי. באמצעות הקלטות חשמליות הראו הצוות שתאים עם SpXpr1 נשאו זרמים התלויים בפוספט שהתגברו בנוכחות המולקולה המסמנת הקטנה אינוזיטול הקסא-פוספט (InsP6). ממצא זה קבע את SpXpr1 כתעלה אמתית המאפשרת ליון הפוספט לעבור ושניתנת לכוונון על ידי שליחים מבוססי אינוזיטול.
שני שערים לאורך מסלול משותף
כדי להבין את פעולת SpXpr1 ברמת האטום, המחברים השתמשו בקריו־אלקטרון מיקרוסקופיה וקבעו את המבנה שלו בהיעדר ובנוכחות InsP6. כל יחידת SpXpr1 מהווה חלק מרכבה זוגית בממברנה ומכילה ליבת נשיאה חיצונית ודומיין רגולאטורי פנימי. לאורך הנתיב המרכזי הם הבחינו בשני מקומות מובחנים בהם פוספט יכול לשבת, המתואמים על ידי חומצות אמינו טעונות חיובית; אתרים אלו שמורים גם בעמיתים האנושיים והצמחיים, מה שמצביע על תבנית משותפת לזיהוי הפוספט עצמו. עם זאת, בשונה מבני משפחתו, החלבון השמרי בונה שני שערים פיזיים בתוך נתיב זה. בפנים, מקטע גמיש שנקרא לולאת N, שמגובה על ידי הליקס קצר סמוך וסוף מוארך של אחד מההליקסים החוצים ממברנה, מתקפל אל תוך פתח הנקבוב וחותם על כניסת הפוספט. בחלק החיצוני, לולאה קטנה בין שני הליקסים יוצרת פקק שסוגר את היציאה. מוטציות או קיצוץ של אחד מהשערים הללו גרמו לדליפה מוגברת של פוספט, ואישרו כי הם בדרך כלל מחזיקים את החלבון במצב עצור עצמי, סגור.
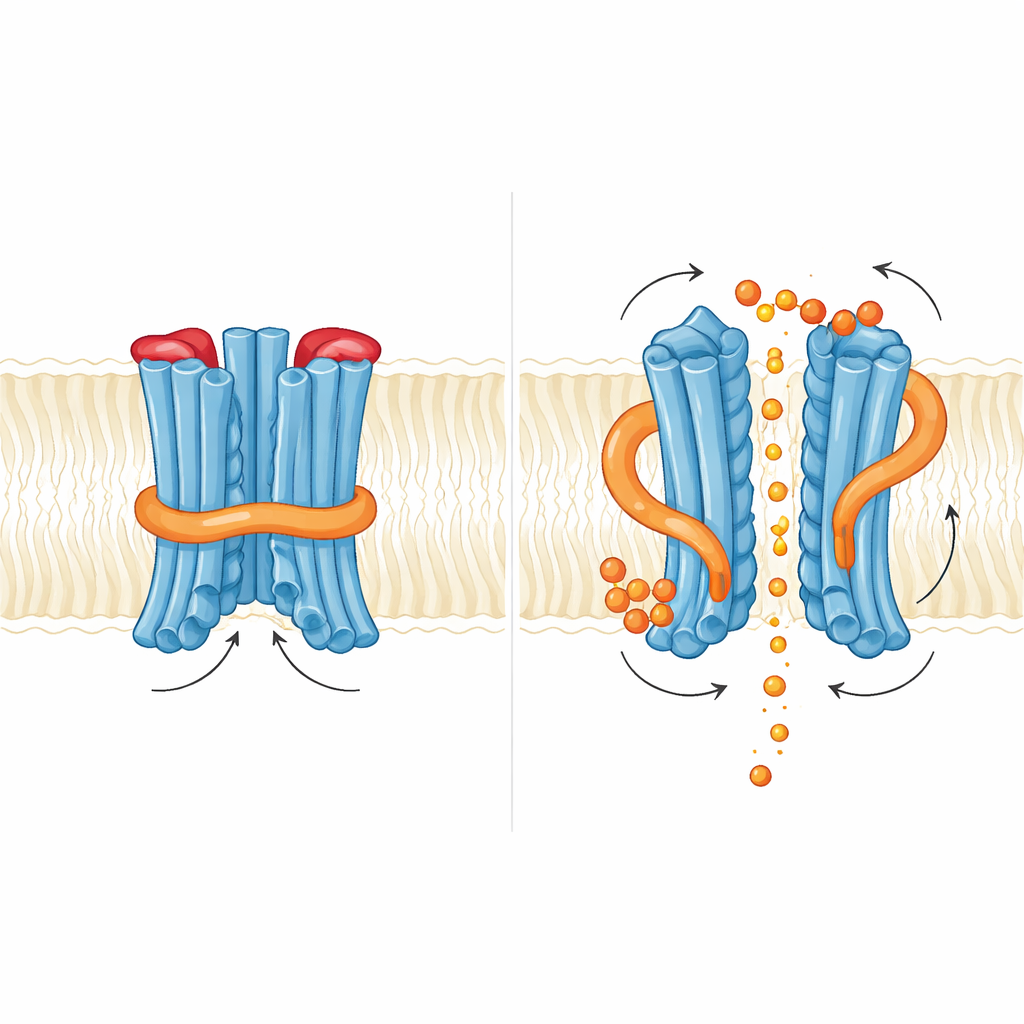
כיצד שליח קטן מזיז את השערים
הצוות חקר לאחר מכן מה קורה כאשר InsP6 נקשר. הם מצאו שני כיסי קשירה עשירים בחומצות בסיסיות: אחד במקום שבו הדומיין הרגולאטורי פוגש את ליבת הממברנה, ואחד בממשק בין שני הדומיינים הרגולאטוריים בדימר. קשירת InsP6 גרמה לסיבוב עדין של האזור הרגולאטורי ולחוסר יציבות של ההליקס הקצר שתומך בלולאת N, אך הלולאה עצמה עדיין ישבה בדרך של הפוספט במבנים שנתפסו. מבחינה פונקציונלית, הוספת InsP6 הגדילה את זרמי הפוספט, אבל מוטציות שהחלישו קשירת InsP6 לא ביטלו את הייצוא ולעתים אף הגבירו אותו. ממצא זה מרמז שבשמרים השליח המבוסס אינוזיטול פועל יותר כמתאם דק שמרחל את המנעול הפנימי מאשר כמתג דלוק־פתוח. המחברים מציעים כי אינוזיטול פיאופוספטים בעלי מטען גבוה יותר, כגון InsP7 או InsP8, עלולים להיות הטריגרים הפיזיולוגיים האמיתיים שיכולים להזיז במלואם גם את שער לולאת N הפנימי וגם את הפקק החיצוני מהמקום.
מה המשמעות מעבר לשמרים
ביחד, הניסויים המבניים והפונקציונליים הללו תומכים במודל פעיל שבו SpXpr1 בדרך כלל יושב במצב נעול כפול, עם שער פנימי וחיצוני השומרים על מסלול הפוספט. עלייה ברמות האותות המבוססים על אינוזיטול שנוצרים בעת עודף פוספט משחררת בהדרגה את המנעולים הללו, ומאפשרת לפוספט לזרום החוצה ולהגן על התא. בהשוואה למייצא האנושי, שמשתמש במקטע ניתן להזזה שונה כדי לחסום ולפתוח את הנקבוב שלו, הפתרון השמרי מדגים כיצד האבולוציה יכולה לשכתב את אותו שלד בסיסי כדי להתאים לאורחות חיים שונות — שימור קשוח בפטריות אל מול ייצוא מהיר ביונקים. הבנת עקרונות העיצוב הללו יכולה לסייע לחוקרים לכוונן שימוש בפוספט בגידולים, לעצב תרופות נגד פטריות שמפריעות לבקרת הפוספט הפטרייתית, ולהבין טוב יותר שינויים במחלתיים בחלבון XPR1 האנושי.
ציטוט: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
מילות מפתח: הומאוסטזיס של פוספט, תעלות יוניים, מבנה בקריו-EM, אינוזיטול פוליפוספטים, העברת ממברנה