Clear Sky Science · sv
Strukturella insikter i grindmekanismen hos fissionjästens fosfatexportör SpXpr1
Varför små portar för fosfat spelar roll
Varje cell måste noggrant balansera fosfat, en liten men oumbärlig komponent i molekyler som DNA, membraner och cellens energivaluta. För lite fosfat hämmar tillväxten; för mycket kan vara giftigt. Denna studie undersöker hur fissionjäst, en modellsvamp, pressar ut överskott av fosfat ur cellen genom en molekylär port kallad SpXpr1. Genom att avslöja portens tredimensionella struktur och hur den öppnas och stängs, belyser arbetet hur mycket olika organismer — från svampar till människor — använder besläktade proteiner för att hålla fosfatnivåerna i schack, med följder för hjärnsjukdomar, njurhälsa, jordbruk och antifungala strategier.
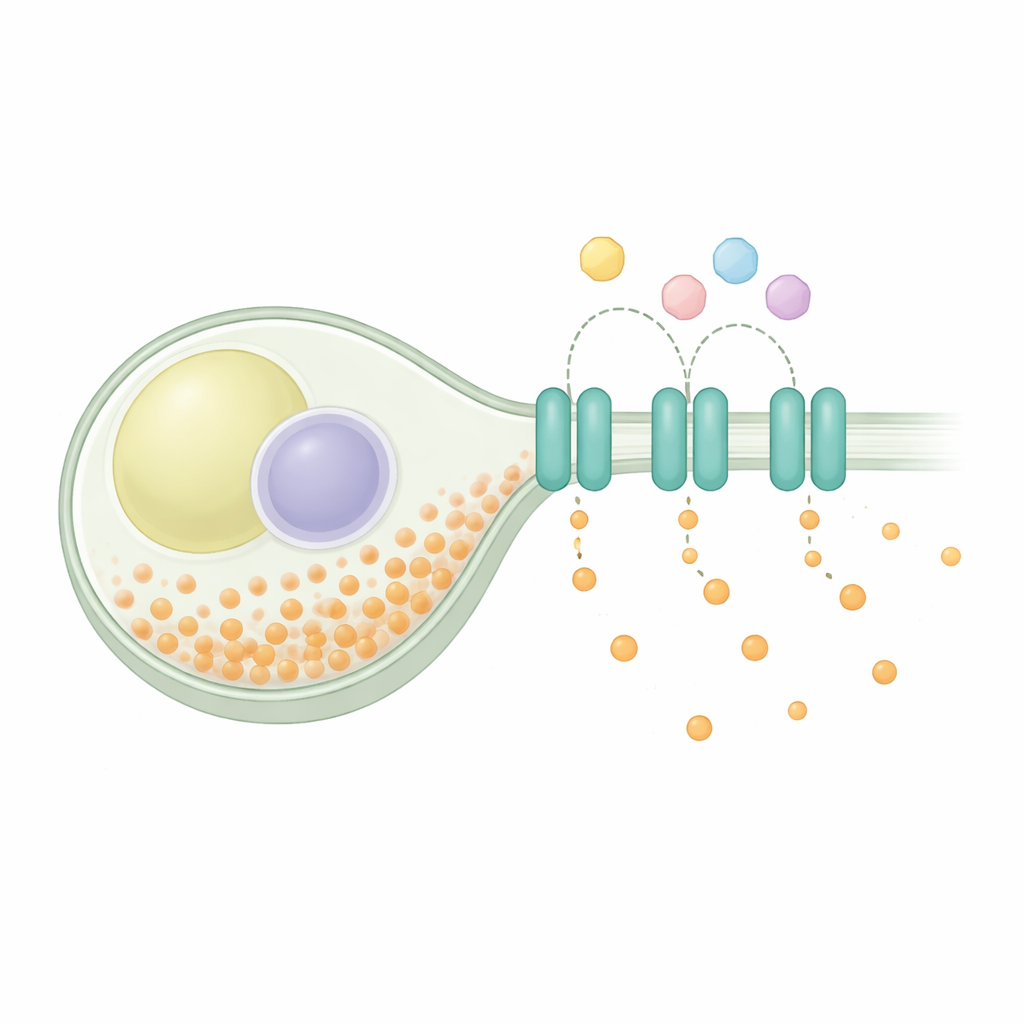
Att hålla balansen inne i en cell
Fosfathomeostas är ett universellt problem: celler måste ta upp fosfat för metabolism och byggstenar, lagra en del säkert och exportera eventuellt överskott. I fissionjäst slås upptagssystem på vid brist och av vid överflöd, medan ett lagringskomplex packar överskott till långa kedjor. Genetiska studier hade pekat på att ett protein kallat SpXpr1 fungerar som en dedikerad exportör och hjälper till att förhindra farlig överbelastning när lagringsvägar är komprometterade. SpXpr1 tillhör XPR1-familjen av exportörer som finns i eukaryoter, inklusive växter och människor, där besläktade proteiner kopplats till sjukdomar som hjärnkalcifiering och njurdysfunktion. Trots detta gemensamma familjebakgrund var det oklart om jästversionen fungerade på samma sätt som det mänskliga proteinet.
Se proteinet och bevisa att det är en kanal
Forskarna testade först om SpXpr1 verkligen förflyttar fosfat över membran. De satte in jästproteinet i humana celler där det egna XPR1 var borttaget och mätte sedan hur mycket fosfat som läckte ut i omgivande lösning. Celler med SpXpr1 exporterade mer fosfat än kontrollceller, vilket bekräftade dess aktivitet, även om det var mindre effektivt än den mänskliga exportören. Med hjälp av elektriska registreringar visade gruppen att celler med SpXpr1 uppvisade fosfatberoende strömmar som ökade när den lilla signalmolekylen inositolhexakisfosfat (InsP6) fanns närvarande. Det etablerade SpXpr1 som en äkta kanal som tillåter fosfationen att passera och som kan justeras av inositolhaltiga budbärare.
Två dörrar längs en gemensam väg
För att förstå hur SpXpr1 fungerar på atomnivå använde författarna kryo-elektronmikroskopi för att bestämma dess struktur i frånvaro och närvaro av InsP6. Varje SpXpr1-enhet ingår i ett parvis montage i membranet och innehåller en yttre transportkärna och en inre regleringsdomän. Längs den centrala vägen observerade de två distinkta platser där fosfat kan sitta, koordinerade av positivt laddade aminosyror; dessa platser är bevarade i mänskliga och växtmotsvarigheter, vilket framhäver en gemensam ritning för hur fosfat självt känns igen. Dock, till skillnad från sina släktingar, bygger jästproteinet in två fysiska grindar i denna väg. På insidan veckar ett flexibelt segment kallat N-loopen, stödd av en närliggande kort helix och av en utsträckt ände av en membranpasserande helix, in i porens ingång och blockerar fosfat från att komma in. På utsidan bildar en liten loop mellan två helixar en plugg som täcker utloppet. Mutationer eller avkapning av någon av dessa grindar gjorde att kanalen läckte mer fosfat, vilket bekräftar att de normalt håller proteinet i ett själv-hämmande, stängt tillstånd.
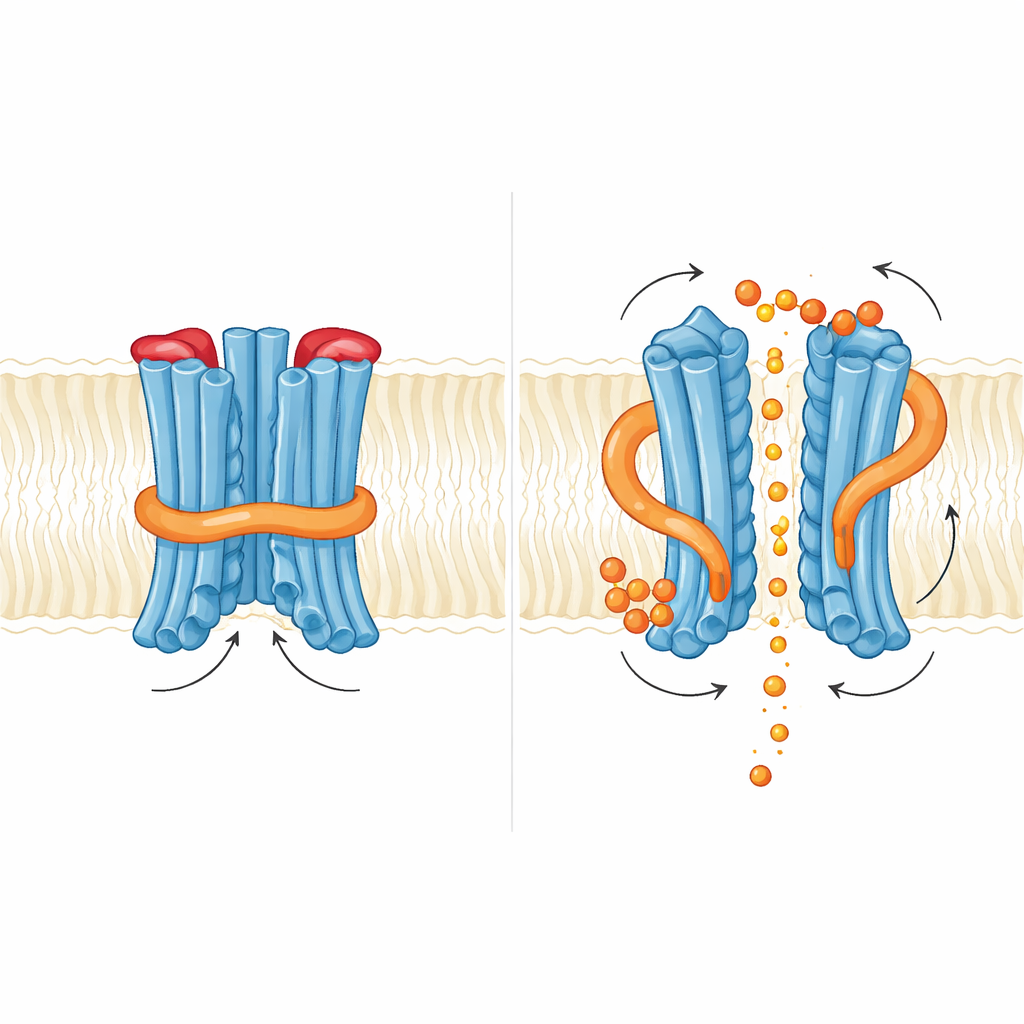
Hur en liten budbärare knuffar grindarna
Gruppen undersökte sedan vad som händer när InsP6 binder. De fann två bindningsfickor rika på basiska rester: en där regleringsdomänen möter membrankärnan, och en annan vid gränsytan mellan de två regleringsdomänerna i dimeren. InsP6-bindning orsakade en subtil rotation av regleringsregionen och destabliserade den korta helix som stöder N-loopen, men loopen själv låg fortfarande i vägen för fosfat i de fångade strukturerna. Funktionellt ökade tillsats av InsP6 fosfatströmmarna, men mutationer som försvagade InsP6-bindningen avskaffade inte exporten och förstärkte ibland den till och med. Detta tyder på att inositolbudbäraren i jäst fungerar mer som en finjusterare som lossar ett inre lås än som en av/på-strömbrytare. Författarna föreslår att högre negativt laddade inositolpyrofosfater, såsom InsP7 eller InsP8, kan vara de verkliga fysiologiska utlösarna som fullt ut kan rubba både den inre N-loop-grinden och den yttre pluggen ur vägen.
Vad detta betyder bortom jäst
Tillsammans stöder dessa strukturella och funktionella experiment en arbetshypotes där SpXpr1 normalt sitter i ett dubbellåst tillstånd, med en inre och en yttre grind som bevakar fosfatvägen. Stegande nivåer av inositolbaserade signaler som produceras vid fosfatoverflöd släpper gradvis dessa lås, vilket tillåter fosfat att strömma ut och skydda cellen. Jämfört med den mänskliga exportören, som använder ett annat rörligt segment för att täppa till och öppna sin por, visar jästlösningen hur evolutionen kan omkoppla samma grundläggande stomme för att passa olika livsstilar — strikt konservativ i svampar kontra snabb export i däggdjur. Förståelse för dessa designprinciper kan hjälpa forskare att justera fosfatanvändning i grödor, designa riktade antifungala läkemedel som stör svampens fosfatkontroll och bättre tolka sjukdomsframkallande förändringar i det mänskliga XPR1-proteinet.
Citering: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
Nyckelord: fosfathomeostas, jonkanaler, kryo-EM-struktur, inositolfosfater, membrantransport