Clear Sky Science · de
Strukturelle Einblicke in den Schaltmechanismus des Phosphat-Exporters SpXpr1 der Spaltpilze
Warum winzige Tore für Phosphat wichtig sind
Jede Zelle muss Phosphat sorgfältig austarieren – ein kleines, aber unverzichtbares Baustein in Molekülen wie DNA, Membranen und der zellulären Energiewährung. Zu wenig Phosphat bremst Wachstum; zu viel kann toxisch sein. Diese Studie untersucht, wie die Spalthefe, ein Modellpilz, überschüssiges Phosphat durch eine molekulare Pforte namens SpXpr1 aus der Zelle hinaustransportiert. Indem sie die dreidimensionale Struktur dieser Pforte und ihren Öffnungs- und Schließmechanismus aufklärt, beleuchtet die Arbeit, wie sehr unterschiedliche Organismen – von Pilzen bis zu Menschen – verwandte Proteine nutzen, um Phosphatspiegel zu regulieren. Das hat Bedeutung für Hirnerkrankungen, Nierenfunktionen, Landwirtschaft und Strategien gegen Pilzinfektionen.
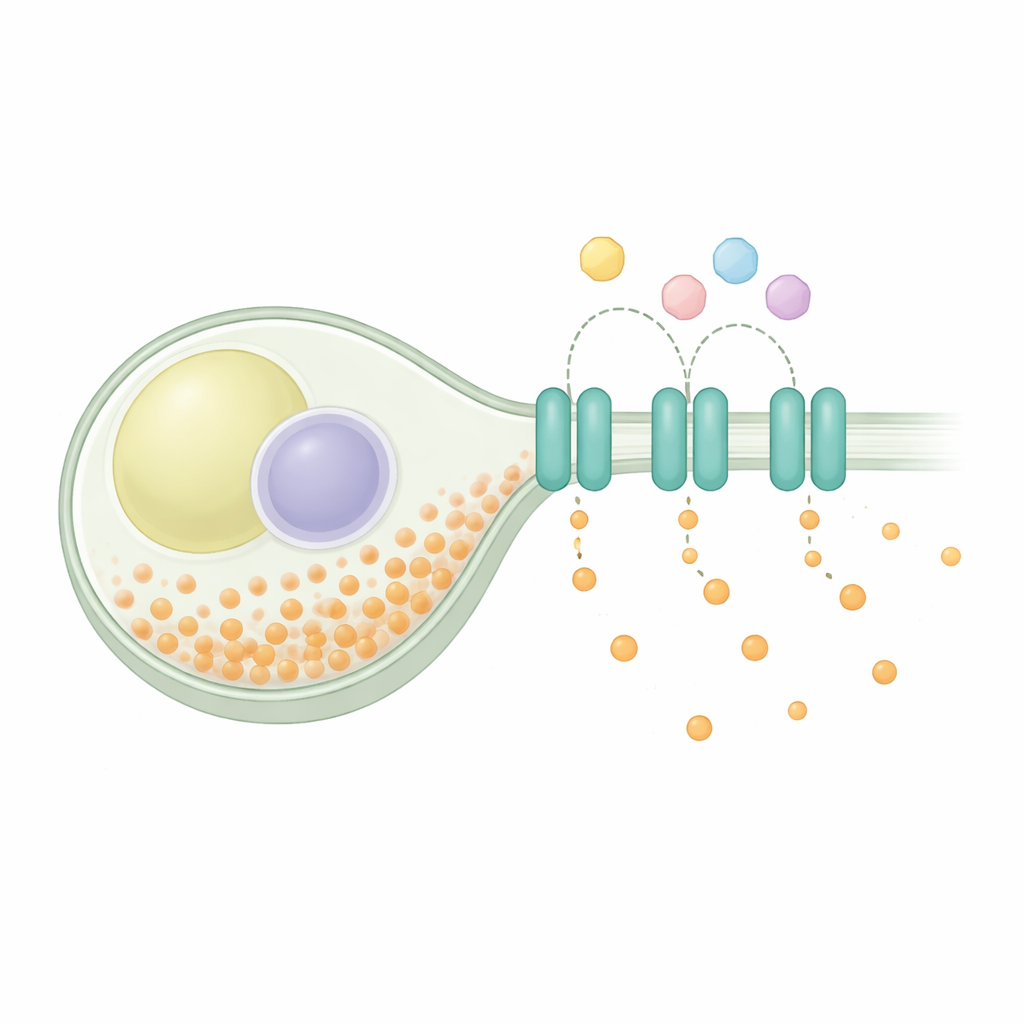
Das innere Gleichgewicht der Zelle bewahren
Phosphat-Homöostase ist ein universelles Problem: Zellen müssen Phosphat für Stoffwechsel und Baustoffe aufnehmen, einen Teil sicher speichern und Überschuss wieder exportieren. Bei der Spalthefe schalten Aufnahmesysteme bei Knappheit ein und bei Fülle ab, während ein Speicherkomplex überschüssiges Phosphat in langen Ketten bindet. Genetische Studien deuteten darauf hin, dass ein Protein namens SpXpr1 als spezialisierter Exporter wirkt und Überladung verhindert, wenn Speicherwege gestört sind. SpXpr1 gehört zur XPR1-Familie von Exportproteinen, die bei Eukaryoten weit verbreitet sind, auch in Pflanzen und Menschen, wo verwandte Proteine mit Erkrankungen wie Hirnverkalkung und Nierenfunktionsstörungen in Verbindung gebracht werden. Trotz dieser familiären Gemeinsamkeit war unklar, ob die Hefe‑Version genauso arbeitet wie das menschliche Protein.
Das Protein sichtbar machen und beweisen, dass es ein Kanal ist
Die Forscher prüften zunächst, ob SpXpr1 tatsächlich Phosphat über Membranen transportiert. Sie setzten das Hefenprotein in menschliche Zellen ein, deren eigenes XPR1 entfernt worden war, und maßen, wie viel Phosphat in die umgebende Lösung gelangte. Zellen mit SpXpr1 exportierten mehr Phosphat als Kontrollzellen, womit die Aktivität bestätigt wurde, wenn auch mit geringer Effizienz im Vergleich zum menschlichen Exporter. Mithilfe elektrischer Messungen zeigten die Autoren dann, dass Zellen mit SpXpr1 phosphatabhängige Ströme aufwiesen, die zunahmen, wenn das kleine Signalmolekül Inositolhexakisphosphat (InsP6) vorhanden war. Das etablierte SpXpr1 als echten Kanal, der Phosphationen passieren lässt und durch inositolhaltige Botenstoffe moduliert werden kann.
Zwei Tore entlang eines gemeinsamen Pfads
Um zu verstehen, wie SpXpr1 auf atomarer Ebene funktioniert, bestimmten die Autoren seine Struktur mittels Kryo‑Elektronenmikroskopie in Abwesenheit und Anwesenheit von InsP6. Jede SpXpr1‑Einheit bildet Teil eines dimeren Assemblats in der Membran und enthält einen äußeren Transportkern sowie eine innere regulatorische Domäne. Entlang des zentralen Pfads beobachteten sie zwei unterschiedliche Stellen, an denen Phosphat binden kann, koordiniert durch positiv geladene Aminosäuren; diese Bindestellen sind in menschlichen und pflanzlichen Gegenstücken konserviert und zeigen einen gemeinsamen Bauplan zur Erkennung des Phosphats. Im Gegensatz zu Verwandten baut das Hefaprotein jedoch zwei physische Sperren in diesen Pfad ein. Im Inneren faltet sich ein flexibler Abschnitt, die sogenannte N‑Schleife, gestützt von einer nahegelegenen kurzen Helix und einem verlängerten Ende einer membranüberspannenden Helix, in den Poreneingang und blockiert so das Eindringen von Phosphat. Außen bildet eine kleine Schleife zwischen zwei Helices einen Pfropfen, der den Ausgang verschließt. Mutationen oder Kürzungen an einer dieser Sperren führten zu stärkerem Phosphatleck, was bestätigt, dass sie das Protein normalerweise in einem selbst‑inhibierten, geschlossenen Zustand halten.
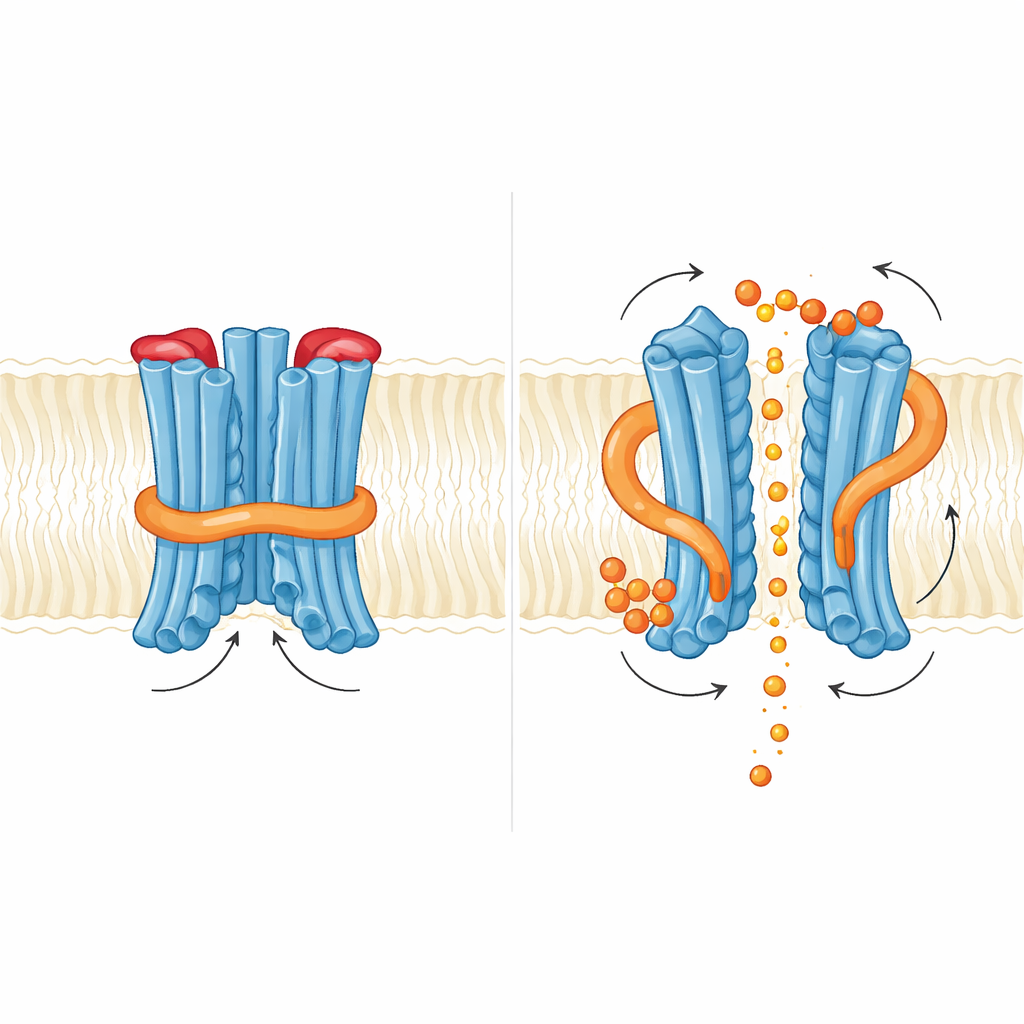
Wie ein kleiner Bote die Tore anstößt
Die Gruppe untersuchte anschließend, was beim Binden von InsP6 passiert. Sie fanden zwei Bindetaschen, reich an basischen Resten: eine dort, wo die regulatorische Domäne auf den Membrankern trifft, und eine weitere an der Schnittstelle zwischen den beiden regulatorischen Domänen im Dimer. InsP6‑Bindung bewirkte eine subtile Rotation der regulatorischen Region und destabilisierte die kurze Helix, die die N‑Schleife abstützt; die Schleife selbst blockierte jedoch in den erfassten Strukturen weiterhin den Phosphatweg. Funktionell erhöhte die Zugabe von InsP6 die Phosphatströme, doch Mutationen, die die InsP6‑Bindung schwächten, beseitigten den Export nicht und verstärkten ihn teils sogar. Das deutet darauf hin, dass der Inositol‑Botenstoff in der Hefe eher als Feineinsteller wirkt, der ein internes Schloss lockert, statt als einfacher Ein‑Aus‑Schalter. Die Autoren schlagen vor, dass höher geladenen Inositol‑Pyrophosphate wie InsP7 oder InsP8 die eigentlichen physiologischen Auslöser sein könnten, die beide Sperren – die innere N‑Schleife und den äußeren Pfropfen – vollständig aus dem Weg räumen.
Was das über die Hefe hinaus bedeutet
Zusammen stützen diese strukturellen und funktionellen Experimente ein Modell, in dem SpXpr1 normalerweise in einem doppelt verriegelten Zustand sitzt, mit innerer und äußerer Sperre, die den Phosphatpfad schützen. Steigende Spiegel inositolbasierter Signale, die bei Phosphatüberschuss entstehen, lösen diese Schlösser allmählich und erlauben so den Phosphatfluss nach außen zum Schutz der Zelle. Im Vergleich zum menschlichen Exporter, der ein anderes bewegliches Segment nutzt, um seine Pore zu verschließen und zu öffnen, zeigt die Hefelösung, wie die Evolution dasselbe Grundgerüst umbauen kann, um verschiedenen Lebensweisen gerecht zu werden – strikte Erhaltung bei Pilzen gegenüber schnellem Export bei Säugetieren. Das Verständnis dieser Gestaltungsprinzipien könnte Forschern helfen, die Phosphatnutzung in Nutzpflanzen zu optimieren, gezielte Antimykotika zu entwickeln, die die pilzliche Phosphatkontrolle stören, und krankheitsverursachende Veränderungen im menschlichen XPR1‑Protein besser zu interpretieren.
Zitation: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
Schlüsselwörter: Phosphat-Homöostase, Ionenkanäle, cryo-EM-Struktur, Inositol-Polyphosphate, Membrantransport