Clear Sky Science · fr
Perspectives structurelles sur le mécanisme d’ouverture du transporteur de phosphate de la levure de fission SpXpr1
Pourquoi de petites portes pour le phosphate comptent
Chaque cellule doit équilibrer soigneusement le phosphate, un ingrédient minuscule mais indispensable présent dans des molécules comme l’ADN, les membranes et la monnaie énergétique de la cellule. Une carence en phosphate bloque la croissance ; un excès peut être toxique. Cette étude examine comment la levure de fission, un champignon modèle, expulse l’excès de phosphate hors de la cellule via une porte moléculaire appelée SpXpr1. En révélant la structure tridimensionnelle de cette porte et son mode d’ouverture et de fermeture, le travail éclaire la façon dont des organismes très différents — des champignons aux humains — utilisent des protéines apparentées pour maintenir l’équilibre en phosphate, avec des implications pour les maladies cérébrales, la santé rénale, l’agriculture et les stratégies antifongiques.
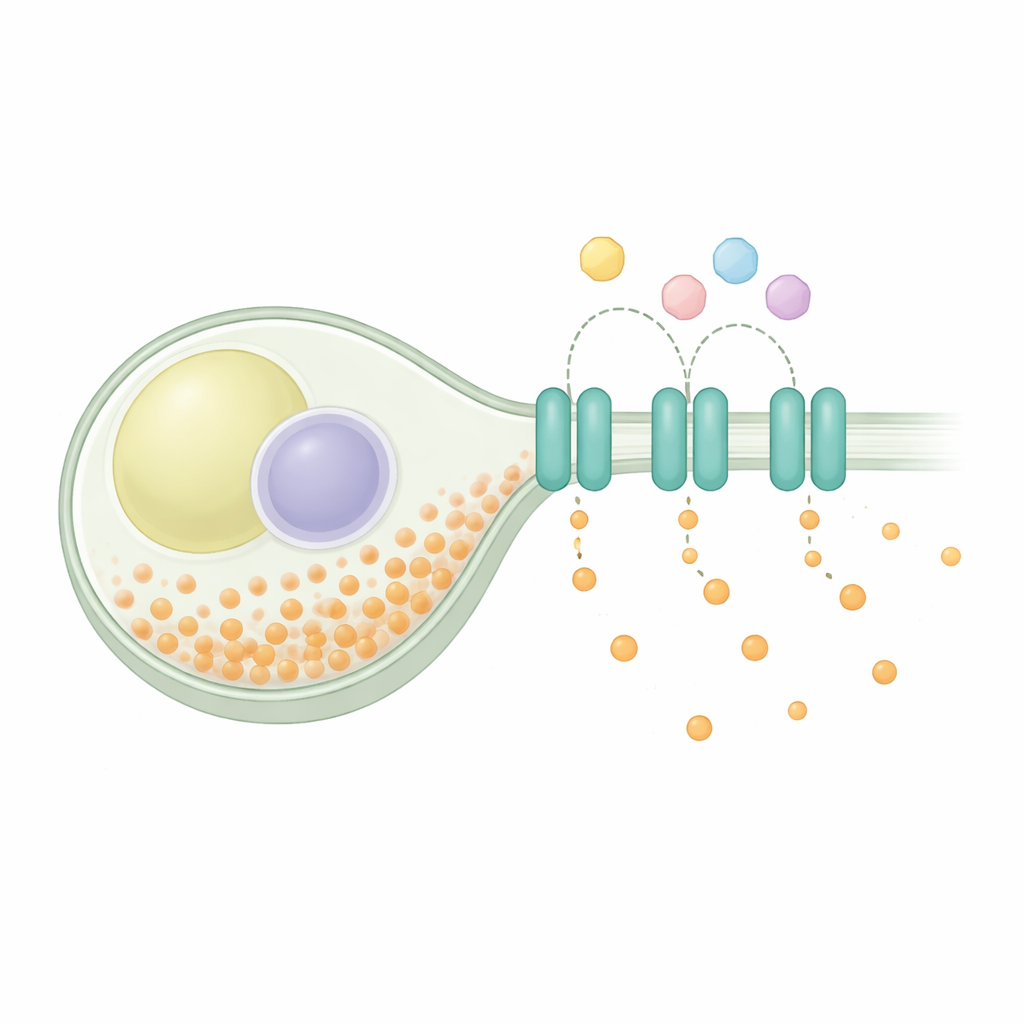
Maintenir l’équilibre à l’intérieur d’une cellule
L’homéostasie du phosphate est un problème universel : les cellules doivent importer du phosphate pour le métabolisme et la synthèse des constituants, en stocker une partie de façon sûre et exporter tout excès. Chez la levure de fission, les systèmes d’import s’activent en cas de rareté et se ferment quand le phosphate est abondant, tandis qu’un complexe de stockage empaquette l’excès en longues chaînes. Des études génétiques avaient suggéré qu’une protéine nommée SpXpr1 agit comme un exporteur dédié, aidant à prévenir une surcharge dangereuse lorsque les voies de stockage sont compromises. SpXpr1 appartient à la famille XPR1 d’exporteurs présente chez les eucaryotes, y compris les plantes et les humains, où des protéines apparentées sont impliquées dans des troubles comme la calcification cérébrale et des dysfonctionnements rénaux. Malgré cet héritage commun, on ignorait si la version de la levure fonctionnait de la même manière que la protéine humaine.
Voir la protéine et prouver qu’il s’agit d’un canal
Les chercheurs ont d’abord testé si SpXpr1 déplace réellement le phosphate à travers les membranes. Ils ont inséré la protéine de levure dans des cellules humaines dont l’XPR1 avait été supprimé, puis mesuré la quantité de phosphate libérée dans le milieu. Les cellules exprimant SpXpr1 exportaient davantage de phosphate que les témoins, confirmant son activité, bien que moins efficace que l’exporteur humain. Par des enregistrements électriques, l’équipe a ensuite montré que les cellules porteuses de SpXpr1 présentaient des courants dépendants du phosphate qui augmentaient en présence de la petite molécule de signalisation inositol hexakisphosphate (InsP6). Cela établit SpXpr1 comme un véritable canal laissant passer des ions phosphate et pouvant être modulé par des messagers contenant de l’inositol.
Deux portes le long d’un même chemin
Pour comprendre le fonctionnement atomique de SpXpr1, les auteurs ont utilisé la cryo-microscopie électronique pour déterminer sa structure en l’absence et en présence d’InsP6. Chaque unité de SpXpr1 fait partie d’un assemblage dimérique dans la membrane et contient un cœur de transport externe et un domaine régulateur interne. Le long du trajet central, ils ont observé deux emplacements distincts où le phosphate peut se stabiliser, coordonné par des acides aminés chargés positivement ; ces sites sont conservés chez les homologues humains et végétaux, soulignant un plan partagé pour la reconnaissance du phosphate lui-même. Pourtant, contrairement à ses apparentés, la protéine de levure incorpore deux verrous physiques dans ce chemin. À l’intérieur, un segment flexible appelé boucle N, soutenu par une courte hélice voisine et par l’extrémité étendue d’une hélice transmembranaire, se replie dans l’entrée du pore et empêche le phosphate d’entrer. À l’extérieur, une petite boucle entre deux hélices forme un bouchon qui coiffe la sortie. Muter ou tronquer l’un ou l’autre de ces verrous provoquait une fuite accrue de phosphate, confirmant qu’ils maintiennent normalement la protéine dans un état auto-inhibé, fermé.
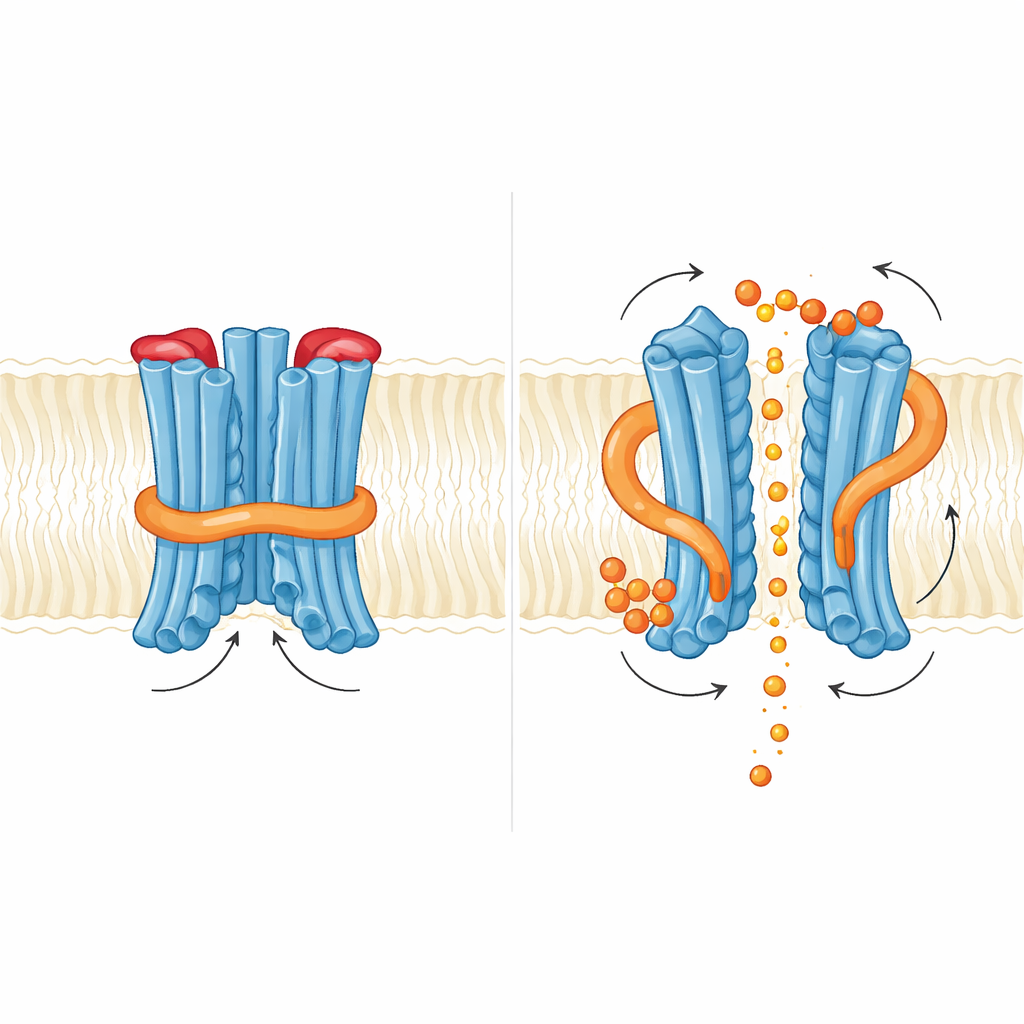
Comment un petit messager pousse sur les verrous
L’équipe a ensuite examiné ce qui se passe lorsque l’InsP6 se lie. Ils ont identifié deux poches de liaison riches en résidus basiques : l’une où le domaine régulateur rencontre le cœur membranaire, et l’autre à l’interface entre les deux domaines régulateurs du dimère. La fixation d’InsP6 entraînait une rotation subtile de la région régulatrice et déstabilisait la courte hélice qui soutient la boucle N, mais la boucle elle-même restait en position bloquant le passage du phosphate dans les structures capturées. Sur le plan fonctionnel, l’ajout d’InsP6 augmentait les courants de phosphate, mais des mutations affaiblissant la liaison à l’InsP6 n’abolissaient pas l’export et pouvaient parfois même l’augmenter. Cela suggère que, chez la levure, le messager inositol agit plutôt comme un réglage fin qui desserre une serrure interne que comme un interrupteur marche/arrêt. Les auteurs proposent que des inositol pyrophosphates plus chargés, tels qu’InsP7 ou InsP8, pourraient être les véritables déclencheurs physiologiques capables de dégager complètement à la fois la porte interne de la boucle N et le bouchon externe.
Ce que cela signifie au-delà de la levure
Ensemble, ces expériences structurelles et fonctionnelles soutiennent un modèle opérationnel dans lequel SpXpr1 se tient normalement en état à double verrouillage, avec une porte intérieure et une porte extérieure protégeant le passage du phosphate. L’élévation des signaux à base d’inositol produite lors d’un excès de phosphate relâche progressivement ces verrous, permettant au phosphate de s’écouler et protégeant la cellule. Par rapport à l’exporteur humain, qui utilise un segment mobile différent pour boucher et déboucher son pore, la solution de la levure montre comment l’évolution peut reconfigurer le même échafaudage de base pour s’adapter à des modes de vie différents — conservation stricte chez les champignons contre exportation rapide chez les mammifères. Comprendre ces principes de conception pourrait aider les chercheurs à moduler l’utilisation du phosphate dans les cultures, concevoir des antifongiques ciblés perturbant le contrôle fongique du phosphate et mieux interpréter les variations pathogènes de la protéine XPR1 humaine.
Citation: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
Mots-clés: homéostasie du phosphate, canaux ioniques, structure cryo-EM, inositol polyphosphates, transport membranaire