Clear Sky Science · pt
Percepções estruturais sobre o mecanismo de abertura do exportador de fosfato da levedura de fissão SpXpr1
Por que portas minúsculas para fosfato importam
Toda célula precisa equilibrar cuidadosamente o fosfato, um componente pequeno, mas indispensável em moléculas como DNA, membranas e na moeda energética da célula. Pouco fosfato impede o crescimento; excesso pode ser tóxico. Este estudo investiga como a levedura de fissão, um fungo modelo, expulsa o excesso de fosfato da célula por meio de uma porta molecular chamada SpXpr1. Ao revelar a estrutura tridimensional dessa porta e como ela se abre e fecha, o trabalho esclarece como organismos muito diferentes — de fungos a humanos — usam proteínas relacionadas para manter os níveis de fosfato sob controle, com implicações para doenças cerebrais, saúde renal, agricultura e estratégias antifúngicas.
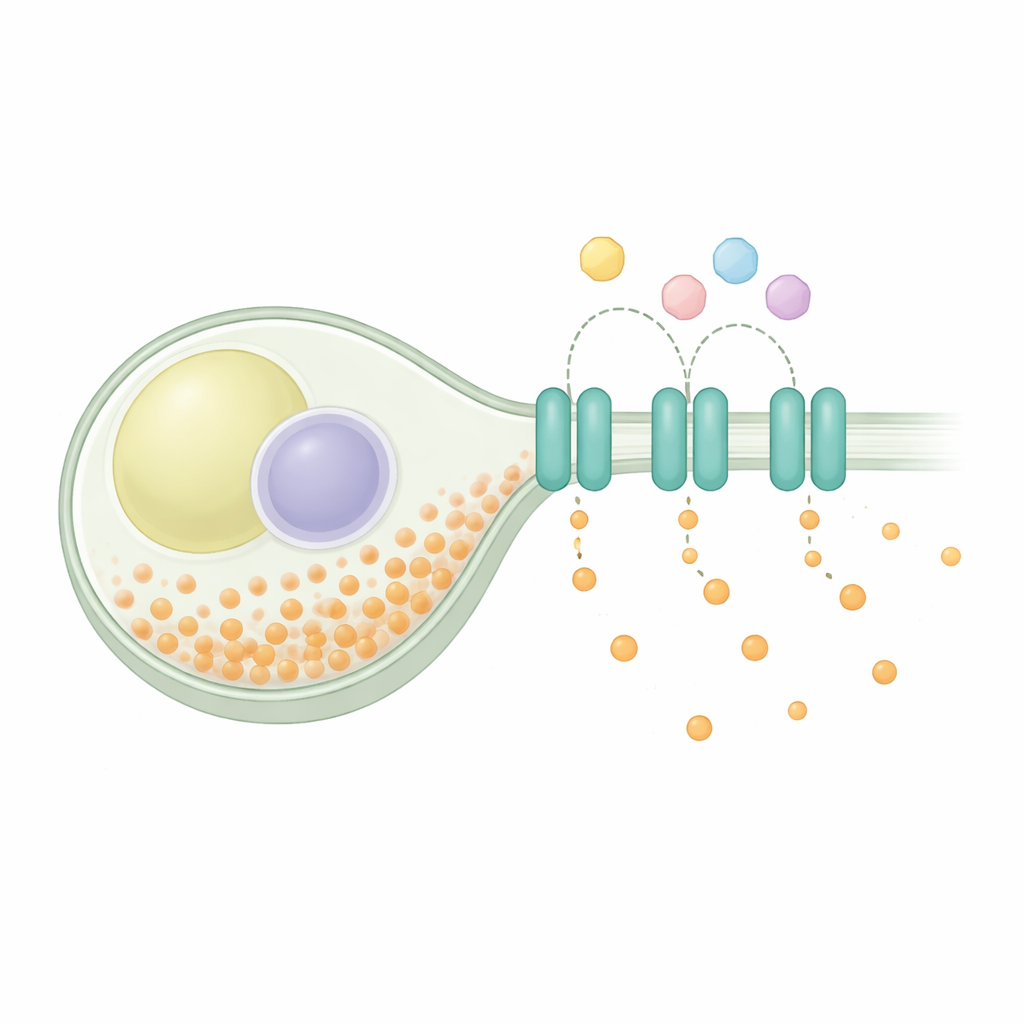
Manter o equilíbrio dentro da célula
A homeostase do fosfato é um problema universal: as células devem importar fosfato para o metabolismo e para blocos de construção, armazenar parte dele com segurança e exportar qualquer excedente. Na levedura de fissão, os sistemas de captação são ativados em escassez e desligados quando o fosfato é abundante, enquanto um complexo de armazenamento empacota o excesso em cadeias longas. Estudos genéticos sugeriam que uma proteína chamada SpXpr1 atua como exportadora dedicada, ajudando a evitar sobrecarga perigosa quando as vias de armazenamento estão comprometidas. A SpXpr1 pertence à família XPR1 de exportadores encontrada em eucariotos, incluindo plantas e humanos, onde proteínas relacionadas estão associadas a distúrbios como calcificação cerebral e disfunção renal. Apesar desse parentesco familiar, não estava claro se a versão de levedura funcionava da mesma forma que a proteína humana.
Ver a proteína e provar que ela é um canal
Os pesquisadores primeiro testaram se a SpXpr1 realmente transporta fosfato através de membranas. Inseriram a proteína de levedura em células humanas com seu próprio XPR1 removido e, em seguida, mediram quanto fosfato vazava para a solução ao redor. Células com SpXpr1 exportaram mais fosfato que células controle, confirmando sua atividade, embora com menor eficiência que o exportador humano. Usando registros elétricos, a equipe mostrou que células contendo SpXpr1 exibiam correntes dependentes de fosfato que aumentavam na presença da pequena molécula sinalizadora inositol hexafosfato (InsP6). Isso estabeleceu a SpXpr1 como um canal legítimo que permite a passagem de íons fosfato e que pode ser modulada por mensageiros contendo inositol.
Duas portas ao longo de um mesmo caminho
Para entender como a SpXpr1 funciona ao nível atômico, os autores usaram crio-microscopia eletrônica para determinar sua estrutura na ausência e na presença de InsP6. Cada unidade de SpXpr1 faz parte de um arranjo pareado na membrana e contém um núcleo de transporte externo e um domínio regulatório interno. Ao longo do caminho central, observaram dois pontos distintos onde o fosfato pode se acomodar, coordenado por aminoácidos carregados positivamente; esses sítios são conservados em contrapartes humanas e vegetais, ressaltando um plano comum de reconhecimento do próprio fosfato. No entanto, ao contrário de seus parentes, a proteína de levedura constrói duas fechaduras físicas nesse caminho. Internamente, um segmento flexível chamado N-loop, apoiado por um curto hélice próxima e por uma extremidade alongada de uma hélice transmembrana, dobra-se na entrada do poro e bloqueia a entrada do fosfato. Externamente, um pequeno laço entre duas hélices forma uma tampa que sela a saída. Mutar ou aparar qualquer uma dessas portas fez o canal vazar mais fosfato, confirmando que elas normalmente mantêm a proteína num estado auto-inibido, fechado.
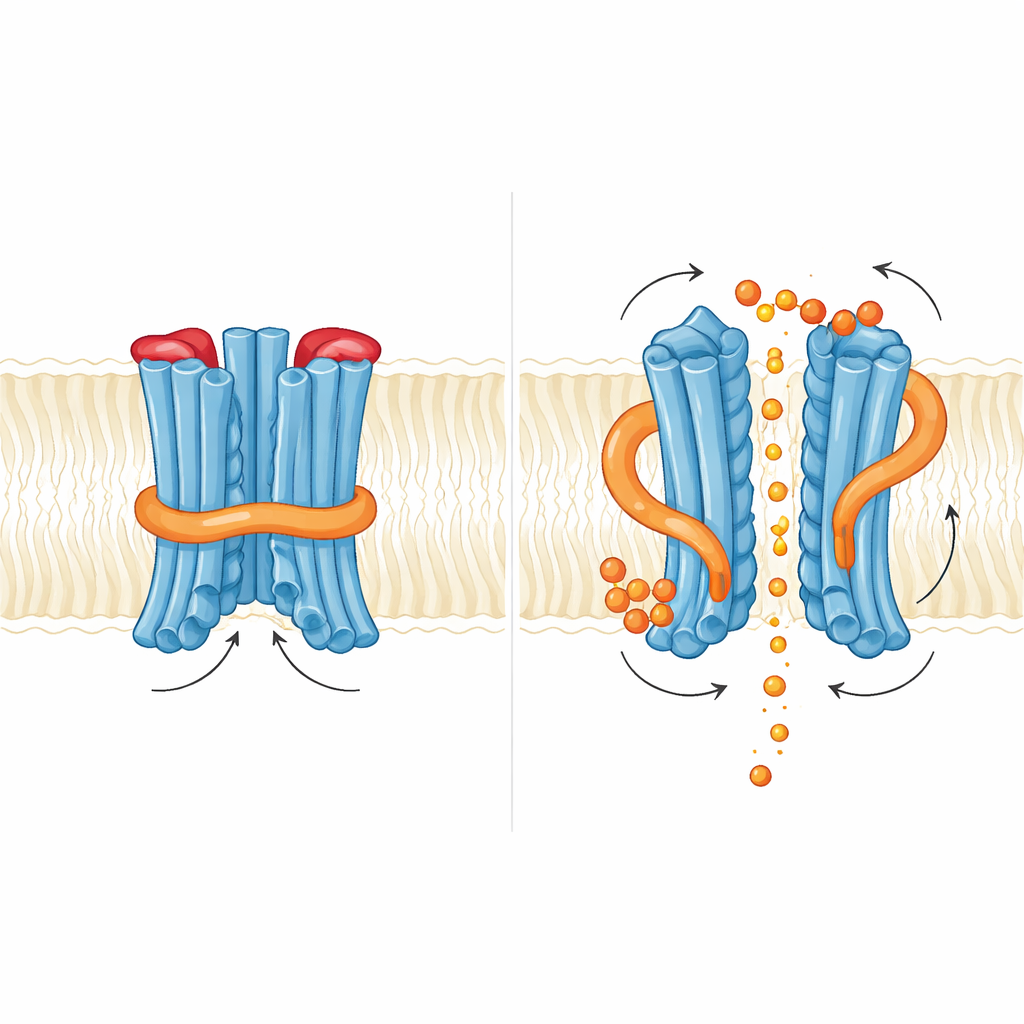
Como um pequeno mensageiro empurra as portas
A equipe então examinou o que acontece quando o InsP6 se liga. Eles encontraram dois bolsões de ligação ricos em resíduos básicos: um onde o domínio regulatório encontra o núcleo da membrana, e outro na interface entre os dois domínios regulatórios no dímero. A ligação do InsP6 causou uma rotação sutil da região regulatória e desestabilizou a pequena hélice que sustenta o N-loop, mas o próprio laço ainda permanecia no caminho do fosfato nas estruturas capturadas. Funcionalmente, adicionar InsP6 aumentou as correntes de fosfato, mas mutações que enfraqueciam a ligação ao InsP6 não aboliram a exportação e, às vezes, até a aumentaram. Isso sugere que, na levedura, o mensageiro inositol atua mais como um regulador fino que afrouxa uma trava interna do que como um interruptor liga-desliga. Os autores propõem que inositol pirofosfatos mais carregados, como InsP7 ou InsP8, podem ser os verdadeiros gatilhos fisiológicos capazes de deslocar completamente tanto a trava interna do N-loop quanto a tampa externa.
O que isso significa além da levedura
No conjunto, esses experimentos estruturais e funcionais apoiam um modelo de trabalho em que a SpXpr1 normalmente se encontra num estado de dupla trava, com uma porta interna e outra externa protegendo a via do fosfato. O aumento dos níveis de sinais à base de inositol produzidos durante o excesso de fosfato libera gradualmente essas travas, permitindo que o fosfato flua para fora e proteja a célula. Em comparação com o exportador humano, que usa um segmento móvel diferente para tampar e destampar seu poro, a solução encontrada na levedura mostra como a evolução pode reconfigurar o mesmo arcabouço básico para atender a estilos de vida diferentes — conservação rigorosa em fungos versus exportação rápida em mamíferos. Entender esses princípios de projeto pode ajudar pesquisadores a ajustar o uso de fosfato em culturas agrícolas, desenhar fármacos antifúngicos direcionados que perturbem o controle de fosfato em fungos e interpretar melhor alterações causadoras de doença na proteína humana XPR1.
Citação: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
Palavras-chave: homeostase de fosfato, canais iônicos, estrutura por crio-EM, inositol polifosfatos, transporte de membrana