Clear Sky Science · tr
Mayoz bölünme mayasında fosfat ihracatçısı SpXpr1’in kapı mekanizmasına yapısal bakış
Fosfat için küçük kapıların önemi
Her hücre, DNA, zarlar ve hücrenin enerji birimi gibi moleküllerin vazgeçilmez bileşeni olan küçük ama hayati bir unsur olan fosfatı dikkatle dengede tutmak zorundadır. Çok az fosfat büyümeyi durdurur; çok fazla ise toksik olabilir. Bu çalışma, model bir mantar olan mayoz bölünme mayasının (fission yeast) fazla fosfatı SpXpr1 adlı bir moleküler kapı aracılığıyla hücre dışına nasıl ittiğini inceliyor. Bu kapının üç boyutlu yapısını ve açılıp kapanma biçimini ortaya koyarak, mantarlardan insanlara kadar çok farklı organizmaların fosfat düzeylerini korumak için ilişkili proteinleri nasıl kullandığına dair ışık tutuyor; bunun beyin hastalıkları, böbrek sağlığı, tarım ve antifungal stratejiler açısından çıkarımları olabilir.
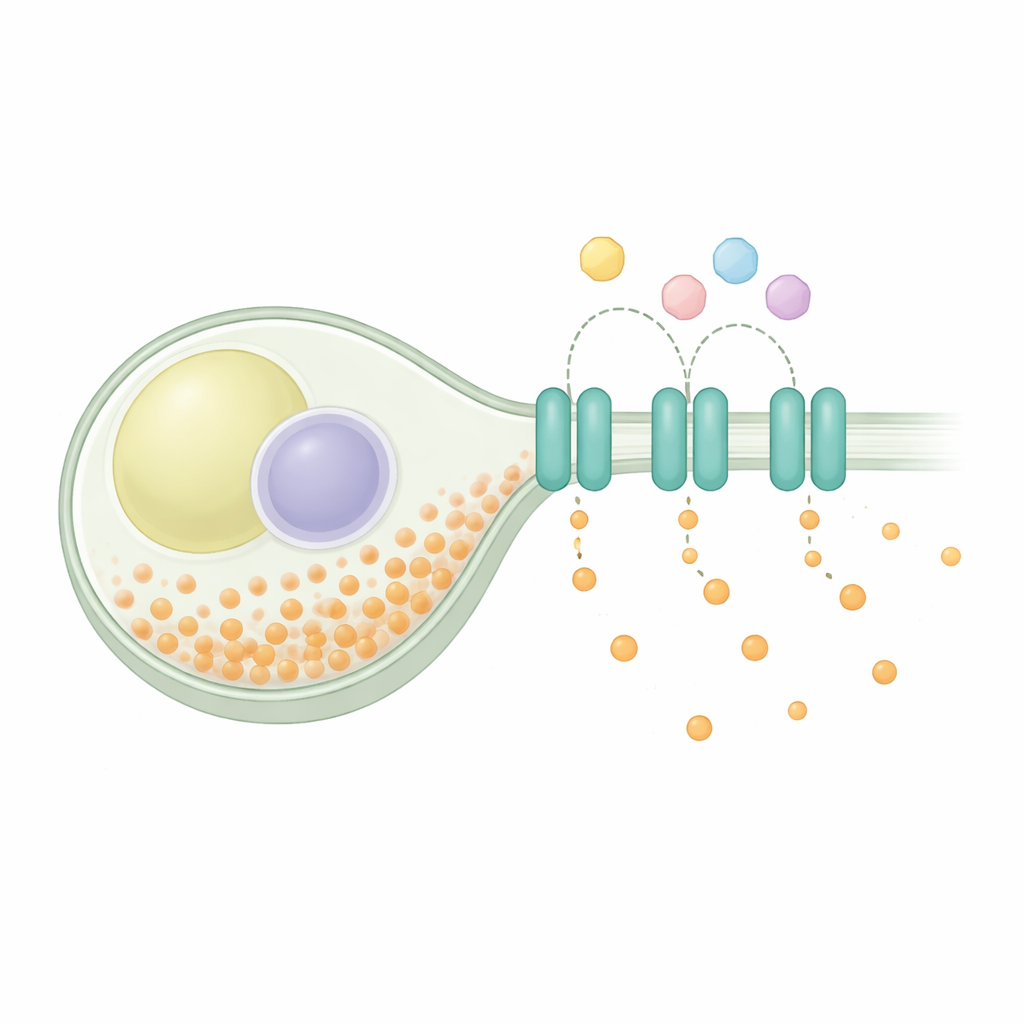
Hücre içinde dengeyi korumak
Fosfat homeostazı evrensel bir sorundur: hücreler metabolizma ve yapı taşları için fosfatı almak, bir kısmını güvenle depolamak ve fazla olanı dışarı vermek zorundadır. Mayoz bölünme mayasında, kıtlık durumunda alım sistemleri devreye girer ve fosfat bol olduğunda kapanır; bir depolama kompleksi de fazla fosfatı uzun zincirlere paketler. Genetik çalışmalar, depolama yolları bozulduğunda tehlikeli aşırı yüklenmeyi önlemeye yardımcı olan özel bir ihracatçı olarak SpXpr1 adlı bir proteinin görev yaptığını öne sürmüştü. SpXpr1, bitkiler ve insanlar da dahil olmak üzere ökaryotlarda bulunan XPR1 ihracatçı ailesine aittir; bu aileye ait ilişkili proteinler insanlarda beyin kireçlenmesi ve böbrek fonksiyon bozukluğu gibi rahatsızlıklarla bağlantılıdır. Bu ortak aile geçmişine rağmen, maya versiyonunun insan proteiniyle aynı şekilde çalışıp çalışmadığı belirsizdi.
Proteini görmek ve kanal olduğunu kanıtlamak
Araştırmacılar önce SpXpr1’in gerçekten fosfatı zarlar boyunca taşıyıp taşımadığını test ettiler. Mayanın proteininin kendi XPR1’i çıkarılmış insan hücrelerine yerleştirildiği deneyde, çevreleyen çözeltiye ne kadar fosfat sızdığı ölçüldü. SpXpr1 taşıyan hücreler kontrol hücrelere göre daha fazla fosfat ihraç etti; bu da aktivitesini doğruladı, ancak insan ihracatçısına göre daha az verimliydi. Elektriksel kayıtlar kullanılarak, SpXpr1 taşıyan hücrelerin inositol heksakisfosfat (InsP6) bulunduğunda artan fosfata bağımlı akımlar taşıdığı gösterildi. Bu, SpXpr1’in fosfat iyonlarının geçişine izin veren gerçek bir kanal olduğunu ve inozitol içeren habercilerle ayarlanabildiğini ortaya koydu.
Ortak bir yol boyunca iki kapı
SpXpr1’in atomik düzeyde nasıl çalıştığını anlamak için yazarlar cryo-elektron mikroskopisi kullanarak yapısını InsP6 yokluğunda ve varlığında belirlediler. Her SpXpr1 birimi membranda çiftli bir düzenin parçasını oluşturur ve dışta bir taşıma çekirdeği ile içeride bir düzenleyici domain içerir. Merkezi yol boyunca, fosfatın oturduğu iki ayrı nokta gözlemlediler; bu noktalar pozitif yüklü amino asitlerle koordine ediliyordu ve insan ile bitki karşıtlarında da korunmuştu; bu, fosfatın kendisinin nasıl tanındığına dair ortak bir planı vurgular. Ancak akraba proteinlerin aksine, maya proteini bu yola iki fiziksel kapı yerleştirir. İç tarafta, N-döngüsü adı verilen esnek bir segment, yakınlardaki kısa bir heliks ve bir zar geçişli heliksin genişlemiş ucu tarafından desteklenir; pore girişine katlanıp fosfatın içeri girmesini engeller. Dışta ise iki heliks arasında küçük bir döngü bir tıpa oluşturarak çıkışı kapatır. Bu kapılardan herhangi birini mutasyona uğratmak veya kesmek kanalın daha fazla fosfat sızdırmasına neden oldu; bu da bu yapıların proteini kendi kendini baskılayan, kapalı bir durumda tuttuğunu doğruladı.
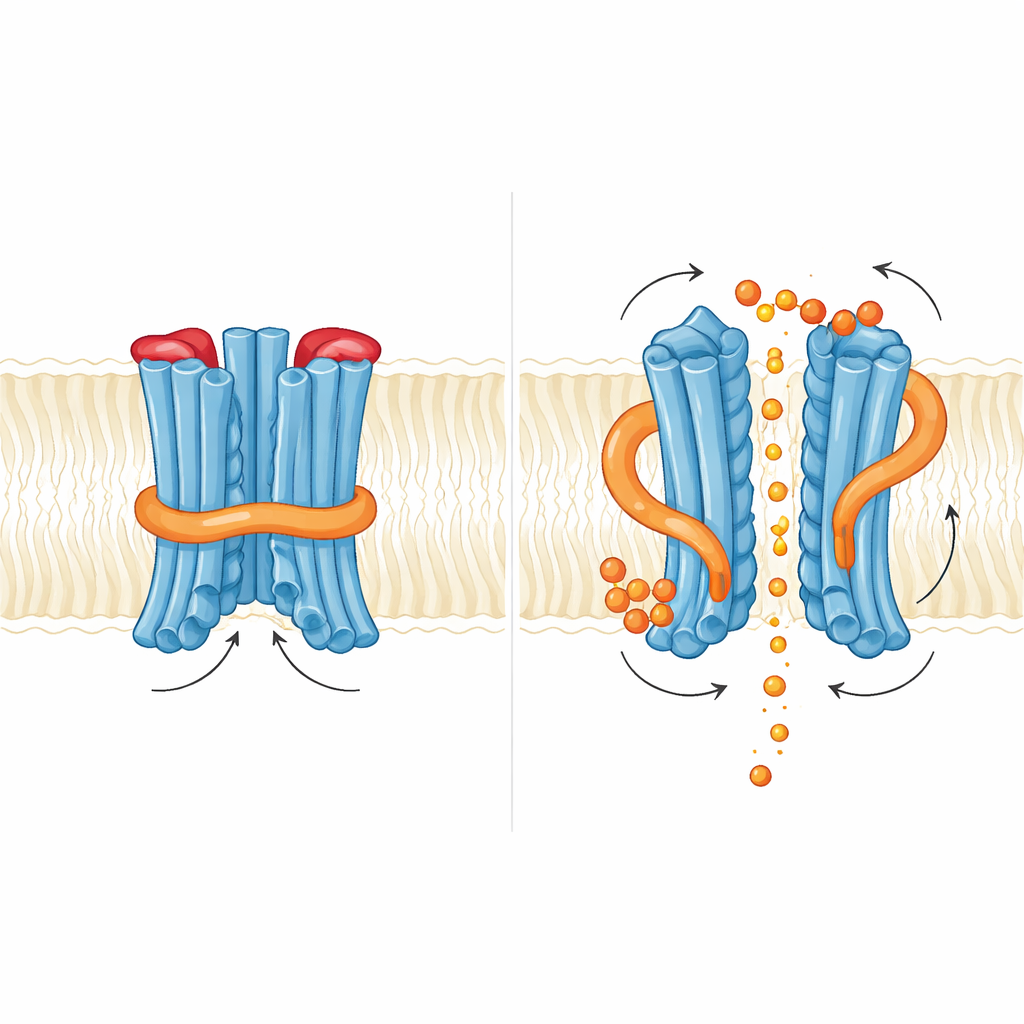
Küçük bir haberci kapıları nasıl iter
Takım daha sonra InsP6 bağlandığında ne olduğunu inceledi. Düzenleyici domainin membran çekirdeğiyle buluştuğu yerde ve dimerdeki iki düzenleyici domain arasındaki yüzeyde olmak üzere bazik kalıntılar bakımından zengin iki bağlanma cebini buldular. InsP6 bağlanması düzenleyici bölgenin ince bir rotasyonuna yol açtı ve N-döngüsünü destekleyen kısa heliksi kararsızlaştırdı, ancak yakalanan yapılarda döngü yine de fosfat yolunu tıkayacak biçimde kaldı. Fonksiyonel olarak, InsP6 eklenmesi fosfat akımlarını artırdı, ancak InsP6 bağlanmasını zayıflatan mutasyonlar ihracatı yok etmedi, bazen hatta artırdı. Bu bulgu, mayada inozitol habercisinin kapalı-açık bir anahtar gibi değil, içsel bir kilidi gevşeten ince ayar yapıcı bir etki gösterdiğini düşündürür. Yazarlar, daha yüksek yüklü inozitol pirofosfatlar olan InsP7 veya InsP8’in, hem içteki N-döngüsü kapısını hem de dıştaki tıpayı tamamen yerinden oynatabilecek gerçek fizyolojik tetikleyiciler olabileceğini öneriyorlar.
Maya ötesinde bunun anlamı
Bu yapısal ve fonksiyonel deneyler birlikte, SpXpr1’in normalde çift kilitli bir durumda oturduğu; iç ve dış kapıların fosfat yolunu koruduğu çalışır bir modeli destekliyor. Fosfat fazlalığı sırasında üretilen inozitol bazlı sinyallerin artması bu kilitleri kademeli olarak gevşeterek fosfatın dışarı akmasına ve hücrenin korunmasına izin verir. İnsan ihracatçısının gözenekini tıkayıp açmak için farklı bir hareketli segment kullanmasıyla karşılaştırıldığında, maya çözümü evrimin aynı temel iskeleti farklı yaşam tarzlarına uyacak şekilde nasıl yeniden kablolayabildiğini gösterir—mantarlarda sıkı korunma versus memelilerde hızlı ihracat. Bu tasarım ilkelerini anlamak, araştırmacıların bitkilerde fosfat kullanımını ayarlamalarına, mantarların fosfat kontrolünü bozacak hedefe yönelik antifungal ilaçlar tasarlamalarına ve insan XPR1 proteinindeki hastalık yapıcı değişiklikleri daha iyi yorumlamalarına yardımcı olabilir.
Atıf: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
Anahtar kelimeler: fosfat homeostazı, iyon kanalları, cryo-EM yapısı, inozitol polifosfatlar, zar taşınımı