Clear Sky Science · it
Approfondimenti strutturali sul meccanismo di gating dell’esportatore di fosfato di lievito Schizosaccharomyces SpXpr1
Perché contano i minuscoli passaggi per il fosfato
Ogni cellula deve bilanciare con cura il fosfato, un componente piccolo ma indispensabile in molecole come il DNA, le membrane e la moneta energetica della cellula. Troppo poco fosfato blocca la crescita; troppo può essere tossico. Questo studio esamina come il lievito Schizosaccharomyces, un fungo modello, espelle l’eccesso di fosfato dalla cellula tramite una porta molecolare chiamata SpXpr1. Svelando la struttura tridimensionale di questa porta e il modo in cui si apre e si chiude, il lavoro illumina come organismi molto diversi — dai funghi agli umani — usino proteine affini per mantenere sotto controllo i livelli di fosfato, con implicazioni per malattie cerebrali, salute renale, agricoltura e strategie antifungine.
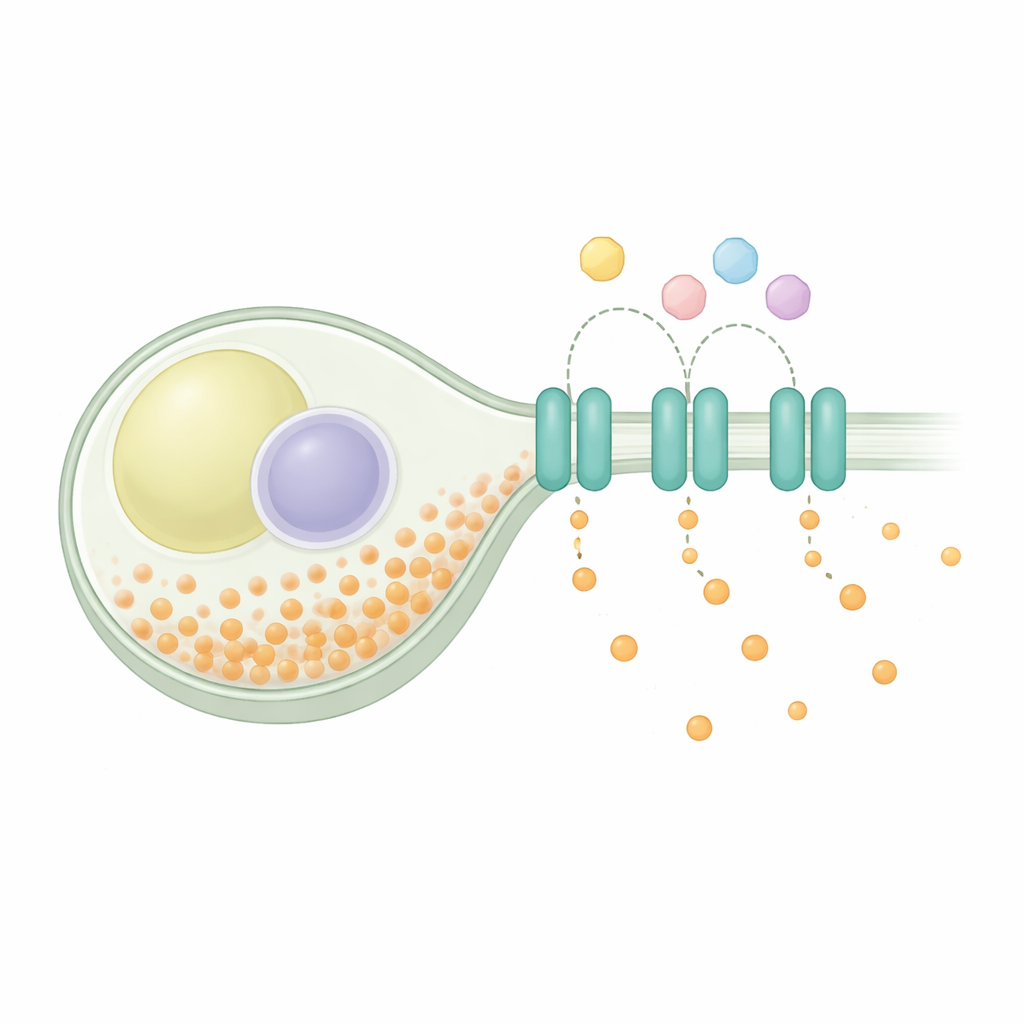
Mantenere l’equilibrio all’interno di una cellula
L’omeostasi del fosfato è un problema universale: le cellule devono importare fosfato per il metabolismo e per i mattoni strutturali, immagazzinarne una parte in modo sicuro e esportare eventuali surplus. Nel lievito, i sistemi di uptake si attivano in condizioni di scarsità e si spengono quando il fosfato è abbondante, mentre un complesso di stoccaggio impacchetta l’eccesso in catene lunghe. Studi genetici avevano suggerito che una proteina chiamata SpXpr1 funge da esportatore dedicato, aiutando a prevenire sovraccarichi pericolosi quando le vie di immagazzinamento sono compromesse. SpXpr1 appartiene alla famiglia XPR1 di esportatori presente negli eucarioti, comprese piante e umani, dove proteine affini sono collegate a patologie come la calcificazione cerebrale e disfunzioni renali. Nonostante questa parentela di famiglia, non era chiaro se la versione del lievito funzionasse allo stesso modo della proteina umana.
Vedere la proteina e dimostrare che è un canale
I ricercatori hanno prima verificato se SpXpr1 spostasse davvero il fosfato attraverso le membrane. Hanno inserito la proteina del lievito in cellule umane cui era stato rimosso l’XPR1 endogeno, quindi hanno misurato quanto fosfato filtrava nella soluzione circostante. Le cellule con SpXpr1 esportavano più fosfato rispetto alle cellule di controllo, confermandone l’attività, sebbene con efficienza inferiore rispetto all’esportatore umano. Tramite registrazioni elettriche, il gruppo ha quindi mostrato che le cellule che esprimevano SpXpr1 presentavano correnti dipendenti dal fosfato che aumentavano in presenza della piccola molecola di segnalazione inositolo esafosfato (InsP6). Ciò ha stabilito SpXpr1 come un vero canale che permette il passaggio di ioni fosfato e che può essere modulato da messaggeri contenenti inositolo.
Due porte lungo un percorso condiviso
Per comprendere il funzionamento di SpXpr1 a livello atomico, gli autori hanno usato la crio–microscopia elettronica per determinarne la struttura in assenza e presenza di InsP6. Ogni unità di SpXpr1 è parte di un assemblaggio a coppia nella membrana e contiene un nucleo di trasporto esterno e un dominio regolatorio interno. Lungo il percorso centrale, hanno osservato due punti distinti dove il fosfato può posizionarsi, coordinato da amminoacidi positivamente carichi; questi siti sono conservati nei corrispondenti umani e vegetali, evidenziando un progetto condiviso per il riconoscimento dello stesso fosfato. Tuttavia, a differenza dei suoi parenti, la proteina del lievito costruisce due porte fisiche in questo percorso. Sul lato interno, un segmento flessibile chiamato N-loop, sostenuto da una breve elica vicina e da un’estremità estesa di un’elica transmembrana, si ripiega nell’ingresso del poro bloccando l’accesso del fosfato. All’esterno, un piccolo loop tra due eliche forma un tappo che sigilla l’uscita. Mutazioni o troncamenti di una qualsiasi di queste porte hanno fatto sì che il canale perdesse più fosfato, confermando che di norma mantengono la proteina in uno stato auto-inibito, chiuso.
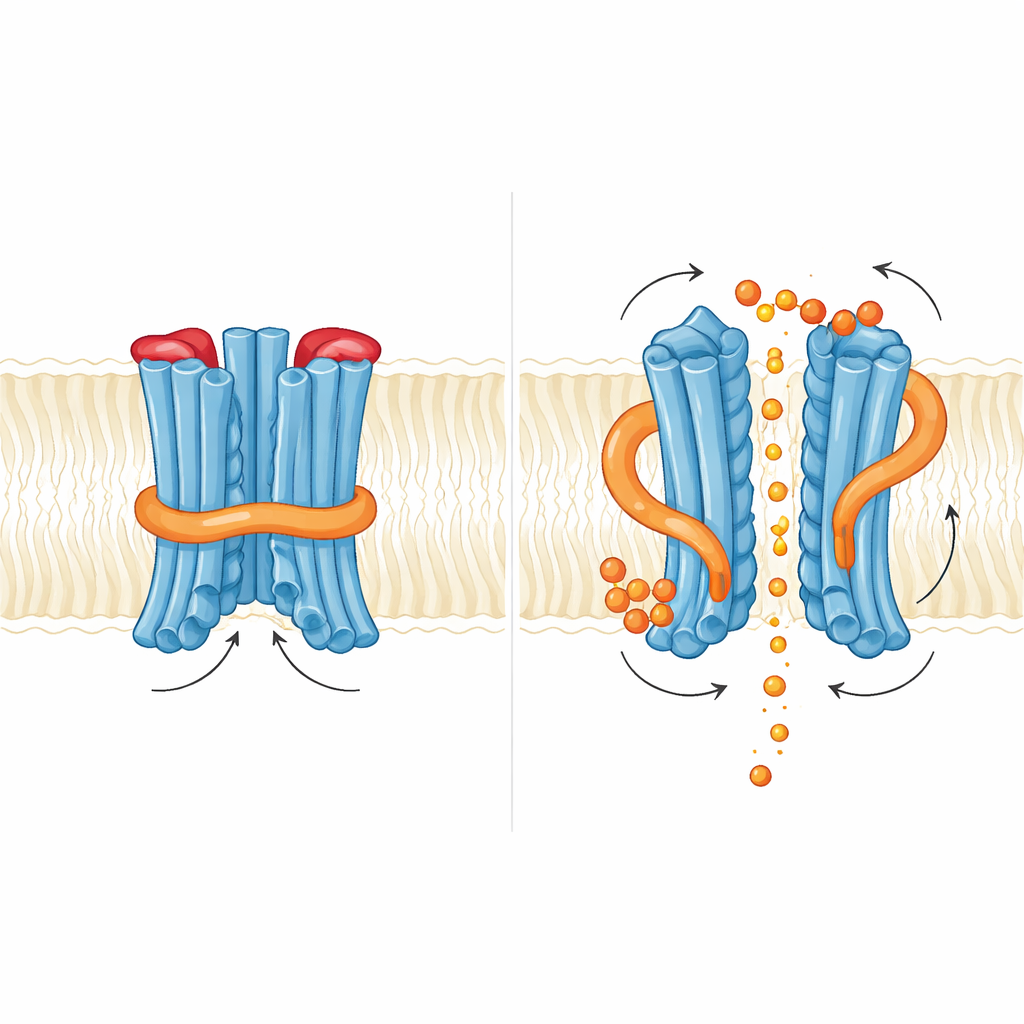
Come un piccolo messaggero smuove le porte
Il gruppo ha poi esaminato cosa accade quando InsP6 si lega. Hanno individuato due tasche di legame ricche di residui basici: una dove il dominio regolatorio incontra il nucleo di membrana e un’altra all’interfaccia tra i due domini regolatori nel dimero. Il legame di InsP6 ha provocato una sottile rotazione della regione regolatoria e ha destabilizzato la breve elica che sostiene l’N-loop, ma il loop stesso rimaneva comunque a ostacolare il passaggio del fosfato nelle strutture catturate. Funzionalmente, l’aggiunta di InsP6 aumentava le correnti di fosfato, ma mutazioni che indebolivano il legame con InsP6 non abolivano l’esportazione e a volte la potenziavano. Ciò suggerisce che, nel lievito, il messaggero inositolo agisca più come un regolatore fine che allenta una serratura interna che come un interruttore on–off. Gli autori propongono che inositolo pirofosfati più carichi, come InsP7 o InsP8, possano essere i veri trigger fisiologici in grado di spostare completamente sia la porta interna dell’N-loop sia il tappo esterno.
Quali implicazioni oltre il lievito
Nel complesso, questi esperimenti strutturali e funzionali supportano un modello operativo in cui SpXpr1 risiede normalmente in uno stato a doppia chiusura, con una porta interna e una esterna che sorvegliano il percorso del fosfato. L’aumento dei segnali a base di inositolo prodotti durante l’eccesso di fosfato rilascia gradualmente queste serrature, permettendo al fosfato di fluire verso l’esterno e proteggere la cellula. Rispetto all’esportatore umano, che usa un segmento mobile diverso per tappare e stappare il suo poro, la soluzione del lievito mostra come l’evoluzione possa riconfigurare lo stesso impalcatura di base per adattarsi a stili di vita differenti — conservazione rigorosa nei funghi contro esportazione rapida nei mammiferi. Comprendere questi principi di progetto potrebbe aiutare i ricercatori a regolare l’uso del fosfato nelle colture, progettare farmaci antifungini mirati che interrompano il controllo fungino del fosfato e interpretare meglio le variazioni patogenetiche nella proteina XPR1 umana.
Citazione: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
Parole chiave: omeostasi del fosfato, canali ionici, struttura cryo-EM, inositolo polifosfati, trasporto attraverso la membrana