Clear Sky Science · ru
Структурные сведения о механизме открытия-закрытия фосфатного экспортера SpXpr1 из дрожжей деления
Почему важны такие крошечные ворота для фосфата
Каждая клетка должна точно уравновешивать фосфат — небольшой, но незаменимый компонент молекул, таких как ДНК, мембраны и энергетическая валюта клетки. Недостаток фосфата тормозит рост; избыток может быть токсичен. В этом исследовании изучают, как дрожжи деления, модельный гриб, выталкивают из клетки лишний фосфат через молекулярную «дверь» под названием SpXpr1. Раскрыв трёхмерную структуру этой «двери» и механизм её открытия и закрытия, работа проливает свет на то, как весьма разные организмы — от грибов до человека — используют родственные белки для поддержания фосфатного баланса, что имеет значение для заболеваний мозга, функции почек, сельского хозяйства и антигрибковых стратегий.
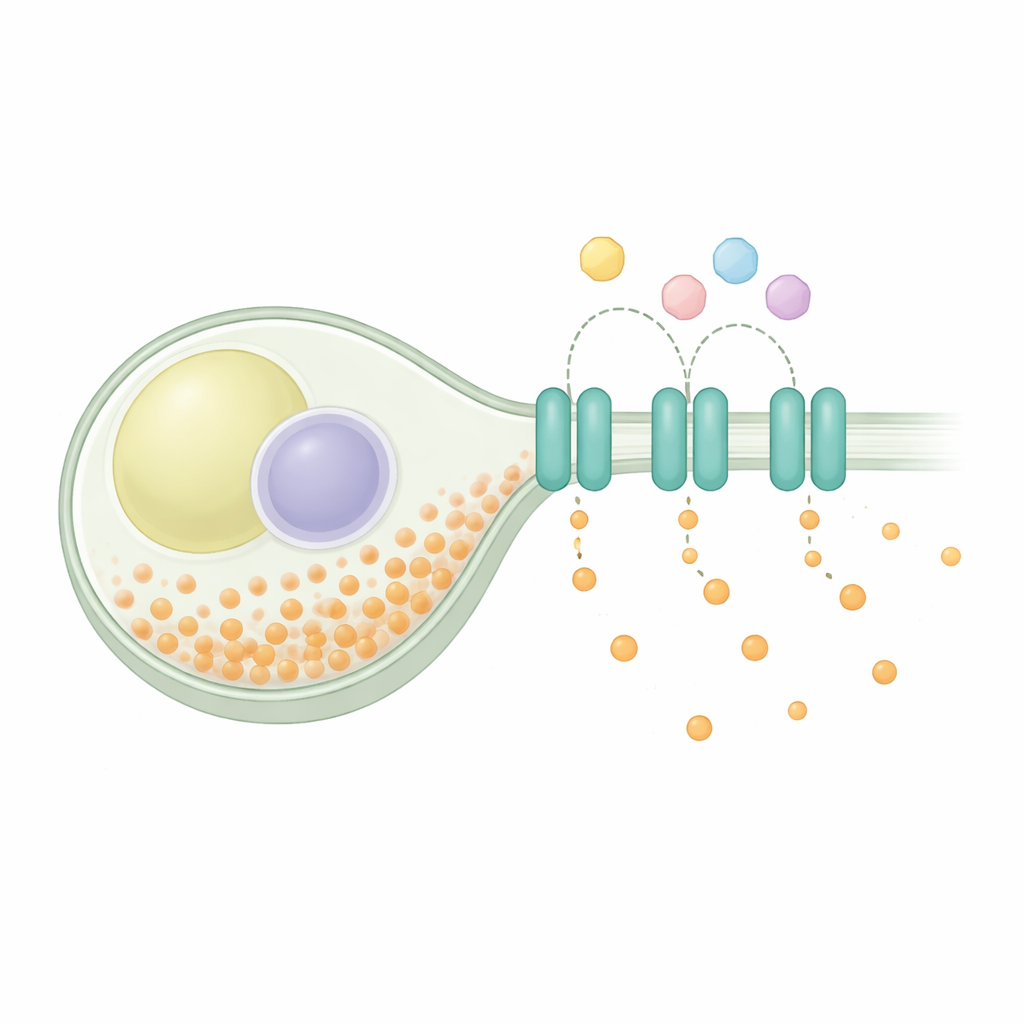
Поддержание баланса внутри клетки
Гомеостаз фосфата — универсальная задача: клетки должны импортировать фосфат для метаболизма и синтеза конструктивных материалов, безопасно хранить его часть и экспортировать излишек. У дрожжей деления системы поглощения включаются при дефиците и выключаются при обилии фосфата, в то время как комплекс для хранения упаковывает избыток в длинные цепи. Генетические исследования предполагали, что белок SpXpr1 действует как специализированный экспортер и помогает предотвратить опасную перегрузку, когда пути хранения нарушены. SpXpr1 принадлежит к семейству XPR1 экспортеров, встречающихся у эукариот, включая растения и человека, где родственные белки связаны с такими расстройствами, как кальцификация мозга и нарушение функции почек. Несмотря на это общее происхождение, оставалось неясным, работает ли дрожжевой вариант так же, как человеческий белок.
Наблюдение белка и доказательство, что он является каналом
Исследователи сначала проверили, действительно ли SpXpr1 перемещает фосфат через мембраны. Они встроили дрожжевой белок в человеческие клетки, у которых удалили собственный XPR1, затем измерили, сколько фосфата просачивается в окружающий раствор. Клетки со SpXpr1 экспортировали фосфат больше, чем контрольные клетки, подтвердив его активность, хотя он был менее эффективен, чем человеческий экспортер. С помощью электрических записей команда показала, что клетки, несущие SpXpr1, создают фосфат-зависимые токи, которые увеличивались в присутствии небольшого сигнального молекулы инозитолгексakisфосфата (InsP6). Это установило SpXpr1 как подлинный канал, пропускающий ионы фосфата и регулируемый иноситолсодержащими мессенджерами.
Две двери вдоль общего пути
Чтобы понять работу SpXpr1 на атомном уровне, авторы использовали крио-электронную микроскопию для определения структуры в отсутствие и присутствие InsP6. Каждая единица SpXpr1 входит в состав парного образования в мембране и содержит внешнее транспортное ядро и внутренний регуляторный домен. Вдоль центрального пути они обнаружили две отдельные позиции, где может располагаться фосфат, координируемый положительно заряженными аминокислотами; эти сайты консервативны у человеческих и растительных аналогов, что подчёркивает общую «чертёжную» схему узнавания самого фосфата. Однако, в отличие от родичей, дрожжевой белок создаёт две физические задвижки в этом пути. Внутри гибкий сегмент, называемый N-петлей, поддерживаемый соседней короткой спиралью и удлинённым концом одного мембранного спирального фрагмента, складывается в вход поры и блокирует попадание фосфата. Снаружи небольшой петлевой участок между двумя спиралями образует пробку, которая закупоривает выход. Мутации или укорачивание любой из этих заслонок вызывало усиленную утечку фосфата через канал, что подтверждает, что в норме они удерживают белок в самотормозящем, закрытом состоянии.
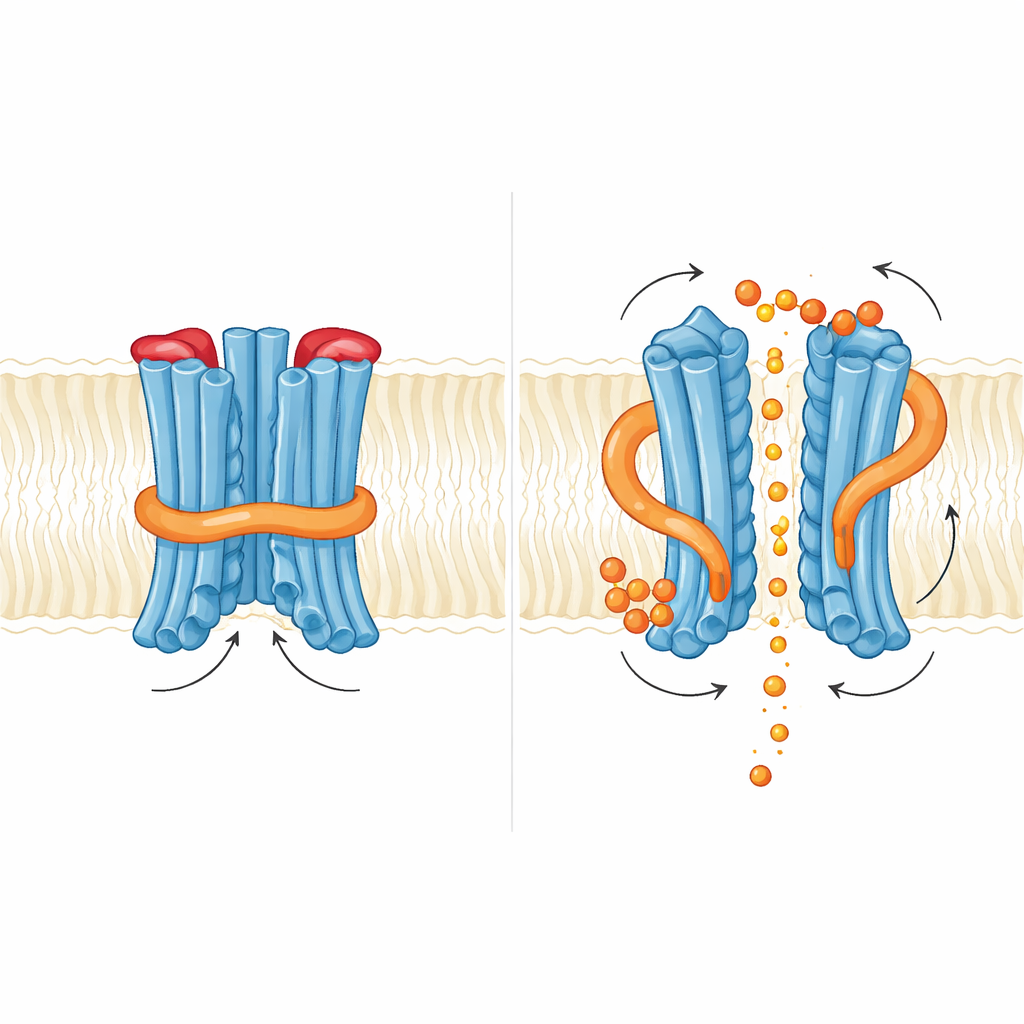
Как малый мессенджер подталкивает заслонки
Далее команда изучила, что происходит при связывании InsP6. Они обнаружили два связывающих кармана, богатых основными остатками: один там, где регуляторный домен встречается с мембранным ядром, и другой на интерфейсе между двумя регуляторными доменами в димере. Связывание InsP6 вызвало небольшое вращение регуляторной области и дестабилизацию короткой спирали, подпирающей N-петлю, но сама петля в захваченных структурах всё ещё блокировала путь для фосфата. Функционально добавление InsP6 увеличивало фосфатные токи, но мутации, ослаблявшие связывание InsP6, не отменяли экспорт и иногда даже усиливали его. Это говорит о том, что у дрожжей инозитолский мессенджер скорее действует как тонкий регулятор, ослабляющий внутренний замок, чем как простой выключатель вкл/выкл. Авторы предполагают, что более сильно заряженные инозитол-пирофосфаты, такие как InsP7 или InsP8, могут быть настоящими физиологическими триггерами, способными полностью отодвинуть как внутреннюю N-петлю, так и внешнюю пробку.
Что это значит за пределами дрожжей
В совокупности структурные и функциональные эксперименты поддерживают рабочую модель, в которой SpXpr1 обычно находится в двойном запертом состоянии, с внутренней и внешней заслонками, охраняющими фосфатный путь. Повышение уровней иноситол-основанных сигналов, возникающее при избытке фосфата, постепенно раскрывает эти замки, позволяя фосфату выйти и защитить клетку. По сравнению с человеческим экспортером, который использует другой подвижный сегмент для закупорки и раскрытия своей поры, решение дрожжей демонстрирует, как эволюция может перенастроить одну и ту же базовую «раму» под разные образ жизни — строгая консервация у грибов против быстрого экспорта у млекопитающих. Понимание этих принципов проектирования может помочь исследователям оптимизировать использование фосфата в сельском хозяйстве, разрабатывать целевые антигрибковые препараты, нарушающие контроль фосфата у грибов, и лучше интерпретировать патогенные изменения в белке XPR1 человека.
Цитирование: Yang, H., Wang, Y., Yue, C. et al. Structural insights into the gating mechanism of the fission yeast phosphate exporter SpXpr1. Cell Discov 12, 27 (2026). https://doi.org/10.1038/s41421-026-00883-8
Ключевые слова: гомеостаз фосфата, ионные каналы, структура крио-ЭМ, инозитол-полифосфаты, мембранный транспорт