Clear Sky Science · zh
沙霉素作为死亡开关:胃癌细胞如何选择其终结方式
这项研究对患者为何重要
胃癌仍然是全球致死率最高的癌症之一,主要原因在于许多肿瘤学会对标准药物产生耐受性。问题的一大部分在于肿瘤由多种不同类型的细胞组成,其中包括一小群顽固的癌症干细胞,它们能在治疗后重新启动疾病。本研究探讨了一种老兽药——沙霉素,是否可以被转化为对抗胃癌的新武器,通过让这些细胞以多种方式走向死亡。
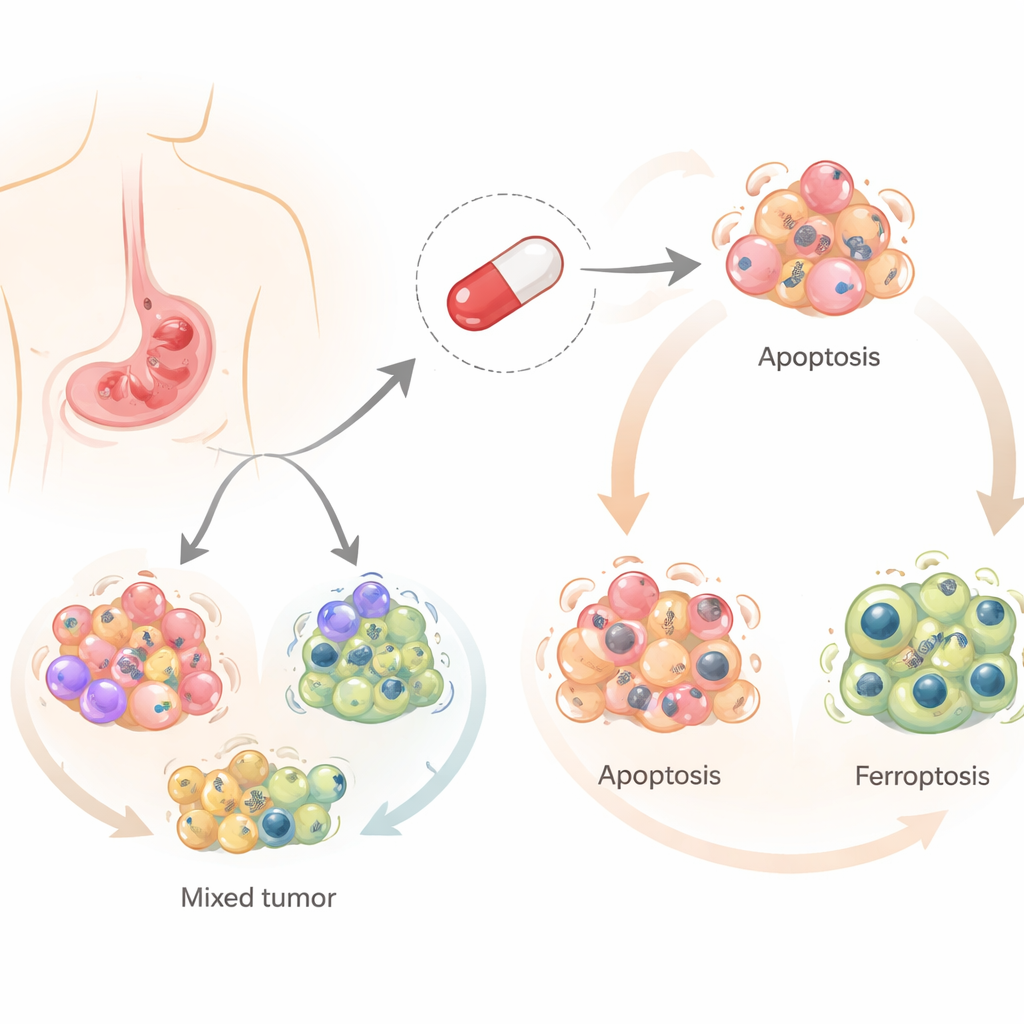
一个有新用途的老药
沙霉素最初用于预防家畜感染,但在过去十年中因其杀灭癌细胞、尤其是癌症干细胞的能力而受到关注。与大多数通常依赖单一主要通路杀死细胞的化疗药不同,沙霉素能够触发多种受控的细胞死亡形式。研究者聚焦于其中三种:经典的程序性细胞死亡(凋亡)、与细胞自我回收有关的过程(自噬)以及一种由脂质损伤驱动、依赖铁的新型死亡形式(铁死亡)。理解哪条路径在胃癌中被激活很重要,因为能够逃避一种途径的肿瘤可能仍然对另一种途径敏感。
肿瘤细胞如何选择死亡方式
研究团队在四种不同的人源胃癌细胞系上测试了沙霉素,这些细胞系代表了患者中观察到的多样性。他们发现相同的药物会将不同细胞推向不同的命运。在两种细胞系中,沙霉素主要引发凋亡,使细胞安静地自我解体。而在另外两种中,它则诱导铁死亡,这是一种与铁、活性氧分子及细胞脂质成分损伤相关的更具爆发性的死亡形式。在所有情况下,自噬都较早被激活,表明存在一个共同的起点,从该起点细胞被引导走向某一特定的死亡通路。
引导死亡决定的信号
进一步研究中,研究者测量了在细胞内起到交通信号作用的关键蛋白。在走向凋亡的细胞中,沙霉素降低了生长与存活信号(如mTOR和survivin),并激活了分解细胞内容物和损伤线粒体的蛋白。在经历铁死亡的细胞中,药物同样抑制了mTOR和survivin,但还抑制了两种重要的脂质损伤防护因子SLC7A11和GPX4。通过分析基因表达数据,他们识别出一组20基因模式,该模式标记出更倾向于发生铁死亡而非凋亡的细胞,提示每个肿瘤的分子“接线”有助于决定其对治疗的死亡响应方式。
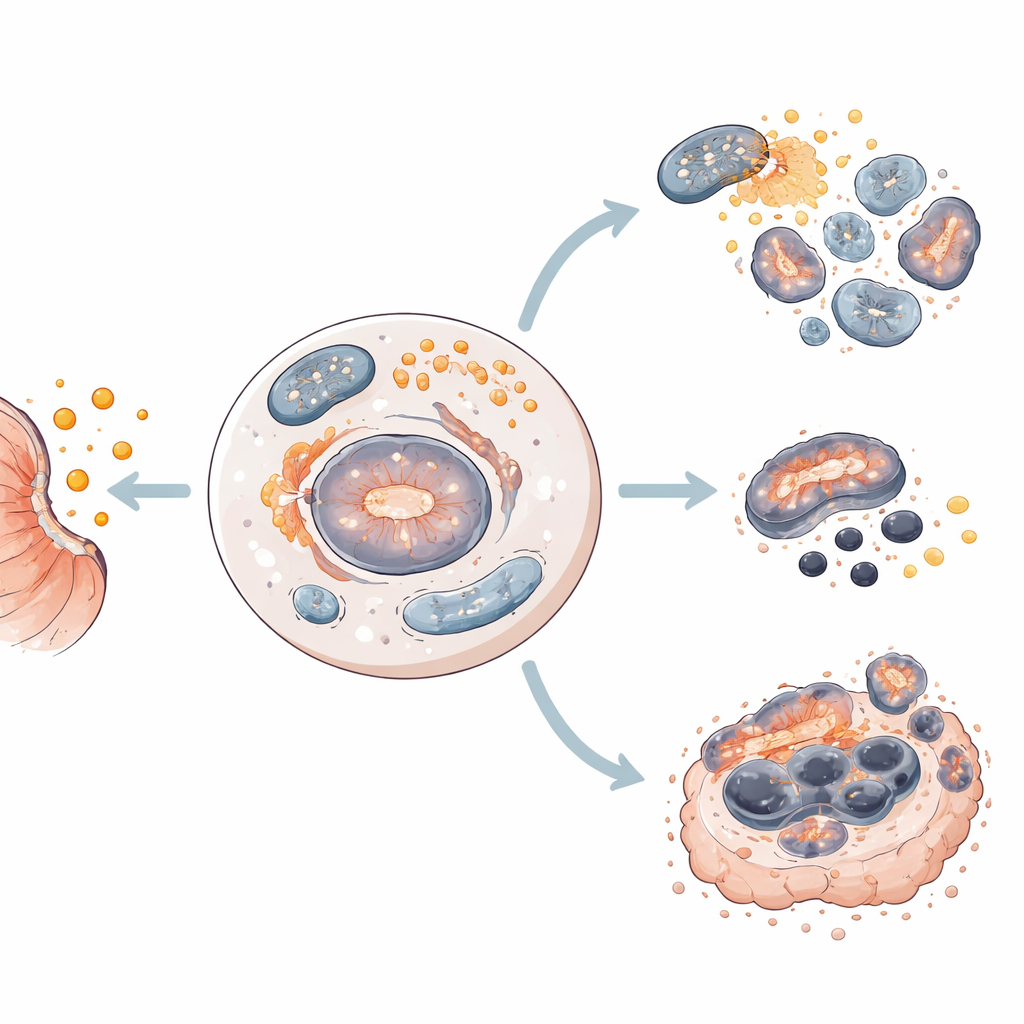
针对复发根源的策略
研究还考察了以表面标志物CD44和CD133识别的癌症干细胞,这些标志与药物耐受性和铁死亡调控相关。在耐药性最强的细胞系中,这类干样细胞普遍存在,能形成稳固的三维“球体”并产生大量克隆。沙霉素显著降低了携带这些标记的细胞比例,缩小或消除了球体并阻止克隆生长,表明它攻击了最可能导致复发的细胞。当研究团队将与铁死亡相关的基因模式应用于大规模患者数据集时,他们能够区分具有不同生存预后的患者群体,表明这一分子指纹具有现实世界的预后价值。
在类患者迷你肿瘤中的测试
为更接近临床应用,研究者在患者来源的胃癌类器官——从人体肿瘤样本培养出的模拟真实癌症诸多特征的微小三维结构上测试了沙霉素。在所有类器官模型中,沙霉素都降低了存活率并破坏了结构。在大多数模型中它激活了凋亡相关酶;在一个未显示凋亡的模型中,则触发了铁死亡的特征,包括线粒体活性改变和保护性铁死亡蛋白的丧失。所有模型中自噬均有所增加,强化了其作为沙霉素诱导细胞死亡共同早期步骤的作用。
这对未来治疗可能意味着什么
总体来看,这项工作将沙霉素描绘成一种“死亡开关”,能够将胃癌细胞切换为凋亡或铁死亡的自毁途径,自噬则作为共同的前奏。通过同时打击肿瘤大体及其干样核心,并在常规通路受阻时提供替代的死亡途径,沙霉素可能有助于克服多药耐受性。这里开发的基于铁死亡的基因特征谱可能帮助医生识别更有可能获益的患者,从而为胃癌提供更个性化和更持久的治疗策略。
引用: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
关键词: 胃癌, 沙霉素, 癌症干细胞, 铁死亡, 药物耐受性