Clear Sky Science · tr
Salinomisin bir ölüm anahtarı olarak: mide kanseri hücreleri nasıl yok oluşlarını seçer
Bu araştırma hastalar için neden önemli
Mide kanseri, birçok tümörün standart ilaçları etkisiz hale getirmeyi öğrenmesi nedeniyle hâlâ dünyanın en ölümcül kanserlerinden biridir. Sorunun büyük bir kısmı, tümörlerin tedaviden sonra hastalığı yeniden başlatabilen küçük ama inatçı bir hücre grubu olan kanser kök hücreleri dahil olmak üzere çeşitli hücre tiplerinden oluşmasıdır. Bu çalışma, eski bir veteriner ilacı olan salinomisinin, bu hücreleri birden fazla yolla ölüme zorlayarak mide kanserine karşı yeni bir silaha dönüştürülüp dönüştürülemeyeceğini araştırıyor.
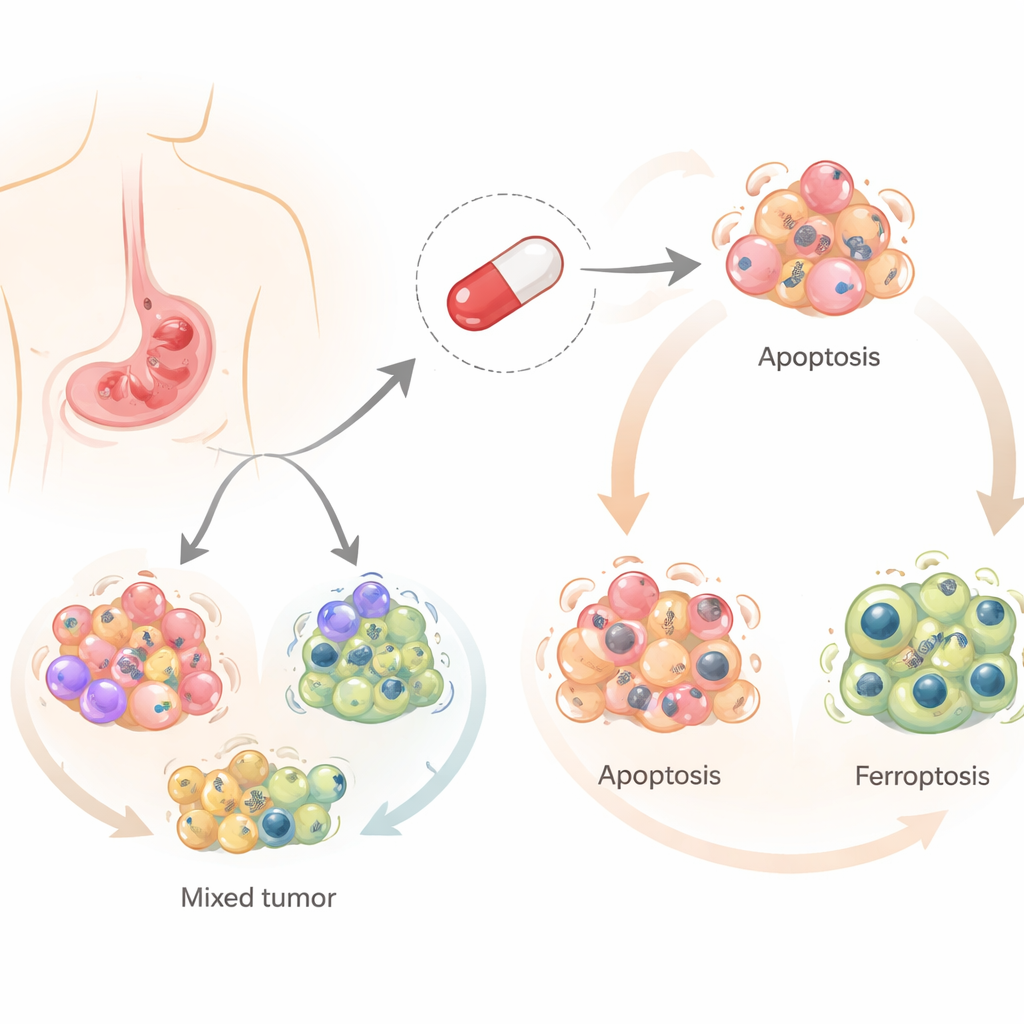
Yeni bir işle görevlendirilmiş eski bir ilaç
Salinomisin başlangıçta çiftlik hayvanlarında enfeksiyonları önlemek için geliştirildi, ancak son on yılda özellikle kanser kök hücreleri olmak üzere kanser hücrelerini öldürme yeteneğiyle dikkat çekti. Çoğu kemoterapi ilacının tek bir ana yola dayanarak hücreleri öldürmesinin aksine, salinomisin birkaç kontrollü hücre ölümü biçimini tetikleyebilir. Araştırmacılar bunlardan üçüne odaklandı: klasik programlı hücre ölümü (apoptoz), geri dönüşümle ilişkili bir süreç (otokfaji) ve yağ zararına bağlı, demir bağımlı daha yeni bir ölüm türü (ferroptoz). Bu yolların mide kanserinde hangilerinin etkinleştiğini anlamak önemlidir; çünkü bir yolu atlatabilen tümörler başka bir yoldan hâlâ savunmasız olabilir.
Tümör hücreleri yok oluş yollarını nasıl seçer
Ekip, hastalardaki çeşitliliği temsil eden dört farklı insan mide kanseri hücre hattında salinomisini test etti. Aynı ilacın farklı hücreleri farklı kaderlere ittiğini buldular. İki hücre hattında salinomisin ağırlıklı olarak hücrelerin sessizce kendilerini dağıttığı apoptozu tetiklerken, diğer iki hattı daha çok demir, reaktif oksijen molekülleri ve hücrenin yağ bileşenlerine verilen zararla bağlantılı daha patlayıcı bir ölüm olan ferroptoz yönüne sürükledi. Her durumda ototfaji erken dönemde etkinleşti; bu, hücrelerin bir ölüm yoluna veya diğerine yönlendirildiği ortak bir başlangıç noktasına işaret ediyor.
Ölüm kararını yönlendiren sinyaller
Daha derine inen araştırmacılar, hücre içindeki trafik ışıkları gibi davranan anahtar proteinleri ölçtüler. Apoptoza giden hücrelerde salinomisin büyüme ve hayatta kalma sinyallerini (mTOR ve survivin gibi) bastırdı ve hücre içeriklerini parçalayan ile mitokondrilere zarar veren proteinleri aktifleştirdi. Ferroptoz geçiren hücrelerde ise ilaç yine mTOR ve survivin düzeylerini düşürdü, ancak ayrıca yağ hasarına karşı iki önemli koruyucu olan SLC7A11 ve GPX4’ü baskıladı. Gen aktivite verilerini analiz ederek, apoptozdan ziyade ferroptoz eğilimli hücreleri işaretleyen 20 genlik bir desen tanımladılar; bu da her tümörün moleküler “devre yapısının” tedaviye nasıl cevap vereceğini belirlemeye yardımcı olduğunu gösteriyor.
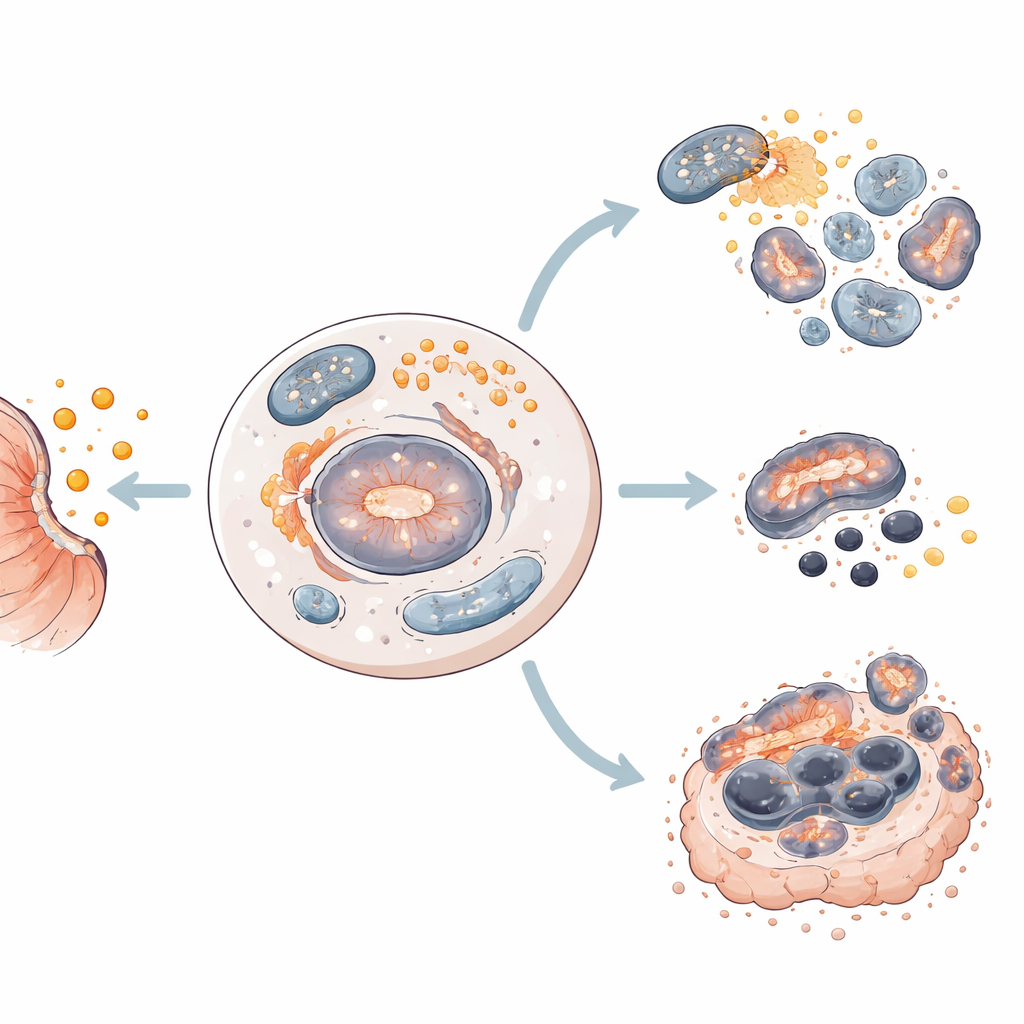
Nüksün köklerini hedef almak
Çalışma ayrıca CD44 ve CD133 yüzey belirteçleriyle tanımlanan, ilaç direnci ve ferroptoz kontrolü ile ilişkilendirilen kanser kök hücrelerini inceledi. En ilaç dirençli hücre hatlarında bu kök benzeri hücreler yaygındı, sağlam 3B “sferoidler” oluşturuyor ve birçok koloni üretiyordu. Salinomisin bu belirteçleri taşıyan hücrelerin oranını keskin şekilde azalttı, sferoidleri küçülttü veya ortadan kaldırdı ve koloni büyümesini engelledi; bu da ilacın nükse en yatkın hücreleri doğrudan hedef aldığını gösteriyor. Araştırmacılar ferroptoz ilişkili gen desenini büyük hasta veri kümelerine uyguladıklarında, farklı sağkalım beklentilerine sahip grupları ayırabildiler; bu da moleküler parmak izinin klinik açıdan prognostik değer taşıdığını ortaya koyuyor.
Hastaya benzer mini-tümörlerde yaklaşımı test etmek
Klinik uygulamaya yaklaşmak için araştırmacılar salinomisini hasta kaynaklı mide kanseri organoidleri üzerinde test ettiler—insan tümör örneklerinden yetiştirilen ve gerçek kanserlerin birçok özelliğini taklit eden küçük 3B yapılar. Tüm organoid modellerinde salinomisin hücre canlılığını azalttı ve yapıyı bozdu. Çoğu durumda apoptotik enzimleri aktive etti; apoptoz göstermeyen bir modelde ise bunun yerine mitokondriyal aktivitede değişiklikler ve koruyucu ferroptoz proteinlerinin kaybı dahil ferroptoz belirteçlerini tetikledi. Otokfaji tüm modellerde arttı ve salinomisin kaynaklı ölümde ortak bir erken adım rolünü pekiştirdi.
Gelecekteki tedavi için olası sonuçlar
Genel olarak bu çalışma, salinomisini mide kanseri hücrelerini otofajiyi ortak bir başlangıç olarak kullanarak ya apoptozik ya da ferroptotik öz-yıkıma çevirebilen bir “ölüm anahtarı” olarak resmediyor. Hem kütle tümörü hem de onun kök-benzeri çekirdeğini eşzamanlı olarak hedefleyerek ve olağan yol engellendiğinde alternatif bir ölüm rotası sunarak, salinomisin çoklu ilaç direncinin aşılmasına yardımcı olabilir. Burada geliştirilen ferroptoz bazlı gen imzası, hangi hastaların daha fazla fayda görme olasılığı olduğunu belirlemede doktorlara yardımcı olabilir ve mide kanseri için daha kişiselleştirilmiş ve kalıcı tedavi stratejilerinin yolunu açabilir.
Atıf: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
Anahtar kelimeler: mide kanseri, salinomisin, kanser kök hücreleri, ferroptoz, ilaç direnci