Clear Sky Science · de
Salinomycin als Todes-Schalter: wie Magenkrebszellen ihr Ende wählen
Warum diese Forschung für Patienten wichtig ist
Magenkrebs gehört nach wie vor zu den tödlichsten Krebsarten weltweit, vor allem weil viele Tumoren lernen, Standardmedikamente zu ignorieren. Ein zentrales Problem ist, dass Tumoren aus verschiedenen Zelltypen bestehen, darunter eine kleine, hartnäckige Gruppe von Krebsstammzellen, die die Erkrankung nach einer Behandlung wieder entfachen können. Diese Studie untersucht, ob ein altes Tierarzneimittel, Salinomycin, als neue Waffe gegen Magenkrebs eingesetzt werden kann, indem es diese Zellen dazu bringt, auf mehr als einem Weg zu sterben.
Ein altes Medikament mit neuer Aufgabe
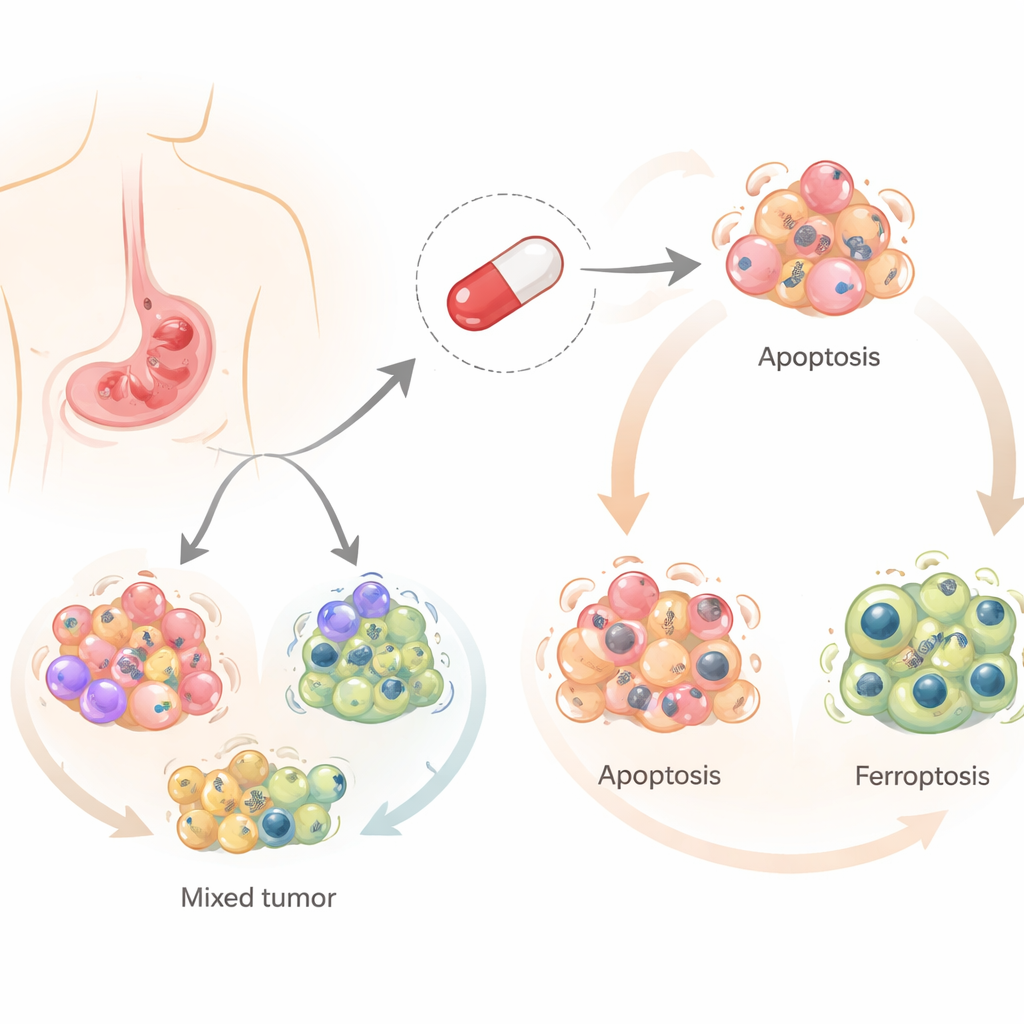
Salinomycin wurde ursprünglich entwickelt, um Infektionen bei Nutztieren zu verhindern, hat aber in den letzten zehn Jahren Aufmerksamkeit dafür erregt, dass es Krebszellen töten kann, insbesondere Krebsstammzellen. Anders als die meisten Chemotherapeutika, die meist über einen dominanten Weg wirken, kann Salinomycin mehrere kontrollierte Formen des Zelltods auslösen. Die Forscher konzentrierten sich auf drei davon: klassischen programmierten Zelltod (Apoptose), einen recycling-bezogenen Prozess (Autophagie) und eine neuere, eisenabhängige Form des Zelltods, die durch Fettschäden gesteuert wird (Ferroptose). Zu wissen, welche dieser Wege bei Magenkrebs aktiviert werden, ist wichtig, denn Tumoren, die einem Weg entkommen, könnten einem anderen weiterhin empfindlich gegenüberstehen.
Wie Tumorzellen ihren Todesweg wählen
Das Team testete Salinomycin an vier verschiedenen humanen Magenkrebszelllinien, die die bei Patienten sichtbare Vielfalt repräsentieren. Sie fanden heraus, dass dasselbe Medikament verschiedene Zellen zu unterschiedlichen Schicksalen trieb. In zwei Zelllinien verursachte Salinomycin überwiegend Apoptose, bei der Zellen sich still und geordnet selbst abbauen. In den anderen beiden löste es Ferroptose aus, einen explosiveren Tod, der mit Eisen, reaktiven Sauerstoffspezies und Schäden an fettigen Komponenten der Zelle verbunden ist. In allen Fällen schaltete sich früh Autophagie ein, was auf einen gemeinsamen Ausgangspunkt hindeutet, von dem aus die Zellen in die eine oder andere Todesbahn gelenkt werden.
Signale, die die Todesentscheidung lenken
Bei genauerer Untersuchung maßen die Forscher Schlüsselproteine, die wie Ampeln im Inneren der Zelle wirken. In Zellen, die auf Apoptose zusteuerten, dämpfte Salinomycin Wachstums- und Überlebenssignale (wie mTOR und Survivin) und aktivierte Proteine, die Zellbestandteile zerschneiden und Mitochondrien schädigen, die Kraftwerke der Zelle. In Zellen, die Ferroptose durchliefen, reduzierte das Medikament ebenfalls mTOR und Survivin, unterdrückte darüber hinaus aber zwei wichtige Schutzfaktoren gegen Fettschäden, SLC7A11 und GPX4. Durch die Analyse von Genaktivitätsdaten identifizierten sie ein 20-Gen-Muster, das Zellen kennzeichnet, die eher zu Ferroptose als zu Apoptose neigen, was darauf hindeutet, dass die molekulare „Verdrahtung“ jedes Tumors mitbestimmt, wie er auf die Behandlung zugrunde geht.
Die Wurzeln des Rückfalls angreifen
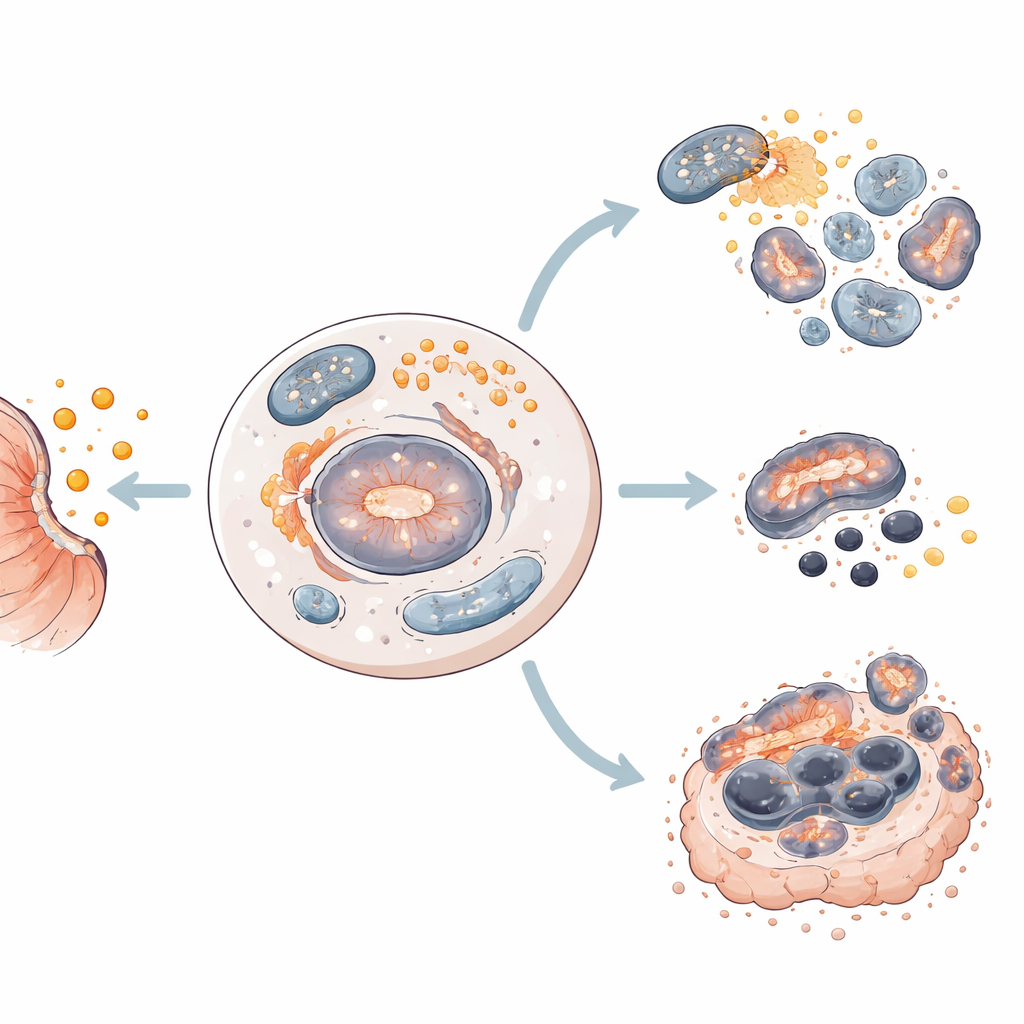
Die Studie untersuchte auch Krebsstammzellen, die über Oberflächenmarker CD44 und CD133 identifiziert wurden und mit Medikamentenresistenz sowie der Kontrolle von Ferroptose in Verbindung stehen. In den resistentesten Zelllinien waren diese stammzellähnlichen Zellen häufig, bildeten robuste 3D‑„Sphäroide“ und erzeugten viele Kolonien. Salinomycin verringerte den Anteil der Zellen mit diesen Markern deutlich, verkleinerte oder beseitigte Sphäroide und blockierte Kolonienwachstum, was darauf hindeutet, dass es gerade die Zellen angreift, die am ehesten einen Rückfall verursachen. Als das Team das ferroptosebezogene Genmuster auf große Patientendatensätze anwandte, konnten sie Gruppen mit unterschiedlichen Überlebensaussichten trennen, was zeigt, dass dieses molekulare Profil prognostischen Wert in der Praxis hat.
Den Ansatz in patientennahen Mini-Tumoren testen
Um dem klinischen Einsatz näherzukommen, testeten die Forscher Salinomycin an patientenabgeleiteten Magenkrebs-Organoiden — kleinen 3D-Strukturen, die aus menschlichen Tumorproben gezüchtet wurden und viele Eigenschaften echter Tumoren nachahmen. In allen Organoid-Modellen verringerte Salinomycin die Lebensfähigkeit und störte die Struktur. In den meisten Fällen aktivierte es apoptotische Enzyme; in einem Modell, das keine Apoptose zeigte, löste es stattdessen typische Merkmale der Ferroptose aus, einschließlich Veränderungen der mitochondrialen Aktivität und dem Verlust schützender Ferroptose-Proteine. In allen Modellen nahm die Autophagie zu, was ihre Rolle als gemeinsamen frühen Schritt bei salinomycinindiziertem Zelltod bestätigt.
Was das für zukünftige Therapien bedeuten könnte
Insgesamt stellt diese Arbeit Salinomycin als einen „Todes-Schalter“ dar, der Magenkrebszellen entweder in apoptotische oder in ferroptotische Selbstzerstörung umschalten kann, wobei Autophagie als gemeinsames Vorspiel fungiert. Indem es gleichzeitig den Tumor als Masse und seinen stammzellähnlichen Kern trifft und eine alternative Todesroute anbietet, wenn der übliche Weg blockiert ist, könnte Salinomycin helfen, Multidrug-Resistenzen zu überwinden. Die hier entwickelte auf Ferroptose basierende Gen-Signatur könnte Ärzten helfen, jene Patienten zu identifizieren, die wahrscheinlich profitieren, und so den Weg für persönlichere und dauerhaftere Behandlungsstrategien bei Magenkrebs öffnen.
Zitation: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
Schlüsselwörter: Magenkrebs, Salinomycin, Krebsstammzellen, Ferroptose, Drogenresistenz