Clear Sky Science · ja
サリノマイシンを“死のスイッチ”に:胃がん細胞がどのように死を選ぶか
この研究が患者にとって重要な理由
胃がんは依然として世界で最も致死率の高いがんの一つであり、その大きな理由の一つが多くの腫瘍が標準治療薬を回避する能力を身につけることです。問題の大部分は、腫瘍が多様な細胞集団で構成されている点にあり、その中には治療後に病気を再燃させる小さく頑強な集団、いわゆるがん幹細胞が含まれます。本研究は、古くからの獣医用薬剤であるサリノマイシンを用い、これらの細胞に複数の経路で死を強制することで胃がんに対抗できるかを探ったものです。
古い薬の新しい役割
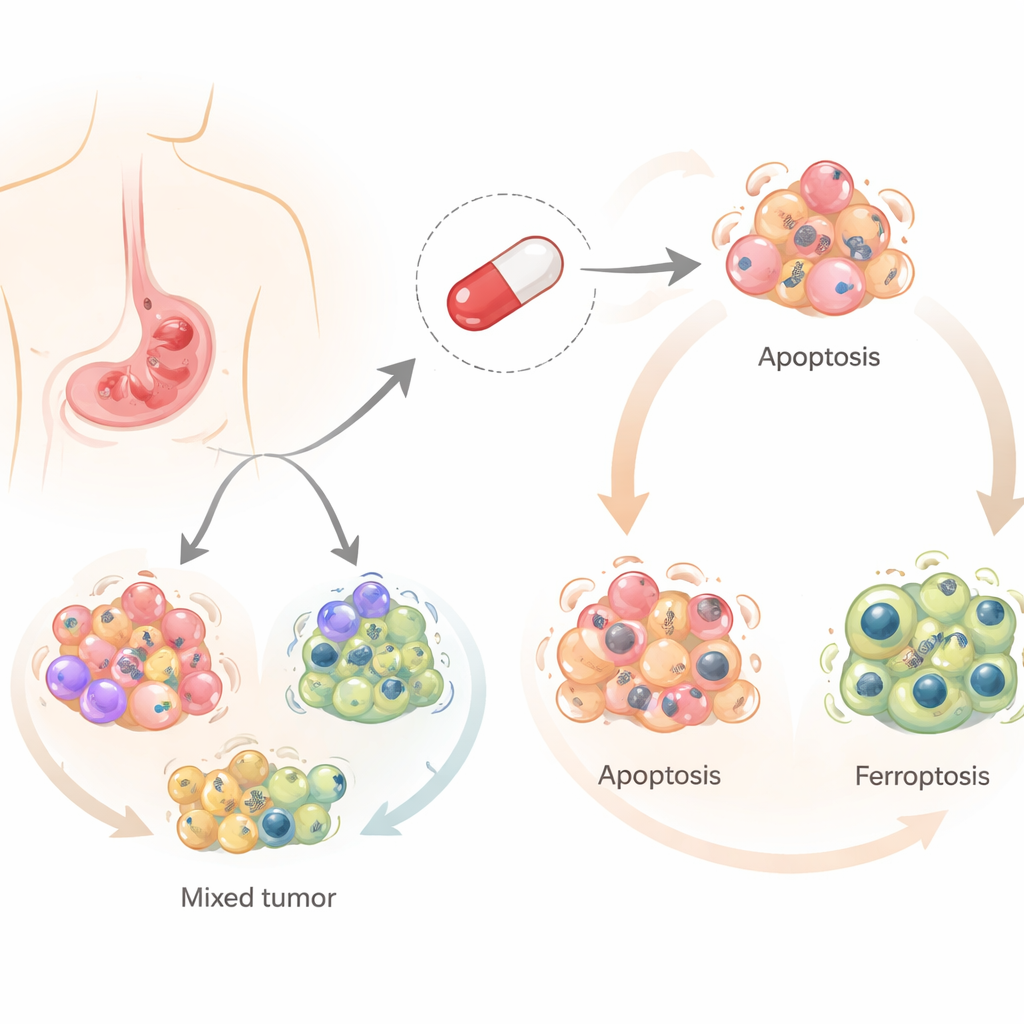
サリノマイシンはもともと家畜の感染予防のために開発されましたが、ここ10年ほどでがん細胞、特にがん幹細胞を殺す能力が注目されてきました。ほとんどの化学療法薬が通常1つの主要経路に依存して細胞を死に至らせるのに対し、サリノマイシンは複数の制御された細胞死様式を誘導できます。研究者らはそのうちの三つ—古典的なプログラム細胞死(アポトーシス)、リサイクリングに関連するプロセス(オートファジー)、そして脂質損傷に起因する鉄依存の新しい細胞死(フェロトーシス)—に着目しました。胃がんでどの経路が活性化されるかを理解することは重要です。なぜなら、ある経路を回避する腫瘍でも別の経路には脆弱である可能性があるからです。
腫瘍細胞はどのように死の道を選ぶか
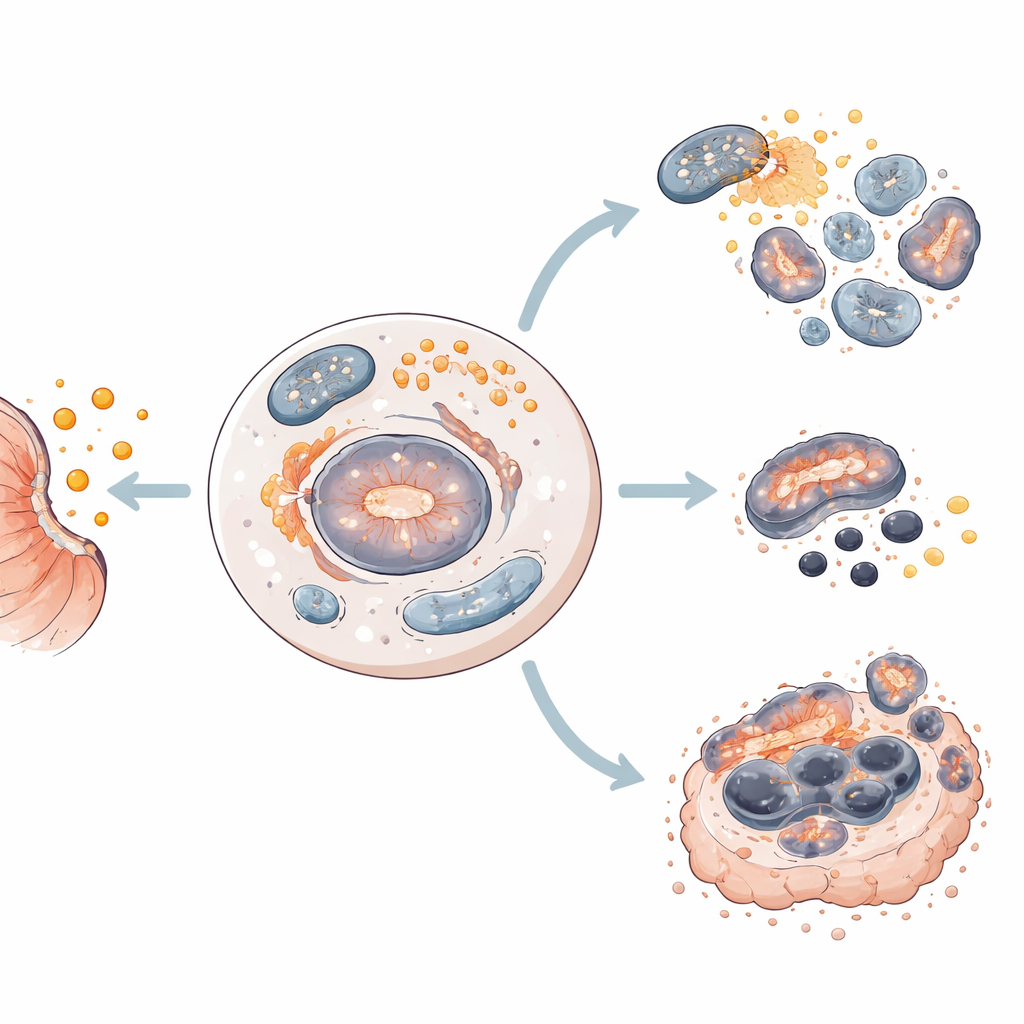
研究チームは、患者に見られる多様性を反映する四つの異なるヒト胃がん細胞株にサリノマイシンを投与しました。その結果、同じ薬剤が異なる細胞に異なる運命を押し付けることが分かりました。二つの細胞株ではサリノマイシンは主にアポトーシスを引き起こし、細胞が静かに自己を解体しました。残りの二つでは、鉄、活性酸素分子、細胞の脂質成分の損傷に結びついたより“爆発的”な死であるフェロトーシスが誘導されました。いずれのケースでもオートファジーは早期に作動しており、そこから細胞がいずれかの死の経路へと導かれる共通の出発点を示唆しています。
死の判断を導くシグナル
さらに掘り下げると、研究者らは細胞内の信号を司る主要なタンパク質を測定しました。アポトーシスへ向かう細胞では、サリノマイシンは成長や生存のシグナル(例えばmTORやsurvivin)を抑え、細胞成分を切断しミトコンドリアを損傷するタンパク質を活性化しました。フェロトーシスが起きる細胞では、薬剤は同様にmTORとsurvivinを低下させる一方で、脂質損傷から保護する重要な因子であるSLC7A11とGPX4も抑制しました。遺伝子発現データを解析することで、アポトーシスよりもフェロトーシスに傾きやすい細胞を示す20遺伝子のパターンを同定し、各腫瘍の分子“配線”が治療にどう屈するかを左右していることを示唆しました。
再発の根を狙う
研究はまた、CD44やCD133といった表面マーカーで同定されるがん幹細胞にも注目しました。これらは薬剤耐性やフェロトーシスの制御と関連しています。最も薬剤耐性の高い細胞株では、これら幹様細胞が多く存在し、堅牢な三次元“スフェロイド”を形成し、多くのコロニーを生じました。サリノマイシンはこれらのマーカーを持つ細胞の割合を大幅に減少させ、スフェロイドを縮小または消失させ、コロニー形成を阻害しました。これは再発の原因となりやすい細胞そのものを攻撃していることを示しています。さらに、フェロトーシス関連の遺伝子パターンを大規模な患者データセットに適用すると、生存見通しの異なる群に分けることができ、この分子指紋が臨床的な予後価値を持つことを示しました。
患者に近いミニ腫瘍での検証
臨床応用に近づけるため、研究者らは患者由来の胃がんオルガノイド—ヒト腫瘍試料から培養した小さな三次元構造で、実際の腫瘍の多くの特徴を模倣するもの—にサリノマイシンを投与しました。すべてのオルガノイドモデルで、サリノマイシンは生存能を低下させ、構造を破壊しました。ほとんどの場合、アポトーシス関連酵素が活性化されましたが、アポトーシスを示さないあるモデルでは代わりにミトコンドリア活性の変化や保護的フェロトーシスタンパクの喪失などフェロトーシスの特徴が認められました。すべてのモデルでオートファジーは増加し、サリノマイシン誘導の死における共通の初期段階としての役割を強化しました。
将来の治療に向けて意味するところ
総じて、本研究はサリノマイシンを胃がん細胞をアポトーシスまたはフェロトーシスのいずれかへと誘う“死のスイッチ”として描いています。オートファジーは共通の前奏であり、腫瘍の塊とその幹様コアを同時に攻撃し、通常の死の経路が遮断された場合に代替経路を提供することで多剤耐性を克服する助けとなる可能性があります。本研究で開発されたフェロトーシスに基づく遺伝子署名は、どの患者が恩恵を受けやすいかを特定する手がかりとなり、胃がんに対するより個別化され持続的な治療戦略への道を開く可能性があります。
引用: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
キーワード: 胃がん, サリノマイシン, がん幹細胞, フェロトーシス, 薬剤耐性