Clear Sky Science · fr
La salinomycine comme interrupteur de mort : comment les cellules du cancer gastrique choisissent leur destin
Pourquoi cette recherche importe pour les patients
Le cancer de l’estomac reste l’un des cancers les plus mortels au monde, principalement parce que de nombreuses tumeurs apprennent à ignorer les traitements standards. Une grande part du problème vient du fait que les tumeurs sont composées de différents types cellulaires, y compris un petit groupe tenace appelé cellules souches cancéreuses, capables de relancer la maladie après le traitement. Cette étude examine si un ancien médicament vétérinaire, la salinomycine, peut être reconverti en nouvel outil contre le cancer gastrique en forçant ces cellules à mourir selon plusieurs voies.
Un vieux médicament à une nouvelle fonction
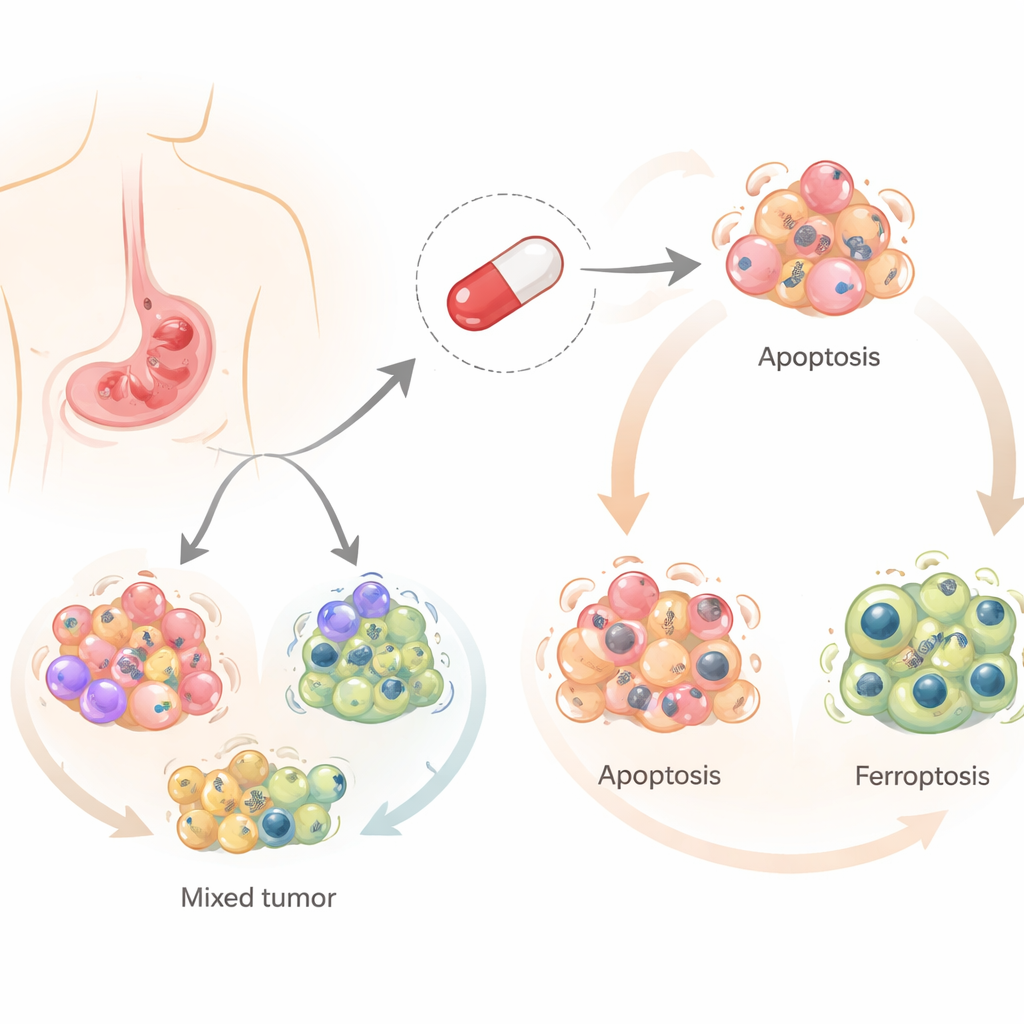
La salinomycine a été développée à l’origine pour prévenir les infections chez les animaux d’élevage, mais au cours de la dernière décennie elle a attiré l’attention pour sa capacité à tuer des cellules cancéreuses, en particulier les cellules souches tumorales. Contrairement à la plupart des chimiothérapies, qui s’appuient généralement sur une voie principale pour tuer les cellules, la salinomycine peut déclencher plusieurs formes contrôlées de mort cellulaire. Les chercheurs se sont concentrés sur trois d’entre elles : l’apoptose programmée classique, un processus lié au recyclage cellulaire (autophagie), et un type plus récent de mort dépendante du fer et liée aux dégâts lipidiques (ferroptose). Comprendre lesquelles de ces voies sont activées dans le cancer gastrique est important, car des tumeurs qui échappent à une voie peuvent rester vulnérables à une autre.
Comment les cellules tumorales choisissent leur façon de mourir
L’équipe a testé la salinomycine sur quatre lignées cellulaires humaines de cancer de l’estomac représentant la diversité observée chez les patients. Ils ont constaté que le même médicament poussait différentes cellules vers des destins différents. Dans deux lignées, la salinomycine provoquait principalement l’apoptose, où les cellules se démantèlent silencieusement. Dans les deux autres, elle induisait la ferroptose, une mort plus explosive liée au fer, aux espèces réactives de l’oxygène et aux lésions des composants lipidiques de la cellule. Dans tous les cas, l’autophagie s’activait tôt, suggérant un point de départ commun à partir duquel les cellules sont orientées vers l’une ou l’autre voie de mort.
Signaux qui guident la décision de mort
En approfondissant, les chercheurs ont mesuré des protéines clés qui fonctionnent comme des feux de circulation à l’intérieur de la cellule. Dans les cellules se dirigeant vers l’apoptose, la salinomycine a abaissé les signaux de croissance et de survie (tels que mTOR et survivine) et activé des protéines qui fragmentent le contenu cellulaire et endommagent les mitochondries, les centrales énergétiques de la cellule. Dans les cellules subissant la ferroptose, le médicament a aussi réduit mTOR et la survivine, mais a en outre supprimé deux protecteurs importants contre les dégâts lipidiques, SLC7A11 et GPX4. En analysant les données d’expression génique, ils ont identifié un motif de 20 gènes marquant les cellules prédisposées à la ferroptose plutôt qu’à l’apoptose, ce qui suggère que le « câblage » moléculaire de chaque tumeur contribue à déterminer comment elle succombera au traitement.
Cibler les racines de la récidive
L’étude a également examiné les cellules souches cancéreuses, identifiées par les marqueurs de surface CD44 et CD133, liés à la résistance aux médicaments et au contrôle de la ferroptose. Dans les lignées les plus résistantes, ces cellules de type souche étaient fréquentes, formaient des « sphéroïdes » 3D robustes et généraient de nombreuses colonies. La salinomycine a fortement réduit la fraction de cellules portant ces marqueurs, réduit ou éliminé les sphéroïdes et bloqué la formation de colonies, indiquant qu’elle attaque précisément les cellules les plus susceptibles de provoquer une rechute. Lorsque l’équipe a appliqué le motif génique lié à la ferroptose à de larges jeux de données de patients, ils ont pu séparer des groupes avec des pronostics de survie différents, montrant que cette empreinte moléculaire a une valeur pronostique en conditions réelles.
Tester l’approche sur des mini-tumeurs proches du patient
Pour se rapprocher d’une application clinique, les chercheurs ont testé la salinomycine sur des organoïdes de cancer gastrique dérivés de patients — de minuscules structures 3D cultivées à partir d’échantillons tumoraux humains qui reproduisent de nombreuses caractéristiques des vrais cancers. Dans tous les modèles d’organoïdes, la salinomycine a réduit la viabilité et perturbé la structure. Dans la plupart des cas elle a activé des enzymes apoptotiques ; dans un modèle qui ne montrait pas d’apoptose, elle a déclenché des signes de ferroptose, incluant des changements dans l’activité mitochondriale et la perte de protéines protectrices contre la ferroptose. L’autophagie a augmenté dans tous les modèles, renforçant son rôle comme étape précoce commune dans la mort induite par la salinomycine.
Ce que cela pourrait signifier pour les traitements futurs
Dans l’ensemble, ce travail présente la salinomycine comme un « interrupteur de mort » capable de basculer les cellules du cancer gastrique vers une autodestruction apoptotique ou ferroptotique, avec l’autophagie comme prélude partagé. En ciblant simultanément la masse tumorale et son noyau de type souche, et en offrant une voie de mort alternative lorsque la voie habituelle est bloquée, la salinomycine pourrait aider à surmonter la multirésistance médicamenteuse. Le signature génique basée sur la ferroptose développée ici pourrait aider les cliniciens à identifier les patients les plus susceptibles de bénéficier, ouvrant la voie à des stratégies de traitement plus personnalisées et durables contre le cancer gastrique.
Citation: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
Mots-clés: cancer gastrique, salinomycine, cellules souches cancéreuses, ferroptose, résistance aux médicaments