Clear Sky Science · pt
Salinomicina como um interruptor de morte: como as células do câncer gástrico escolhem seu destino
Por que esta pesquisa importa para os pacientes
O câncer de estômago continua sendo um dos tipos mais letais no mundo, em grande parte porque muitos tumores aprendem a ignorar os medicamentos padrão. Uma parte importante do problema é que os tumores são compostos por diferentes tipos de células, incluindo um pequeno, porém resistente, grupo chamado células-tronco do câncer, que pode reiniciar a doença após o tratamento. Este estudo investiga se um antigo medicamento veterinário, a salinomicina, pode ser convertido em uma nova arma contra o câncer gástrico ao forçar essas células a morrer de mais de uma maneira.
Um medicamento antigo com um novo papel
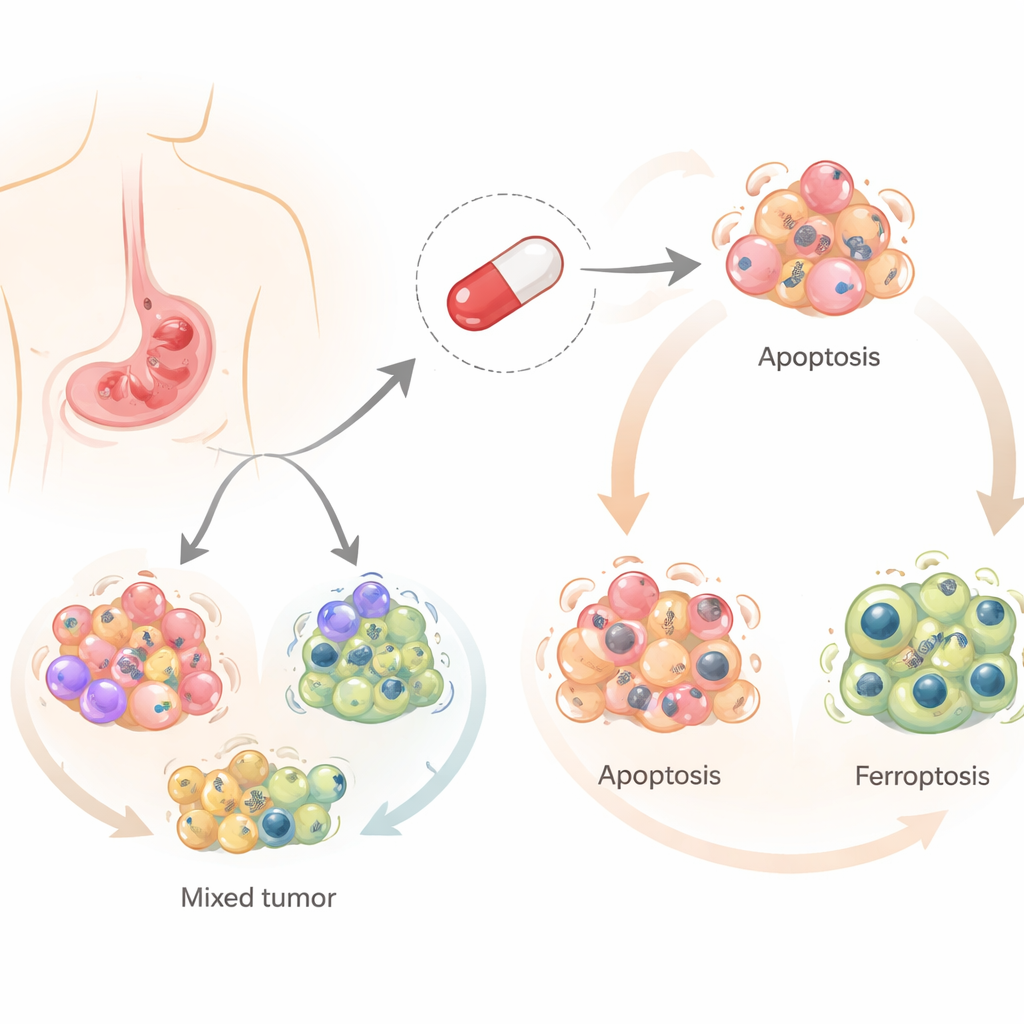
A salinomicina foi originalmente desenvolvida para prevenir infecções em animais de criação, mas na última década atraiu atenção por sua capacidade de matar células cancerosas, especialmente as células-tronco do câncer. Diferente da maioria dos quimioterápicos, que geralmente dependem de uma única via principal para matar células, a salinomicina pode desencadear várias formas controladas de morte celular. Os pesquisadores se concentraram em três dessas: a morte celular programada clássica (apoptose), um processo relacionado à reciclagem celular (autofagia) e um tipo mais recente de morte dependente de ferro, causado por dano lipídico (ferroptose). Entender quais desses caminhos são ativados no câncer gástrico é importante, porque tumores que escapam de uma rota ainda podem ser vulneráveis a outra.
Como as células tumorais escolhem sua maneira de morrer
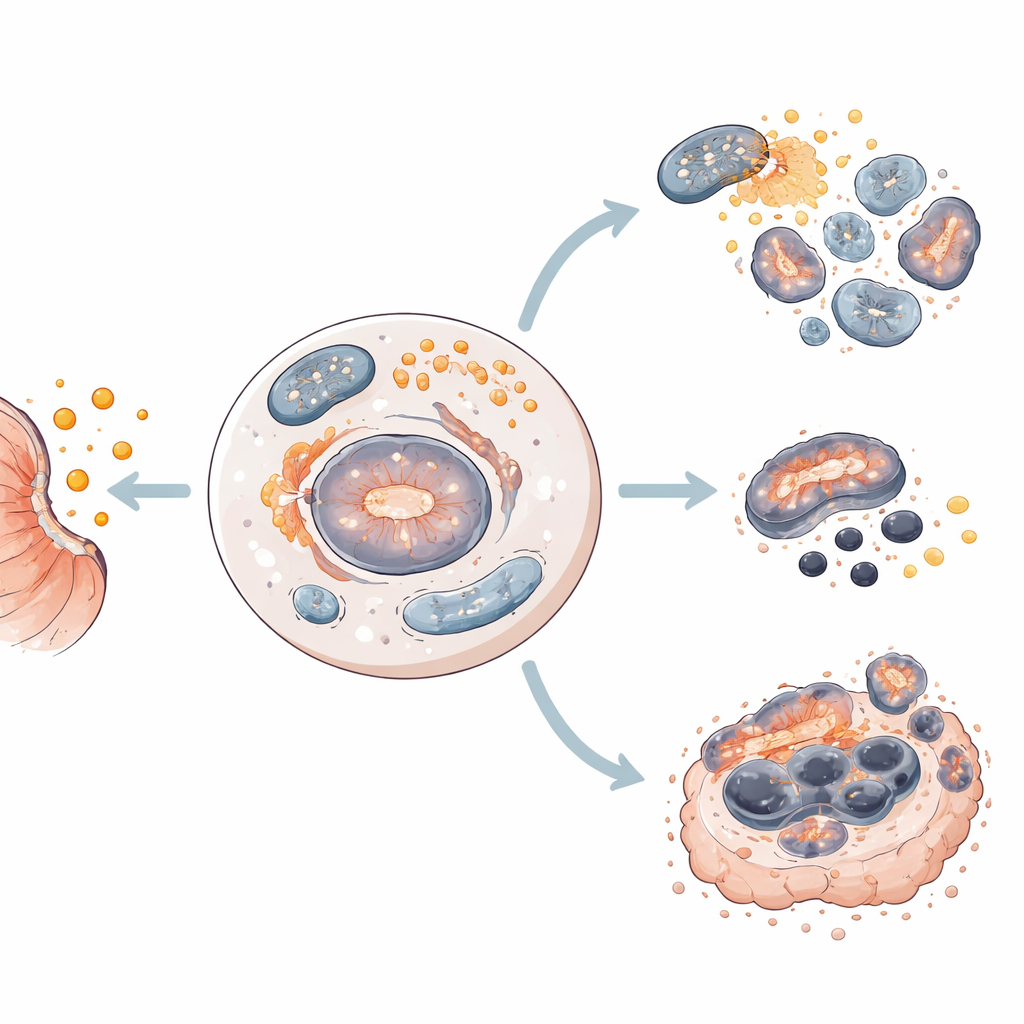
A equipe testou a salinomicina em quatro linhas celulares humanas de câncer gástrico que representam a diversidade observada em pacientes. Eles descobriram que o mesmo fármaco empurrava células diferentes para destinos distintos. Em duas linhas celulares, a salinomicina causou principalmente apoptose, em que as células se desmontam silenciosamente. Nas outras duas, ela induziu ferroptose, uma morte mais explosiva ligada ao ferro, moléculas reativas de oxigênio e dano aos componentes lipídicos da célula. Em todos os casos, a autofagia foi ativada cedo, sugerindo um ponto de partida compartilhado a partir do qual as células são direcionadas para uma rota de morte ou outra.
Sinais que orientam a decisão de morte
Ao aprofundar, os pesquisadores mediram proteínas-chave que agem como semáforos dentro da célula. Nas células dirigidas à apoptose, a salinomicina reduziu sinais de crescimento e sobrevivência (como mTOR e survivina) e ativou proteínas que degradam o conteúdo celular e danificam as mitocôndrias, as usinas de energia da célula. Nas células que sofreram ferroptose, o fármaco também reduziu mTOR e survivina, mas suprimiu dois protetores importantes contra dano lipídico, SLC7A11 e GPX4. Ao analisar dados de atividade gênica, eles identificaram um padrão de 20 genes que marca células predispostas à ferroptose em vez da apoptose, sugerindo que a “fiação” molecular de cada tumor ajuda a determinar como ele sucumbirá ao tratamento.
Alvejando as raízes da recaída
O estudo também examinou as células-tronco do câncer, identificadas por marcadores de superfície CD44 e CD133, que estão ligados à resistência a drogas e ao controle da ferroptose. Nas linhas celulares mais resistentes a medicamentos, essas células com características de tronco eram comuns, formavam robustos “esferoides” 3D e geravam muitas colônias. A salinomicina reduziu drasticamente a fração de células que carregavam esses marcadores, encolheu ou eliminou os esferoides e bloqueou o crescimento de colônias, indicando que ataca justamente as células mais propensas a causar recaída. Quando a equipe aplicou o padrão gênico relacionado à ferroptose em grandes conjuntos de dados de pacientes, eles conseguiram separar grupos com diferentes prognósticos de sobrevida, mostrando que essa assinatura molecular tem valor prognóstico no mundo real.
Testando a abordagem em mini-tumores semelhantes aos de pacientes
Para avançar em direção à clínica, os pesquisadores testaram a salinomicina em organoides de câncer gástrico derivados de pacientes — pequenas estruturas 3D cultivadas a partir de amostras tumorais humanas que imitam muitas características de tumores reais. Em todos os modelos de organoides, a salinomicina reduziu a viabilidade e perturbou a estrutura. Na maioria dos casos, ativou enzimas apoptóticas; em um modelo que não mostrou apoptose, ela desencadeou sinais de ferroptose, incluindo alterações na atividade mitocondrial e perda de proteínas protetoras contra ferroptose. A autofagia aumentou em todos os modelos, reforçando seu papel como um passo inicial comum na morte induzida pela salinomicina.
O que isso pode significar para tratamentos futuros
No conjunto, este trabalho apresenta a salinomicina como um “interruptor de morte” que pode levar as células do câncer gástrico a uma autodestruição por via apoptótica ou ferroptótica, com a autofagia como prelúdio compartilhado. Ao atingir simultaneamente o tumor em massa e seu núcleo com características de tronco, e ao oferecer uma rota alternativa de morte quando a habitual está bloqueada, a salinomicina pode ajudar a superar a resistência a múltiplos medicamentos. A assinatura gênica baseada em ferroptose desenvolvida aqui pode ajudar médicos a identificar quais pacientes têm maior probabilidade de se beneficiar, abrindo caminho para estratégias de tratamento mais personalizadas e duradouras para o câncer gástrico.
Citação: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
Palavras-chave: câncer gástrico, salinomicina, células-tronco do câncer, ferroptose, resistência a drogas