Clear Sky Science · es
Salinomicina como interruptor de muerte: cómo las células del cáncer gástrico eligen su final
Por qué esta investigación importa para los pacientes
El cáncer de estómago sigue siendo uno de los más letales del mundo, en gran parte porque muchos tumores aprenden a ignorar los fármacos estándar. Una parte importante del problema es que los tumores están formados por muchos tipos de células diferentes, incluida un pequeña pero obstinada población llamada células madre cancerosas, que pueden reiniciar la enfermedad tras el tratamiento. Este estudio explora si un viejo fármaco veterinario, la salinomicina, puede convertirse en una nueva arma contra el cáncer gástrico al forzar a estas células a morir por más de un mecanismo.
Un fármaco antiguo con un nuevo papel
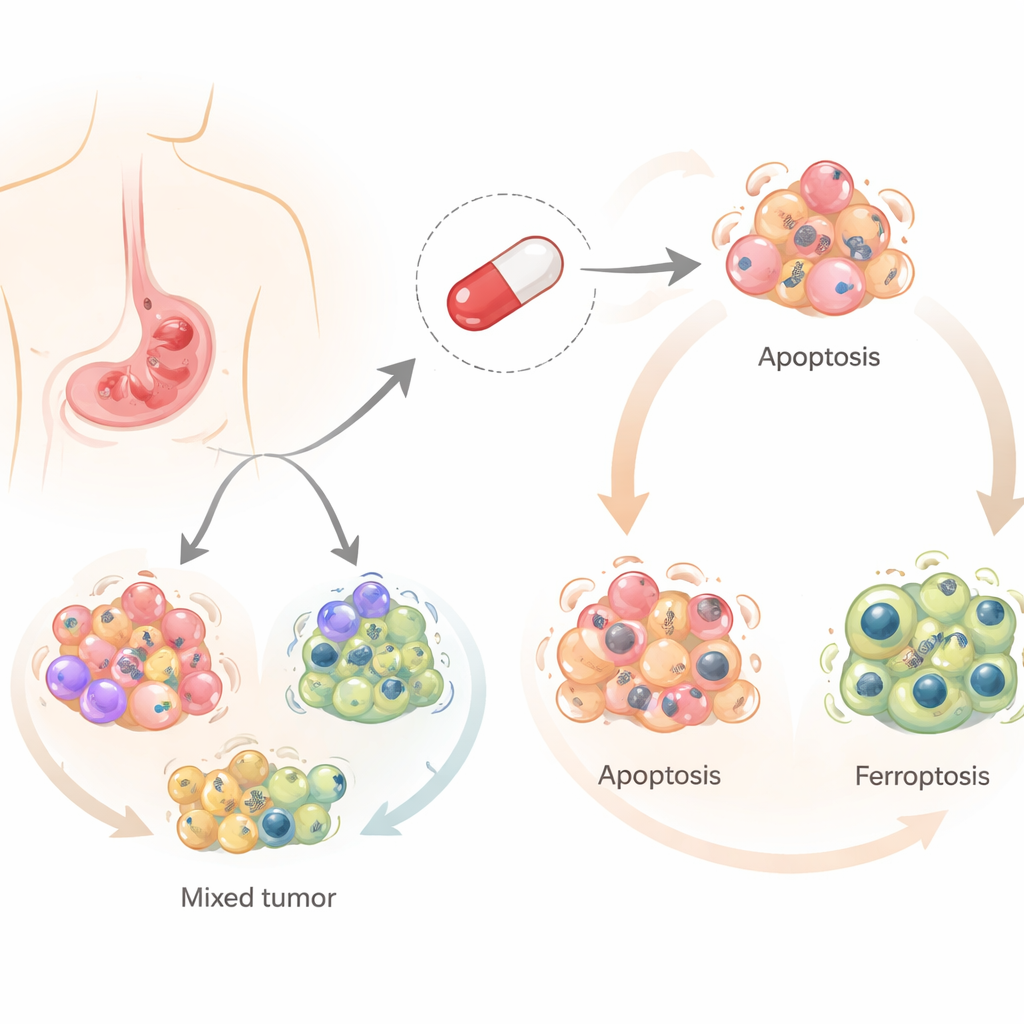
La salinomicina se desarrolló originalmente para prevenir infecciones en animales de granja, pero en la última década ha atraído atención por su capacidad para matar células cancerosas, especialmente las células madre cancerosas. A diferencia de la mayoría de los fármacos quimioterapéuticos, que suelen depender de una única vía principal para eliminar células, la salinomicina puede desencadenar varias formas reguladas de muerte celular. Los investigadores se centraron en tres de ellas: la muerte celular programada clásica (apoptosis), un proceso relacionado con el reciclaje celular (autofagia) y un tipo más reciente, dependiente del hierro, provocado por el daño a los lípidos (ferroptosis). Entender cuáles de estos caminos se activan en el cáncer gástrico es importante, porque los tumores que evitan una ruta podrían seguir siendo vulnerables a otra.
Cómo las células tumorales eligen su forma de morir
El equipo probó la salinomicina en cuatro líneas celulares humanas de cáncer gástrico que representan la diversidad observada en pacientes. Encontraron que el mismo fármaco empujaba a diferentes células hacia destinos distintos. En dos líneas celulares, la salinomicina provocó principalmente apoptosis, donde las células se desmantelan silenciosamente. En las otras dos, indujo ferroptosis, una muerte más explosiva ligada al hierro, a moléculas reactivas de oxígeno y al daño de los componentes lipídicos de la célula. En todos los casos, la autofagia se activó temprano, lo que sugiere un punto de partida común desde el cual las células se dirigen hacia una u otra vía de muerte.
Señales que guían la decisión de muerte
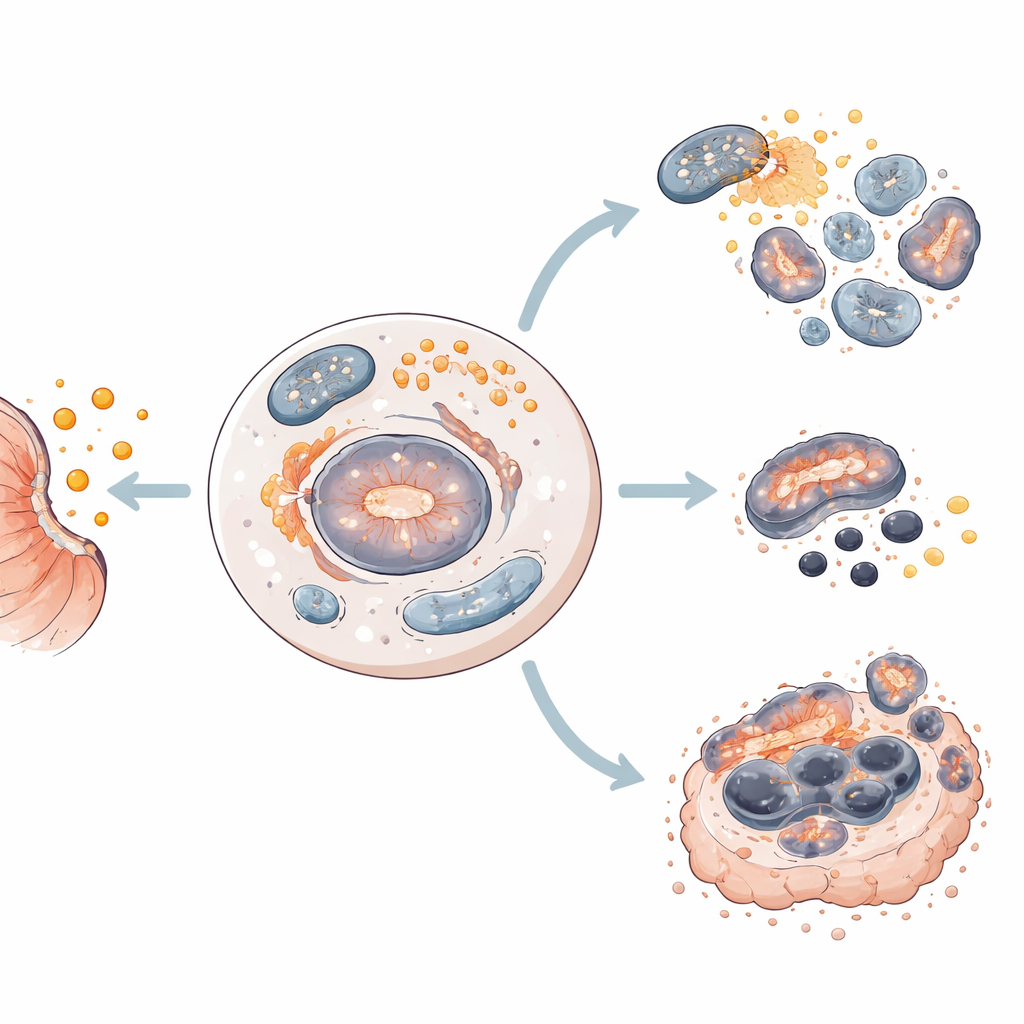
Profundizando, los investigadores midieron proteínas clave que actúan como semáforos dentro de la célula. En las células encaminadas a la apoptosis, la salinomicina redujo las señales de crecimiento y supervivencia (como mTOR y survivina) y activó proteínas que degradan el contenido celular y dañan las mitocondrias, las centrales energéticas de la célula. En las células que experimentaban ferroptosis, el fármaco también disminuyó mTOR y survivina, pero además suprimió dos protectores importantes contra el daño lipídico, SLC7A11 y GPX4. Mediante el análisis de datos de actividad génica, identificaron un patrón de 20 genes que marca a las células predispuestas a la ferroptosis en lugar de a la apoptosis, lo que sugiere que el “cableado” molecular de cada tumor ayuda a determinar cómo sucumbirá al tratamiento.
Apuntar a las raíces de la recaída
El estudio también examinó las células madre cancerosas, identificadas por los marcadores de superficie CD44 y CD133, que se asocian con resistencia a fármacos y control de la ferroptosis. En las líneas celulares más resistentes, estas células con rasgos de progenitor eran frecuentes, formaban robustos “esferoides” 3D y generaban muchas colonias. La salinomicina redujo drásticamente la fracción de células que portaban estos marcadores, encogió o eliminó los esferoides y bloqueó el crecimiento de colonias, lo que indica que ataca precisamente a las células más propensas a causar recaída. Cuando el equipo aplicó el patrón génico relacionado con la ferroptosis a grandes conjuntos de datos de pacientes, pudo separar grupos con diferentes perspectivas de supervivencia, mostrando que esta huella molecular tiene valor pronóstico en el mundo real.
Pruebas del enfoque en mini-tumores similares a los de pacientes
Para acercarse más a la clínica, los investigadores probaron la salinomicina en organoides de cáncer gástrico derivados de pacientes—pequeñas estructuras 3D cultivadas a partir de muestras tumorales humanas que imitan muchas características de los cánceres reales. En todos los modelos de organoides, la salinomicina redujo la viabilidad y alteró la estructura. En la mayoría de los casos activó enzimas apoptóticas; en un modelo que no mostró apoptosis, en cambio desencadenó características de ferroptosis, incluyendo cambios en la actividad mitocondrial y pérdida de proteínas protectoras contra la ferroptosis. La autofagia aumentó en todos los modelos, reforzando su papel como un paso temprano común en la muerte inducida por salinomicina.
Qué podría significar esto para tratamientos futuros
En conjunto, este trabajo presenta a la salinomicina como un “interruptor de muerte” que puede voltear a las células del cáncer gástrico hacia una autodestrucción apoptótica o ferroptótica, con la autofagia como preludio compartido. Al atacar simultáneamente al tumor en masa y a su núcleo con rasgos de progenitor, y al ofrecer una vía alternativa de muerte cuando la habitual está bloqueada, la salinomicina podría ayudar a superar la resistencia a múltiples fármacos. La firma génica basada en ferroptosis desarrollada aquí podría ayudar a los médicos a identificar qué pacientes tienen más probabilidades de beneficiarse, abriendo la puerta a estrategias de tratamiento más personalizadas y duraderas para el cáncer gástrico.
Cita: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
Palabras clave: cáncer gástrico, salinomicina, células madre cancerosas, ferroptosis, resistencia a fármacos