Clear Sky Science · nl
Salinomycine als doodsschakelaar: hoe maagkankercellen hun ondergang kiezen
Waarom dit onderzoek van belang is voor patiënten
Maagkanker behoort nog steeds tot de dodelijkste kankers wereldwijd, grotendeels omdat veel tumoren leren standaardmedicijnen te negeren. Een groot deel van het probleem is dat tumoren uit verschillende celtypen bestaan, waaronder een kleine maar hardnekkige groep die kankerstamcellen wordt genoemd en die de ziekte na behandeling kan doen herstarten. Deze studie onderzoekt of een oud diergeneesmiddel, salinomycine, kan worden omgevormd tot een nieuw wapen tegen maagkanker door deze cellen op meerdere manieren tot de dood te dwingen.
Een oud middel met een nieuwe taak
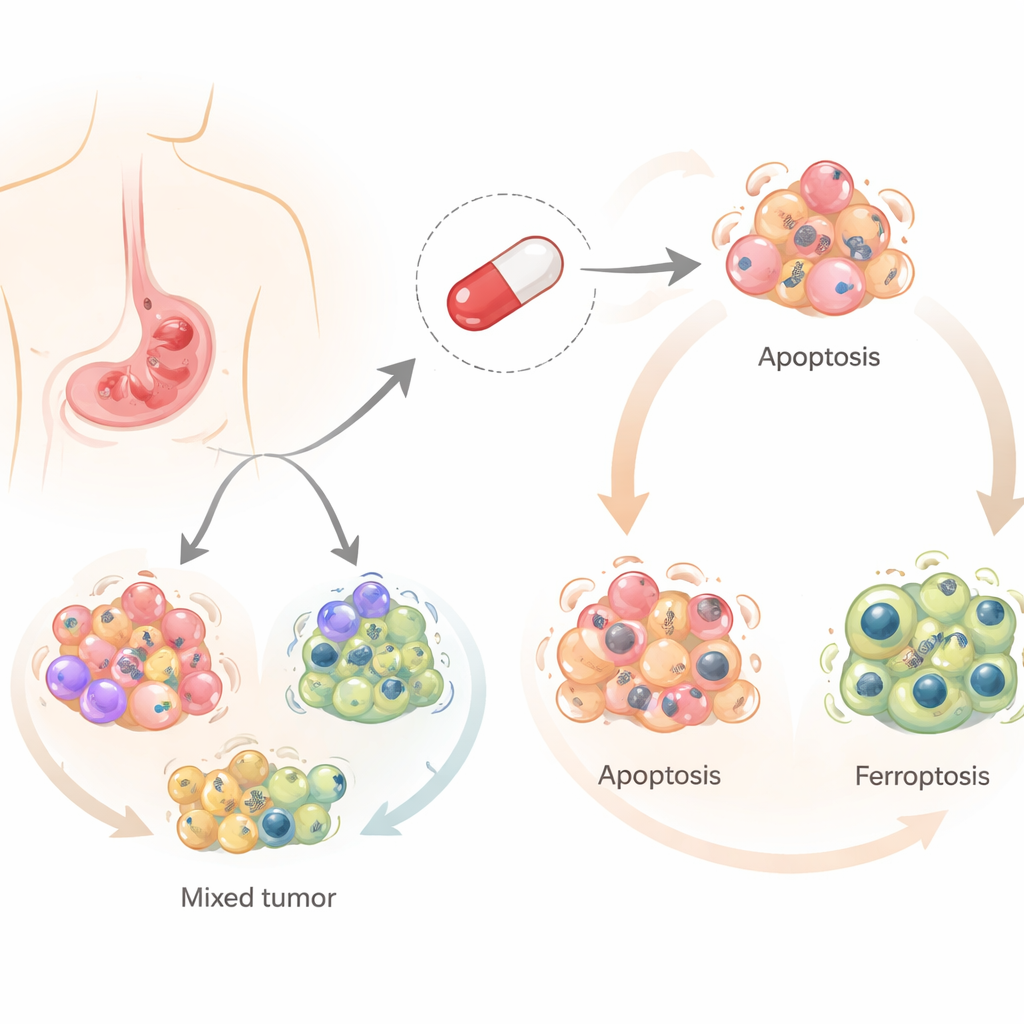
Salinomycine werd oorspronkelijk ontwikkeld om infecties bij landbouwhuisdieren te voorkomen, maar trok het afgelopen decennium aandacht vanwege zijn vermogen kankercellen te doden, met name kankerstamcellen. In tegenstelling tot de meeste chemotherapiemiddelen, die gewoonlijk via één hoofdroute cellen doden, kan salinomycine meerdere gecontroleerde vormen van celdood in gang zetten. De onderzoekers richtten zich op drie daarvan: klassieke geprogrammeerde celdood (apoptose), een recycling-gerelateerd proces (autofagie) en een nieuwere, ijzerafhankelijke vorm van dood veroorzaakt door vetbeschadiging (ferroptose). Begrijpen welke van deze paden in maagkanker geactiveerd worden is belangrijk, omdat tumoren die één route ontwijken mogelijk toch kwetsbaar zijn voor een andere.
Hoe tumorcellen hun manier van sterven kiezen
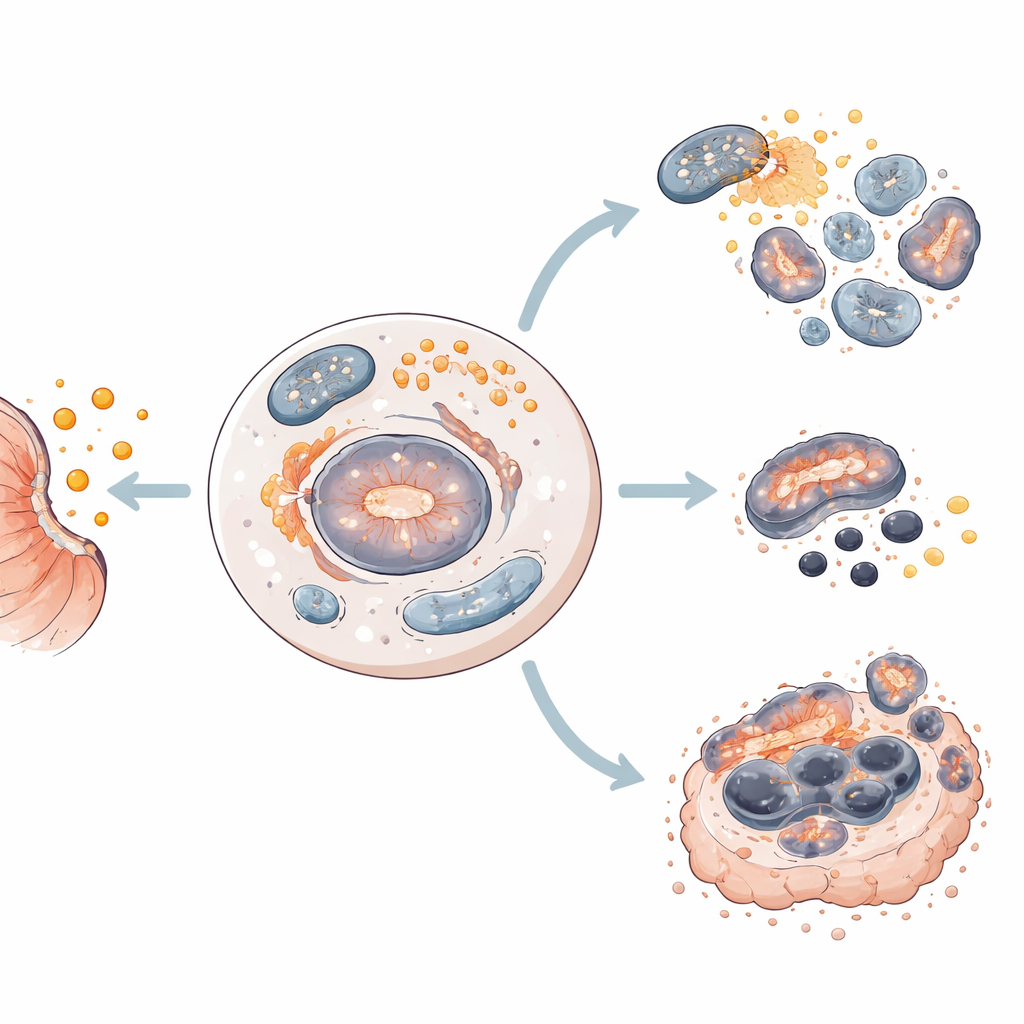
Het team testte salinomycine op vier verschillende menselijke maagkankercellijnen die de diversiteit bij patiënten weerspiegelen. Ze ontdekten dat hetzelfde middel verschillende cellen naar verschillende loten dreef. In twee cellijnen veroorzaakte salinomycine voornamelijk apoptose, waarbij cellen zichzelf rustig ontmantelen. In de andere twee leidde het tot ferroptose, een meer explosieve dood die samenhangt met ijzer, reactieve zuurstofmoleculen en beschadiging van vetachtige onderdelen van de cel. In elk geval schakelde autofagie vroegtijdig in, wat wijst op een gedeeld uitgangspunt waarvandaan cellen naar de ene of de andere doodsroute worden gestuurd.
Signalen die de doodsbeslissing sturen
Dieper gravend maten de onderzoekers sleuteleiwitten die functioneren als verkeerslichten in de cel. In cellen die naar apoptose gingen, zette salinomycine groeien overlevingssignalen (zoals mTOR en survivin) uit en activeerde eiwitten die celinhoud afbreken en mitochondriën beschadigen, de energiecentrales van de cel. In cellen die ferroptose ondergingen, verminderde het middel opnieuw mTOR en survivin, maar onderdrukte het ook twee belangrijke beschermers tegen vetbeschadiging, SLC7A11 en GPX4. Door genactiviteitsgegevens te analyseren, identificeerden ze een patroon van 20 genen dat cellen markeert die vatbaarder zijn voor ferroptose dan voor apoptose, wat suggereert dat de moleculaire ‘bekabeling’ van elke tumor mede bepaalt hoe deze aan behandeling zal bezwijken.
De wortels van terugkeer gericht aanvallen
De studie onderzocht ook kankerstamcellen, geïdentificeerd door oppervlakte-eiwitten CD44 en CD133, die gekoppeld zijn aan medicijnresistentie en controle van ferroptose. In de meest medicijnresistente cellijnen kwamen deze stamachtige cellen veel voor, vormden ze robuuste 3D-‘sferoïden’ en genereerden ze veel kolonies. Salinomycine verminderde het aandeel cellen met deze merkers scherp, liet sferoïden krimpen of verdwijnen en blokkeerde koloniegroei, wat erop wijst dat het juist de cellen aanvalt die het meest waarschijnlijk een terugkeer veroorzaken. Toen het team het ferroptose-gerelateerde genpatroon toepaste op grote patiëntendatasets, konden ze groepen onderscheiden met verschillende overlevingsvooruitzichten, wat aantoont dat deze moleculaire vingerafdruk prognostische waarde heeft in de echte wereld.
De aanpak testen in patiëntachtige mini-tumoren
Om dichter bij de kliniek te komen, testten de onderzoekers salinomycine op patiënt-afgeleide maagkanker-organoïden — kleine 3D-structuren gekweekt uit menselijke tumormonsters die veel kenmerken van echte kankers nabootsen. In alle organoïdemodellen verminderde salinomycine de levensvatbaarheid en verstoorde het de structuur. In de meeste gevallen activeerde het apoptotische enzymen; in één model dat geen apoptose toonde, wekte het in plaats daarvan kenmerken van ferroptose op, waaronder veranderingen in mitochondriale activiteit en verlies van beschermende ferroptose-eiwitten. Autofagie nam in alle modellen toe, wat de rol ervan als gemeenschappelijke vroege stap in salinomycine-geïnduceerde celdood onderstreept.
Wat dit kan betekenen voor toekomstige behandelingen
Alles bij elkaar portretteert dit werk salinomycine als een ‘doodsschakelaar’ die maagkankercellen kan omschakelen naar zowel apoptotische als ferroptotische zelfvernietiging, met autofagie als gedeeld voorspel. Door gelijktijdig de bulk van de tumor en de stamachtige kern aan te pakken, en door een alternatieve doodsroute te bieden wanneer de gebruikelijke geblokkeerd is, kan salinomycine helpen meervoudige medicijnresistentie te overwinnen. De hier ontwikkelde ferroptose-gebaseerde genhandtekening zou artsen kunnen helpen bepalen welke patiënten waarschijnlijker baat hebben, en daarmee de weg openen naar meer gepersonaliseerde en duurzame behandelstrategieën voor maagkanker.
Bronvermelding: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
Trefwoorden: maagkanker, salinomycine, kankerstamcellen, ferroptose, medicatieresistentie