Clear Sky Science · it
Salinomicina come interruttore di morte: come le cellule del cancro gastrico scelgono la loro sorte
Perché questa ricerca è importante per i pazienti
Il cancro dello stomaco rimane uno dei tumori più letali al mondo, in gran parte perché molti tumori imparano a ignorare i farmaci standard. Gran parte del problema deriva dal fatto che i tumori sono composti da diversi tipi di cellule, tra cui un piccolo ma ostinato gruppo chiamato cellule staminali tumorali, in grado di riavviare la malattia dopo il trattamento. Questo studio indaga se un vecchio farmaco veterinario, la salinomicina, possa essere trasformato in una nuova arma contro il cancro gastrico inducendo la morte di queste cellule attraverso più modalità.
Un vecchio farmaco con un nuovo ruolo
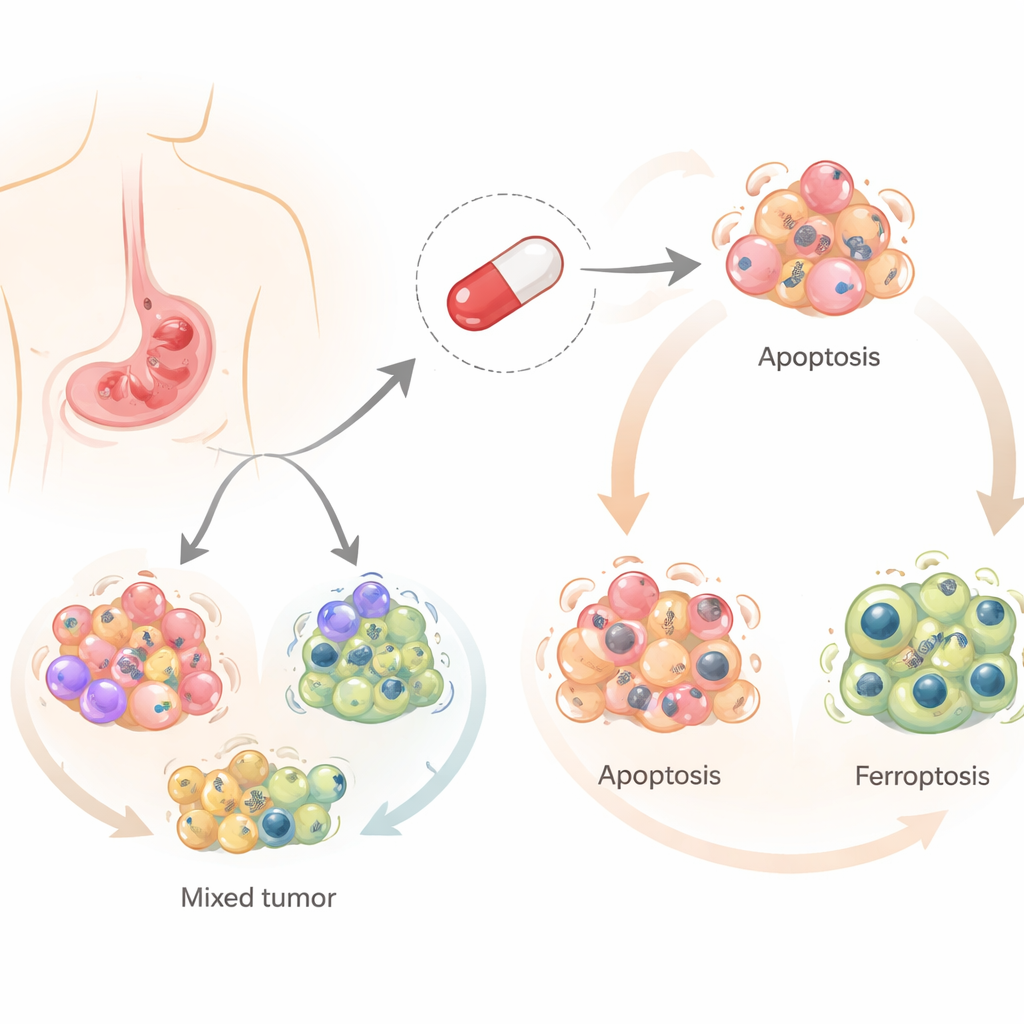
La salinomicina è stata sviluppata originariamente per prevenire infezioni negli animali da allevamento, ma nell’ultimo decennio ha attirato attenzione per la sua capacità di uccidere cellule tumorali, in particolare le cellule staminali tumorali. Diversamente dalla maggior parte dei chemioterapici, che si basano di solito su un’unica via principale per eliminare le cellule, la salinomicina può innescare diverse forme regolamentate di morte cellulare. I ricercatori si sono concentrati su tre di queste: la classica morte programmata (apoptosi), un processo legato al riciclo cellulare (autofagia) e un più recente tipo di morte dipendente dal ferro causata da danno lipidico (ferroptosi). Capire quali di questi percorsi vengono attivati nel cancro gastrico è importante, perché i tumori che sfuggono a una via potrebbero ancora essere vulnerabili a un’altra.
Come le cellule tumorali scelgono la via della morte
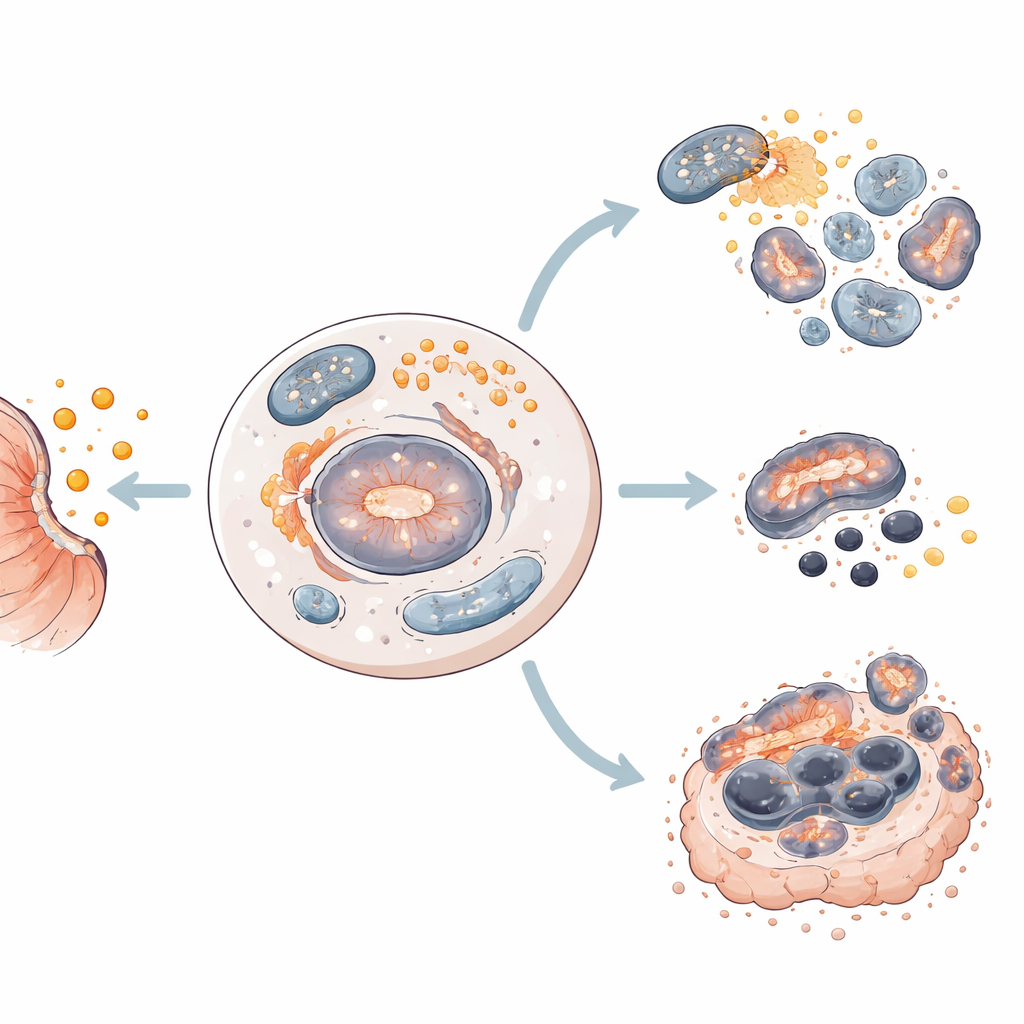
Il gruppo ha testato la salinomicina su quattro diverse linee cellulari umane di cancro gastrico che rappresentano la diversità osservata nei pazienti. Hanno scoperto che lo stesso farmaco induceva destini diversi in cellule diverse. In due linee cellulari la salinomicina provocava principalmente apoptosi, in cui le cellule si smontano in modo ordinato. Nelle altre due induceva ferroptosi, una morte più esplosiva legata al ferro, a specie reattive dell’ossigeno e al danneggiamento dei componenti lipidici della cellula. In ogni caso l’autofagia si attivava precocemente, suggerendo un punto di partenza condiviso dal quale le cellule vengono indirizzate verso una o l’altra via di morte.
Segnali che guidano la decisione di morte
Approfondendo, i ricercatori hanno misurato proteine chiave che funzionano come semafori all’interno della cellula. Nelle cellule dirette all’apoptosi, la salinomicina ha attenuato segnali di crescita e sopravvivenza (come mTOR e survivin) e ha attivato proteine che degradano il contenuto cellulare e danneggiano i mitocondri, le centrali energetiche della cellula. Nelle cellule soggette a ferroptosi, il farmaco ha nuovamente ridotto mTOR e survivin, ma ha anche soppresso due importanti protettori contro il danno lipidico, SLC7A11 e GPX4. Analizzando i dati di attività genica, gli autori hanno identificato un pattern di 20 geni che contrassegna le cellule predisposte alla ferroptosi piuttosto che all’apoptosi, suggerendo che il “cablaggio” molecolare di ciascun tumore contribuisce a determinare come soccomberà al trattamento.
Colpire le radici della recidiva
Lo studio ha esaminato anche le cellule staminali tumorali, identificate da marcatori di superficie CD44 e CD133, associati a resistenza ai farmaci e al controllo della ferroptosi. Nelle linee cellulari più resistenti ai farmaci, queste cellule di tipo staminale erano comuni, formavano robuste “sfere” 3D e generavano molte colonie. La salinomicina ha drasticamente ridotto la frazione di cellule con questi marcatori, ridotto o eliminato le sfere e bloccato la crescita delle colonie, indicando che colpisce proprio le cellule più propense a causare recidiva. Applicando il pattern genico relativo alla ferroptosi a grandi dataset di pazienti, il team è riuscito a separare gruppi con prospettive di sopravvivenza differenti, dimostrando che questa impronta molecolare ha valore prognostico nel mondo reale.
Testare l’approccio in mini-tumori simili a quelli dei pazienti
Per avvicinarsi alla clinica, i ricercatori hanno testato la salinomicina su organoidi gastrici derivati da pazienti—piccole strutture 3D cresciute da campioni tumorali umani che imitano molte caratteristiche dei tumori reali. In tutti i modelli di organoidi, la salinomicina ha ridotto la vitalità e alterato la struttura. Nella maggior parte dei casi ha attivato enzimi apoptotici; in un modello che non mostrava apoptosi ha invece innescato i segni distintivi della ferroptosi, inclusi cambiamenti nell’attività mitocondriale e perdita delle proteine protettive contro la ferroptosi. L’autofagia è aumentata in tutti i modelli, rafforzando il suo ruolo come fase precoce comune nell’induzione della morte da salinomicina.
Cosa potrebbe significare per i trattamenti futuri
Complessivamente, questo lavoro dipinge la salinomicina come un “interruttore di morte” in grado di far inclinare le cellule del cancro gastrico verso l’autodistruzione apoptotica o ferroptotica, con l’autofagia come preludio condiviso. Colpendo simultaneamente il tumore di massa e il suo nucleo di tipo staminale, e offrendo una via alternativa di morte quando quella usuale è bloccata, la salinomicina potrebbe contribuire a superare la resistenza multipla ai farmaci. La firma genica basata sulla ferroptosi sviluppata qui potrebbe aiutare i medici a individuare i pazienti più suscettibili a beneficiarne, aprendo la strada a strategie di trattamento più personalizzate e durature per il cancro gastrico.
Citazione: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
Parole chiave: cancro gastrico, salinomicina, cellule staminali tumorali, ferroptosi, resistenza ai farmaci