Clear Sky Science · ru
Салино myцин как переключатель смерти: как клетки рака желудка выбирают свою погибель
Почему это исследование важно для пациентов
Рак желудка по‑прежнему входит в число самых смертельных видов рака в мире, во многом потому, что многие опухоли научаются игнорировать стандартные препараты. Большая часть проблемы — в том, что опухоли состоят из разных типов клеток, включая небольшую, но упорную группу, называемую раковыми стволовыми клетками, которые способны возобновить болезнь после лечения. В этом исследовании изучают, можно ли старый ветеринарный препарат салино myцин превратить в новое оружие против рака желудка, заставляя эти клетки гибнуть по нескольким путям.
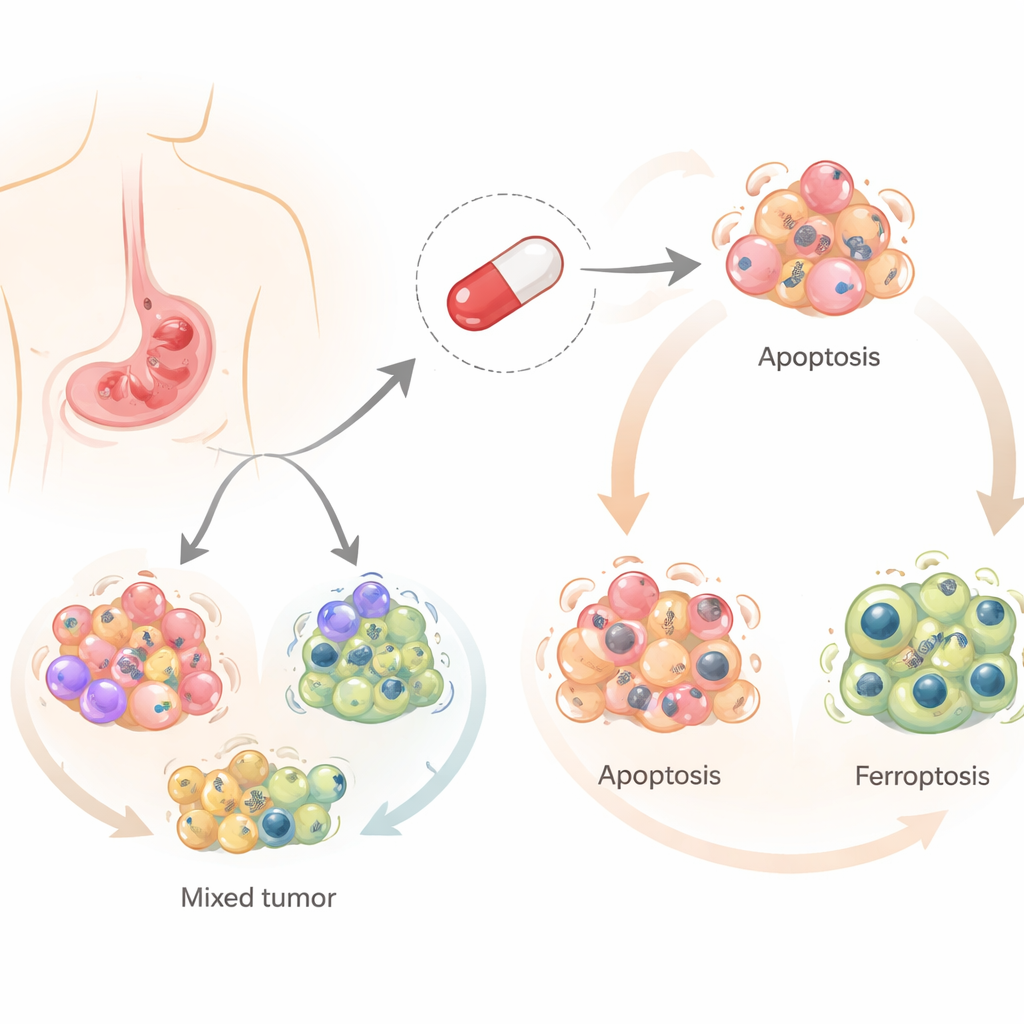
Старый препарат с новой задачей
Салиномицин первоначально разрабатывали для предотвращения инфекций у сельскохозяйственных животных, но за последнее десятилетие он привлёк внимание за способность убивать раковые клетки, особенно раковые стволовые клетки. В отличие от большинства химиотерапевтических средств, которые обычно опираются на один основной путь гибели клеток, салино myцин может запустить несколько контролируемых форм смерти клетки. Исследователи сосредоточились на трёх из них: классической программируемой клеточной смерти (апоптоз), процессе, связанном с утилизацией компонентов клетки (аутофагия), и относительно новой железозависимой форме гибели, вызванной повреждением липидов (ферроптоз). Понимание того, какие из этих путей активируются в раке желудка, важно, поскольку опухоли, избегающие одного пути, могут оставаться уязвимыми перед другим.
Как опухолевые клетки выбирают путь гибели
Команда протестировала салино myцин на четырёх различных линиях клеток человеческого рака желудка, отражающих разнообразие, наблюдаемое у пациентов. Они обнаружили, что один и тот же препарат направлял разные клетки к разным исходам. В двух линиях салино myцин преимущественно вызывал апоптоз — тихую саморазборку клетки. В других двух он индуцировал ферроптоз — более «взрывную» гибель, связанную с железом, активными формами кислорода и повреждением липидов клетки. Во всех случаях аутофагия включалась на ранней стадии, указывая на общий отправной пункт, от которого клетки направляются по тому или иному пути гибели.
Сигналы, направляющие выбор смерти
Углубляясь, исследователи измеряли ключевые белки, действующие как светофоры внутри клетки. В клетках, идущих к апоптозу, салино myцин подавлял сигналы роста и выживания (такие как mTOR и survivin) и активировал белки, разрушающие клеточный материал и повреждающие митохондрии, энергетические станции клетки. В клетках, переживающих ферроптоз, препарат также снижал mTOR и survivin, но дополнительно подавлял два важных защитника от липидного повреждения — SLC7A11 и GPX4. Анализ активности генов позволил выделить 20‑генный паттерн, характерный для клеток, склонных к ферроптозу, а не к апоптозу, что указывает на то, что молекулярная «проводка» каждой опухоли помогает предопределить, как она ответит на лечение.
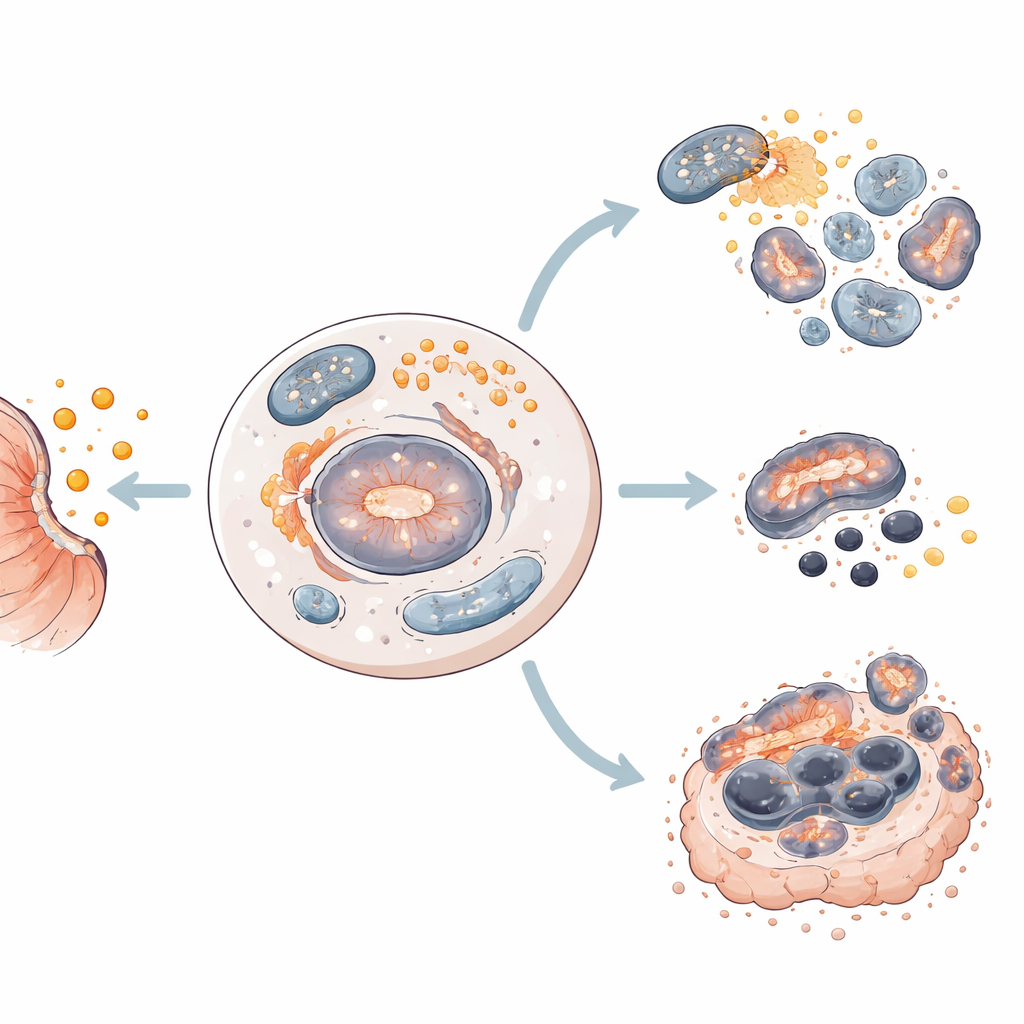
Нацеливание на корни рецидива
Исследование также рассмотрело раковые стволовые клетки, идентифицируемые поверхностными маркёрами CD44 и CD133, которые связаны с лекарственной устойчивостью и контролем ферроптоза. В наиболее резистентных линиях такие стволоподобные клетки были распространены, образовывали прочные трёхмерные «сфероиды» и давали много колоний. Салиномицин резко сокращал долю клеток с этими маркёрами, уменьшал или полностью разрушал сфероиды и блокировал рост колоний, что указывает на то, что препарат атакует те клетки, которые с наибольшей вероятностью вызовут рецидив. Применение ферроптоз‑связанного генного паттерна к большим наборам данных пациентов позволило разделить группы с разной выживаемостью, показывая, что этот молекулярный отпечаток имеет прогностическую ценность в клинической практике.
Тестирование подхода на мини‑опухолях, похожих на пациентские
Чтобы приблизиться к клинике, исследователи испытали салино myцин на органоидах рака желудка, полученных от пациентов — крошечных трёхмерных структур, выращенных из человеческих опухолевых образцов, которые имитируют многие черты настоящих опухолей. Во всех моделях органоидов салино myцин снижал жизнеспособность и нарушал структуру. В большинстве случаев он активировал апоптотические ферменты; в одной модели, где апоптоз не проявлялся, препарат вызвал признаки ферроптоза, включая изменения митохондриальной активности и потерю защитных ферроптоз‑белков. Аутофагия увеличивалась во всех моделях, что укрепляет её роль как общего раннего шага при гибели, вызванной салино myцином.
Что это может значить для будущего лечения
В целом работа представляет салино myцин как «переключатель смерти», который может переводить клетки рака желудка в состояние апоптотической или ферроптотической самоуничтожения, причём аутофагия выступает общей прелюдией. Одновременное воздействие на основную массу опухоли и её стволоподобное ядро, а также наличие альтернативного пути гибели, когда обычный заблокирован, делает салино myцин перспективным средством для преодоления мультирезистентности. Разработанная здесь ферроптоз‑основанная генная сигнатура может помочь врачам определить пациентов, которые с большей вероятностью принесут пользу, открывая путь к более персонализированным и долговременным стратегиям лечения рака желудка.
Цитирование: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
Ключевые слова: рак желудка, салиномицин, раковые стволовые клетки, ферроптоз, лекарственная устойчивость