Clear Sky Science · pl
Salinomycin jako przełącznik śmierci: jak komórki raka żołądka wybierają swoją zgubę
Dlaczego te badania mają znaczenie dla pacjentów
Rak żołądka nadal należy do najbardziej śmiertelnych nowotworów na świecie, głównie dlatego, że wiele guzów uczy się ignorować standardowe leki. Duża część problemu wynika z tego, że guz składa się z różnych typów komórek, w tym niewielkiej, lecz uporczywej populacji zwanej komórkami macierzystymi nowotworu, które mogą wznowić chorobę po leczeniu. W tym badaniu sprawdzono, czy stary lek weterynaryjny, salinomycin, można przekształcić w nowe narzędzie przeciw rakowi żołądka, zmuszając te komórki do śmierci na więcej niż jeden sposób.
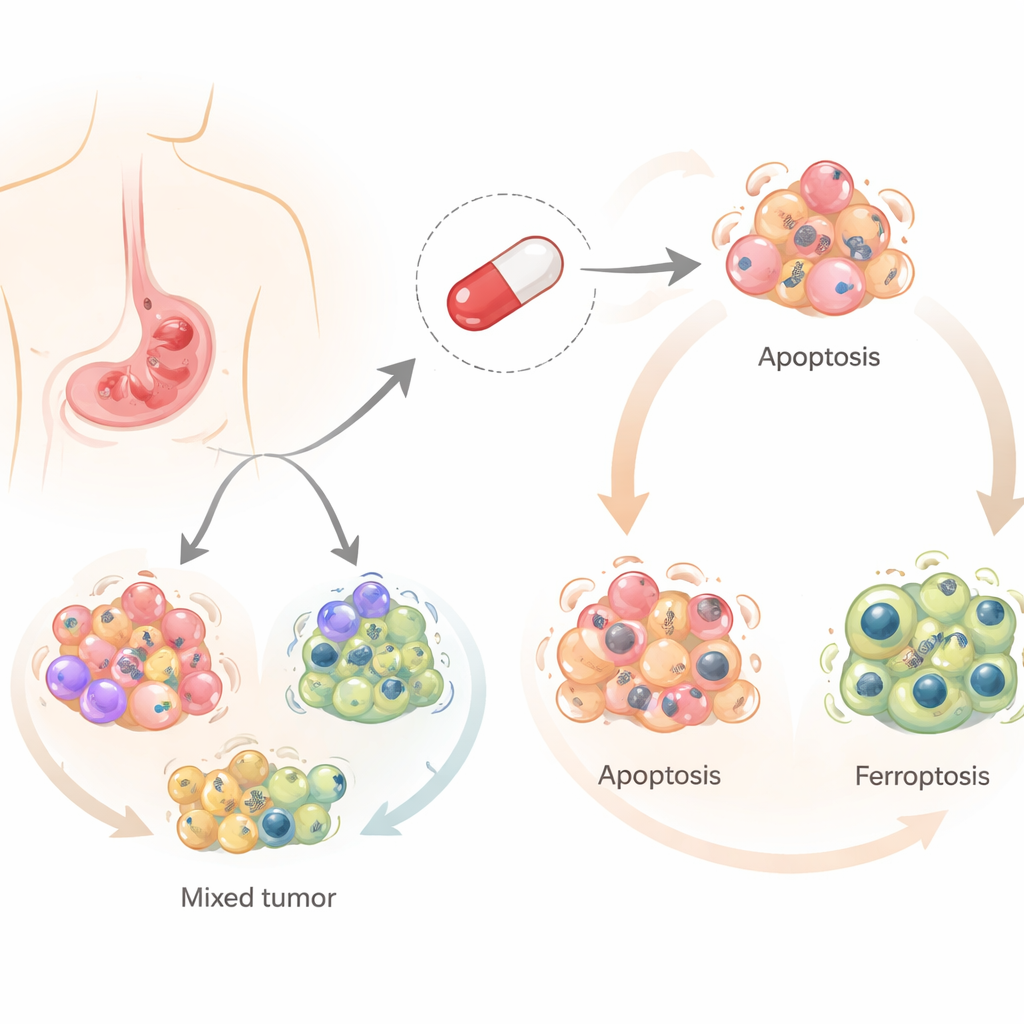
Stary lek z nową rolą
Salinomycin został pierwotnie opracowany do zapobiegania infekcjom u zwierząt gospodarskich, ale w ciągu ostatniej dekady zwrócił uwagę dzięki zdolności zabijania komórek nowotworowych, zwłaszcza komórek macierzystych nowotworu. W przeciwieństwie do większości chemioterapeutyków, które zwykle polegają na jednej dominującej ścieżce prowadzącej do śmierci komórki, salinomycin może wywoływać kilka kontrolowanych form śmierci komórkowej. Badacze skoncentrowali się na trzech z nich: klasycznej zaprogramowanej śmierci komórki (apoptozie), procesie związanym z recyklingiem (autofagii) oraz nowszym, zależnym od żelaza typie śmierci wywołanym uszkodzeniem lipidów (ferroptozie). Zrozumienie, które z tych dróg są aktywowane w raku żołądka, jest ważne, ponieważ guzy unikające jednej ścieżki mogą wciąż być wrażliwe na inną.
Jak komórki nowotworowe wybierają sposób umierania
Zespół przetestował salinomycynę na czterech różnych liniach komórkowych ludzkiego raka żołądka, które odzwierciedlają zróżnicowanie obserwowane u pacjentów. Stwierdzili, że ten sam lek popycha różne komórki ku różnym losom. W dwóch liniach salinomycin przede wszystkim indukował apoptozę, w której komórki cicho się demontują. W pozostałych dwóch prowadził do ferroptozy, bardziej „eksplozywnej” śmierci związanej z żelazem, reaktywnymi formami tlenu i uszkodzeniem lipidowych składników komórki. W każdym przypadku autofagia uruchamiała się wcześnie, co sugeruje wspólny punkt wyjścia, z którego komórki są kierowane w stronę jednej lub drugiej ścieżki śmierci.
Sygnały kierujące decyzją o śmierci
Pogłębiając analizę, badacze zmierzyli kluczowe białka pełniące rolę sygnalizacji wewnątrzkomórkowej. W komórkach zmierzających ku apoptozie salinomycin osłabił sygnały wzrostu i przeżycia (takie jak mTOR i survivin) oraz aktywował białka rozkładające komponenty komórki i uszkadzające mitochondria, elektrownie komórkowe. W komórkach przechodzących ferroptozę lek także obniżył mTOR i survivin, ale dodatkowo stłumił dwóch ważnych obrońców przed uszkodzeniem lipidów — SLC7A11 i GPX4. Analiza aktywności genów pozwoliła zidentyfikować 20-genowy wzorzec, który oznacza komórki predysponowane do ferroptozy zamiast apoptozy, co sugeruje, że molekularne „okablowanie” każdego guza pomaga określić, jak ulegnie on leczeniu.
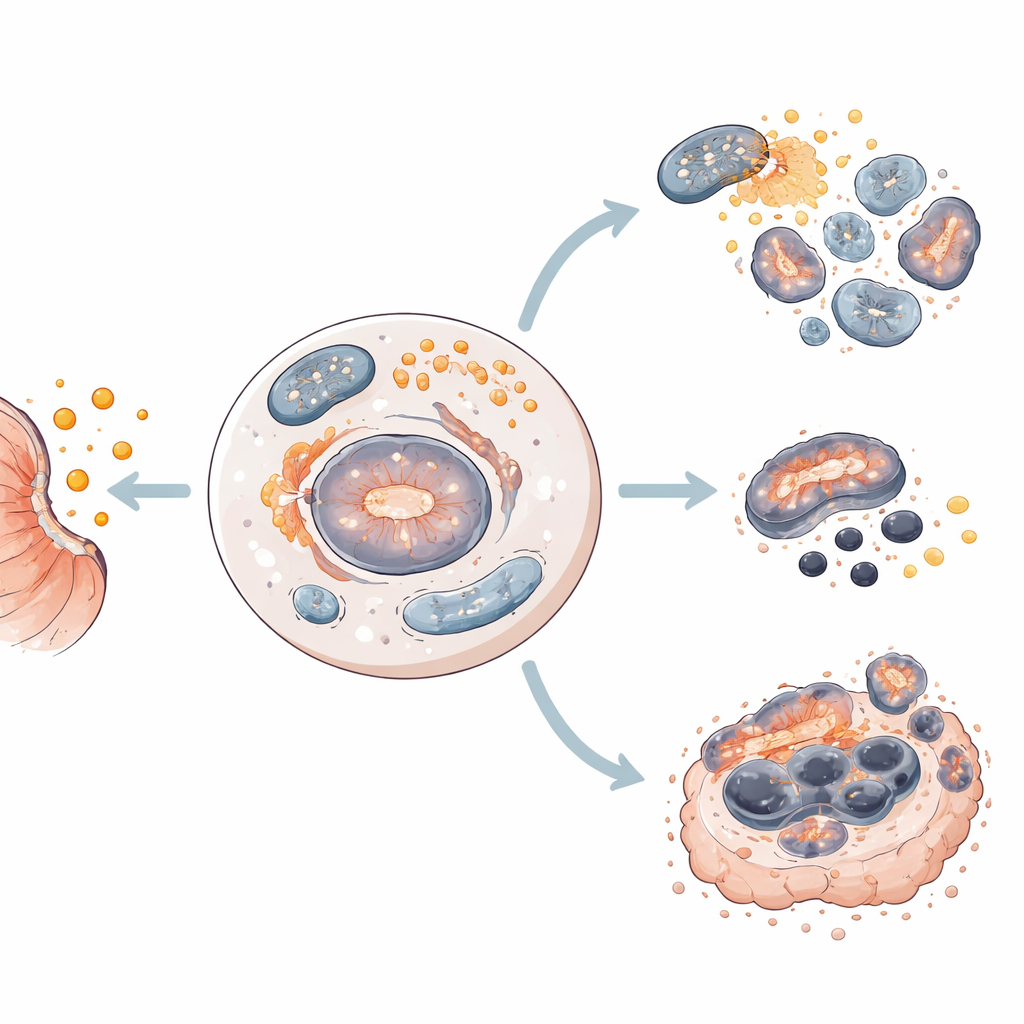
Skierowanie uwagi na źródła nawrotów
Badanie obejmowało także komórki macierzyste nowotworu, identyfikowane przez markery powierzchniowe CD44 i CD133, które wiążą się z opornością na leki i kontrolą ferroptozy. W najbardziej opornych liniach komórkowych komórki o cechach macierzystych były powszechne, tworzyły trwałe trójwymiarowe „sfereoidy” i generowały liczne kolonie. Salinomycin znacznie zmniejszył odsetek komórek noszących te markery, zmniejszył lub wyeliminował sferoidy i zablokował wzrost kolonii, co wskazuje, że atakuje on te komórki, które najprawdopodobniej powodują nawrót. Po zastosowaniu wzorca genów związanych z ferroptozą do dużych zbiorów danych pacjentów, badacze byli w stanie rozdzielić grupy o różnych rokowaniach, pokazując, że ten molekularny odcisk palca ma rzeczywistą wartość prognostyczną.
Testowanie podejścia na mini-guzach podobnych do pacjentów
Aby przybliżyć badania do praktyki klinicznej, badacze sprawdzili działanie salinomycyny na organoidach raka żołądka pochodzących od pacjentów — małych trójwymiarowych struktur hodowanych z próbek ludzkich guzów, które naśladują wiele cech prawdziwych nowotworów. We wszystkich modelach organoidów salinomycin zmniejszał żywotność i zaburzał strukturę. W większości przypadków aktywował enzymy apoptyczne; w jednym modelu, który nie wykazywał apoptozy, wywołał zamiast tego cechy ferroptozy, w tym zmiany w aktywności mitochondriów i utratę ochronnych białek przeciw ferroptozie. Autofagia zwiększyła się we wszystkich modelach, wzmacniając jej rolę jako wspólnego wczesnego etapu indukowanej przez salinomycynę śmierci.
Co to może oznaczać dla przyszłego leczenia
Podsumowując, praca ta prezentuje salinomycynę jako „przełącznik śmierci”, który może przełączać komórki raka żołądka w apoptyczną lub ferroptotyczną samozagładę, z autofagią jako wspólną introdukcją. Poprzez jednoczesne uderzenie w masę guza i jego macierzystą, odporną część oraz przez zaoferowanie alternatywnej drogi śmierci, gdy zwykła jest zablokowana, salinomycin może pomóc przezwyciężyć wielolekową oporność. Opracowany tutaj genowy sygnatur oparty na ferroptozie mógłby pomóc lekarzom wybrać pacjentów, którzy najprawdopodobniej skorzystają na takim podejściu, otwierając drogę do bardziej spersonalizowanych i trwałych strategii leczenia raka żołądka.
Cytowanie: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
Słowa kluczowe: rak żołądka, salinomycin, komórki macierzyste nowotworu, ferroptoza, oporność na leki