Clear Sky Science · he
סלינומיצין כמתג מוות: כיצד תאים של סרטן הקיבה בוחרים את גורלם
מדוע המחקר הזה חשוב עבור מטופלים
סרטן הקיבה נשאר אחד הסרטנים הקטלניים ביותר בעולם, בעיקר כי גידולים רבים לומדים להתעלם מתרופות סטנדרטיות. חלק גדול מהבעיה נובע מהמגוון התאי בתוך הגידול, כולל קבוצה קטנה אך עיקשת שנקראת תאי גזע של סרטן, שיכולה להפעיל מחדש את המחלה לאחר טיפול. המחקר בוחן האם תרופה וטרינרית ישנה, סלינומיצין, אפשר להפוך לנשק חדש נגד סרטן הקיבה על ידי הכרחת תאים אלה למות ביותר מאופן אחד.
תרופה ישנה עם תפקיד חדש
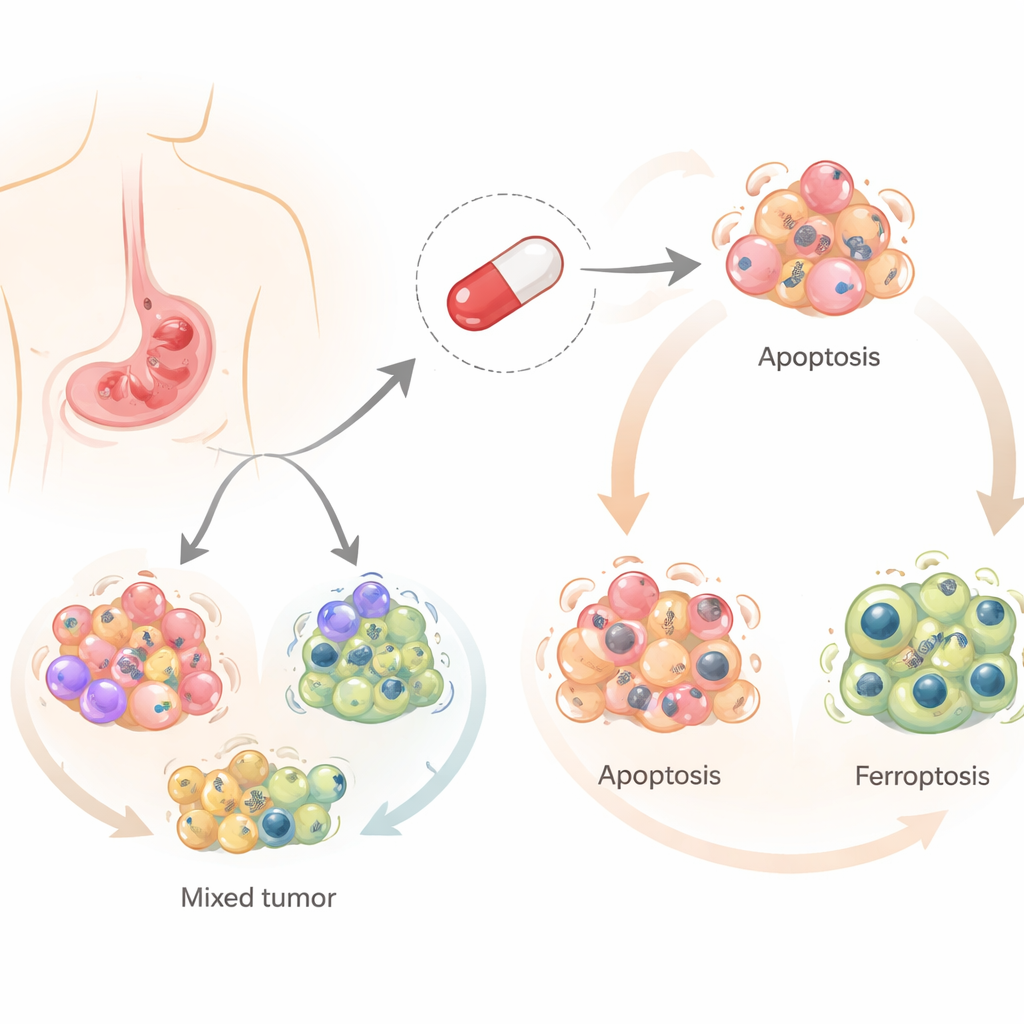
סלינומיצין פותח במקור למניעת זיהומים בבעלי חיים חקלאיים, אך בעשור האחרון זכה לתשומת לב בשל יכולתו להרוג תאי סרטן, ובפרט תאי גזע סרטניים. בניגוד לרוב תרופות הכימותרפיה, שמתבססות בדרך כלל על מסלול מרכזי יחיד כדי להרוג תאים, סלינומיצין יכול להפעיל כמה צורות מבוקרות של מוות תאי. החוקרים התרכזו בשלוש מהן: מוות מתוכנת קלאסי (אפופטוזיס), תהליך הקשור למחזור תאי (אוטופאגיה), וסוג חדש יותר של מוות התלוי בברזל הנובע מנזק לשומנים (פרוטופטוזיס). הבנת אילו מסלולים אלו מופעלים בסרטן הקיבה חשובה, כיוון שגידולים המתחמקים ממסלול אחד עשויים להיות פגיעים לאחר.
כיצד תאי הגידול בוחרים את דרך המוות שלהם
הצוות בדק את השפעת סלינומיצין על ארבע שורות תאים אנושיות של סרטן הקיבה המייצגות את הגיוון שנצפה בחולים. הם מצאו כי אותה תרופה דחפה תאים שונים לעתידונים שונים. בשתי שורות התאים סלינומיצין גרם בעיקר לאפופטוזיס, שבו התאים פורקים את עצמם בצורה שקטה. בשתי האחרות הוא הוביל לפרוטופטוזיס, מוות יותר מערב שלשב ברזל, מולקולות חמצון ונזק לרכיבים שומניים של התא. בכל המקרים האוטופאגיה הופעלה מוקדם, דבר שמרמז על נקודת פתיחה משותפת שממנה מוסטות התאים לאחד ממסלולי המוות.
אותות שמנחים את החלטת המוות
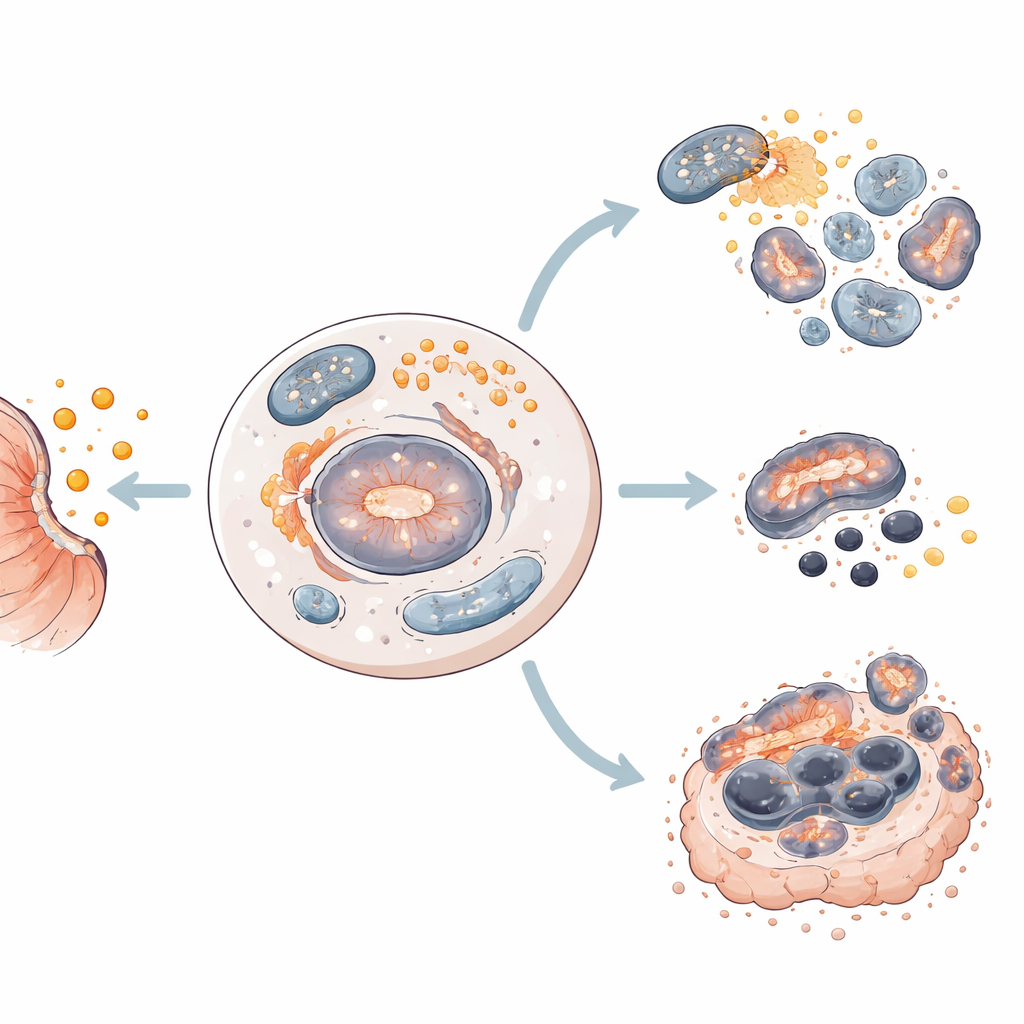
בהעמקה נוספת מדדו החוקרים חלבונים מרכזיים הפועלים כמו אורות תנועה בתוך התא. בתאים שהולכים לעבר אפופטוזיס, סלינומיצין כיבה אותות גדילה והישרדות (כגון mTOR ו-survivin) והפעיל חלבונים שפורקים תכולה תאית ומזיקים למיטוכונדריה — בתי הכוח של התא. בתאים שעברו פרוטופטוזיס התרופת שוב הקטינה mTOR ו-survivin, אך גם דיכאה שני מגינים חשובים מפני נזק שומני, SLC7A11 ו-GPX4. באמצעות ניתוח נתוני פעילות גנים זיהו החוקרים תבנית של 20 גנים שמסמנת תאים הנוטים לפרוטופטוזיס ולא לאפופטוזיס, מה שמרמז כי "החיווט" המולקולרי של כל גידול מסייע לקבוע כיצד הוא ייכנע לטיפול.
מניעת שורשי החזרה
המחקר בחן גם תאי גזע סרטניים, שזוהו על־ידי סמנים על־משטח CD44 ו-CD133, הקשורים לעמידות לתרופות ולבקרת פרוטופטוזיס. בשורות התאים העמידות ביותר התרכיזים דמויי-שורש אלה היו שכיחים, יצרו "ספירואידים" תלת־ממדיים עמידים ויצרו מושבות רבות. סלינומיצין הקטין בצורה חדה את השיעור של תאים נושאי הסמנים האלה, כיווץ או חיסל ספירואידים וחסם צמיחת מושבות, דבר המעיד שהוא תוקף את אותם תאים שסביר שיגרמו לחזרה. כאשר היישמו החוקרים את תבנית הגנים הקשורה לפרוטופטוזיס על מאגרי נתונים גדולים של חולים, הם הצליחו להפריד קבוצות עם סיכויי הישרדות שונים, מה שמראה שלטביעת האצבע המולקולרית הזו יש ערך פרוגנוסטי בעולם האמיתי.
בדיקת הגישה במיני־גידולים המדמים חולים
לצורך קירבה יותר לקליניקה, החוקרים בחנו את סלינומיצין על אורגאאידים של סרטן קיבה שמקורם בחולים — מבנים תלת־ממדיים זעירים שגודלו מדגימות גידול אנושיות ומדמים תכונות רבות של גידולים אמיתיים. בכל דגמי האורגאאיד סלינומיצין הוריד את החיוניות ופגע במבנה. ברוב המקרים הוא הפעיל אנזימי אפופטוזיס; בדגם אחד שלא הראה אפופטוזיס, הוא הלהיב סימני פרוטופטוזיס, כולל שינויים בפעילות מיטוכונדריאלית ואובדן חלבוני הגנה מפרוטופטוזיס. האוטופאגיה עלתה בכל הדגמים, מה שמחזק את תפקידה כשלב מוקדם משותף במוות המושרה על־ידי סלינומיצין.
מה זה יכול לשנות בטיפול העתידי
בסך הכל מחקר זה מציג את סלינומיצין כ"מתג מוות" שיכול להפוך תאי סרטן קיבה להריסה עצמית אפופטוטית או פרוטופטוטית, כשהאוטופאגיה משמשת כמבוא משותף. על ידי פגיעה בו-זמנית בגידול ההמוני ובגרעין הדמוי־הגזעי שלו, ובמתן מסלול מוות חלופי כשהמסלול הרגיל חסום, סלינומיצין עשוי לעזור להתגבר על עמידות מולטידראגית. חתימת הגנים מבוססת־הפרוטופטוזיס שפיתחו כאן עשויה לסייע לרופאים לזהות אילו חולים צפויים להרוויח, ולפתוח דלתות לאסטרטגיות טיפול מותאמות ועמידות יותר בסרטן הקיבה.
ציטוט: Laurenziello, P., Luongo, M., Lospinoso Severini, F. et al. Salinomycin as a death switch: how gastric cancer cells choose their demise. Cell Death Discov. 12, 171 (2026). https://doi.org/10.1038/s41420-026-03058-2
מילות מפתח: סרטן הקיבה, סלינומיצין, תאי גזע של סרטן, פרוטופטוזיס, עמידות לתרופות